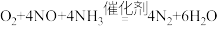高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水的处理。工业上制备高铁酸钠(Na2FeO4)的一种方法的化学原理可用离子方程式表示为:ClO-+Fe3++OH-= +Cl-+H2O(未配平)。下列说法中不正确的是
+Cl-+H2O(未配平)。下列说法中不正确的是
 +Cl-+H2O(未配平)。下列说法中不正确的是
+Cl-+H2O(未配平)。下列说法中不正确的是A. 是氧化产物 是氧化产物 |
| B.Na2FeO4中铁元素的化合价为+6价 |
| C.每生成1molNa2FeO4,反应转移6mol电子 |
D.ClO-的氧化性强于 |
更新时间:2024-03-23 20:30:48
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列关于SO2性质的预测中,不合理 的是
| A.从S元素价态看,具有氧化性 | B.从S元素价态看,具有还原性 |
| C.属于酸性氧化物,能与碱溶液反应 | D.属于酸性氧化物,能与稀硫酸反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】对于以下的反应过程,一定要加入氧化剂才能够实现的是( )
| A.O2→H2O | B.SO2→SO42- |
| C.H2SO4→CuSO4 | D.HNO3→NO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验操作,现象与结论匹配的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将缠绕铜丝灼烧后反复插入盛乙醇的试管,然后滴入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色 | 乙醇催化氧化生成乙醛 |
| B | 将装有NO2的平衡球放入热水中 | 颜色加深 | 2NO2(g) N2O4(g)ΔH>0 N2O4(g)ΔH>0 |
| C | 向含0.1mol的FeI2溶液中通入0.1molCl2,再滴加淀粉溶液 | 溶液变蓝色 | 还原性:I->Fe2+ |
| D | 向碳酸钠溶液中加入稀硫酸,反应产生的气体通入苯酚钠溶液中 | 溶液变浑浊 | 酸性:碳酸>苯酚 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】已知有如下反应:①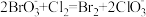 ②
②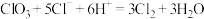 ③
③ 根据上述反应,判断下列结论中错误的是
根据上述反应,判断下列结论中错误的是
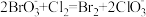 ②
②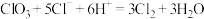 ③
③ 根据上述反应,判断下列结论中错误的是
根据上述反应,判断下列结论中错误的是A. 在反应①中作还原剂 在反应①中作还原剂 |
B. 在反应②中既是氧化产物又是还原产物 在反应②中既是氧化产物又是还原产物 |
C.氧化性的由强到弱的顺序: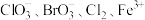 |
D.溶液中可发生反应: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列过程中对应的离子方程式正确的是
A.向含有 的溶液中通入一定量氯气发生反应,当转移电子数为 的溶液中通入一定量氯气发生反应,当转移电子数为 时: 时: |
B.向次氯酸钠溶液中通入少量 : :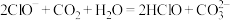 |
C.向含有 明矾 明矾 的溶液中滴加 的溶液中滴加 溶液至沉淀的物质的量最大: 溶液至沉淀的物质的量最大: |
D.向大理石上滴加浓硝酸: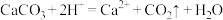 |
您最近一年使用:0次
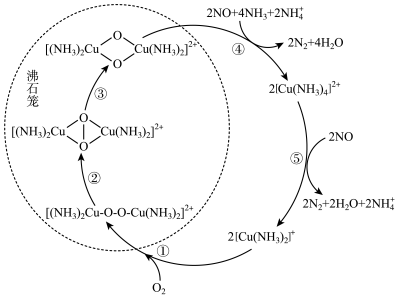
【推荐2】氧化亚铜(Cu2O)主要用于制作杀虫剂,分析试剂和红色玻璃等。其在潮湿的空气中会逐渐转化为黑色的氧化铜。以肼(N2H4)为原料与醋酸铜反应制取Cu2O的反应为4Cu(CH3COO)2+N2H4+2H2O=2Cu2O↓+N2↑+8CH3COOH,下列有关该反应的说法错误的是
| A.生成1 mol CH3COOH转移0.5 mol电子 |
| B.还原性N2H4>Cu2O |
| C.氧化产物和还原产物的物质的量之比为2:1 |
| D.沉淀用水洗后,再用乙醇洗可以除去Cu2O表面的水,防止其被氧气氧化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】2020年11月7日是被誉为“中国稀土之父”的徐光宪先生诞辰一百年纪念日。铈(Ce)是地壳中含量最高的稀土元素。金属铈在空气中易被氧化变暗,能与水反应,常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是
| A.铈元素在自然界中主要以化合态形式存在 |
B.四种稳定的核素 Ce、 Ce、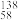 Ce、 Ce、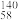 Ce、 Ce、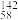 Ce,它们互称为同素异形体 Ce,它们互称为同素异形体 |
| C.铈能从硫酸铜溶液中置换出铜:Ce+2Cu2+=2Cu+Ce4+ |
| D.CeO2溶于氢碘酸的化学方程式可表示为:CeO2+4HI=CeI4+2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】NA为阿伏加德罗常数的值,下列有关说法正确的是
| A.18gD2O 中含有的质子数为 10 NA |
B.14.2g 含 σ 键的数目为 0.6 NA 含 σ 键的数目为 0.6 NA |
| C.反应2KMnO4+2KF+10HF+3H2O2=2K2MnF6+8H2O+3O2中,每有 1 mol KMnO4被还原,转移电子数为 3NA |
| D.向FeI2溶液中通入适量 Cl2,当有 1mol Fe2+被氧化时,共转移电子的数目为 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为
常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为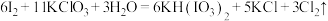 。下列说法正确的是
。下列说法正确的是
 常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为
常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为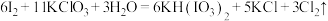 。下列说法正确的是
。下列说法正确的是A.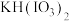 为还原产物 为还原产物 |
B.产生11.2L(标准状况) 时,转移10mol 时,转移10mol |
C.可用澄清石灰水吸收反应产生的 尾气,防止污染空气 尾气,防止污染空气 |
| D.反应中氧化剂和还原剂的物质的量之比为6∶11 |
您最近一年使用:0次

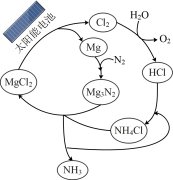
 的水溶液可得到Mg和
的水溶液可得到Mg和 既是氧化产物又是还原剂
既是氧化产物又是还原剂 是催化剂
是催化剂