I.氮、磷、砷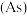 、锑
、锑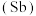 、铋
、铋 、镆
、镆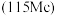 为元素周期表中原子序数依次增大的同族元素。回答下列问题:
为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)①砷的原子序数为___________ ,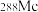 的中子数为
的中子数为___________ 。
②已知:P(s,白磷)=P(s,黑磷)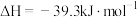 ;
;
P(s,白磷)=P(s,红磷)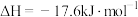 ;
;
由此推知,其中最稳定的磷单质是___________ 。
(2)氮和磷氢化物性质的比较:热稳定性
___________  (填“>”或“<”);氮和磷最高价氧化物对应水化物性质的比较:酸性
(填“>”或“<”);氮和磷最高价氧化物对应水化物性质的比较:酸性
___________  (填“>”或“<”)。
(填“>”或“<”)。
(3) 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应产物的推断正确的是
反应产物的推断正确的是___________ (填序号)。
a.能与 反应 b.含离子键、共价键 c.受热能分解产生无色气体
反应 b.含离子键、共价键 c.受热能分解产生无色气体
Ⅱ.我国力争于2030年前做到碳达峰,2060年前实现碳中和, 与
与 重整是
重整是 利用的研究热点之一、该重整反应体系主要涉及以下反应:
利用的研究热点之一、该重整反应体系主要涉及以下反应:
a.

b.

c.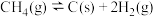

d.

e.

(4)根据盖斯定律,反应a的
___________ (写出一个代数式即可)
(5)大气中的二氧化碳主要来自于煤、石油及其它含碳化合物的燃烧。已知 时,相关物质的摩尔燃烧焓
时,相关物质的摩尔燃烧焓 数据如下表:
数据如下表:
则 时
时 和C(石墨,s)生成
和C(石墨,s)生成 的热化学方程式为
的热化学方程式为___________ 。
(6)已知
 ,当放出的热量为
,当放出的热量为 时,该反应转移电子的物质的量为
时,该反应转移电子的物质的量为___________  (用含m、n的代数式表示)。
(用含m、n的代数式表示)。
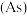 、锑
、锑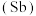 、铋
、铋 、镆
、镆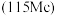 为元素周期表中原子序数依次增大的同族元素。回答下列问题:
为元素周期表中原子序数依次增大的同族元素。回答下列问题:(1)①砷的原子序数为
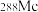 的中子数为
的中子数为②已知:P(s,白磷)=P(s,黑磷)
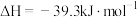 ;
;P(s,白磷)=P(s,红磷)
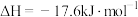 ;
;由此推知,其中最稳定的磷单质是
(2)氮和磷氢化物性质的比较:热稳定性

 (填“>”或“<”);氮和磷最高价氧化物对应水化物性质的比较:酸性
(填“>”或“<”);氮和磷最高价氧化物对应水化物性质的比较:酸性
 (填“>”或“<”)。
(填“>”或“<”)。(3)
 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应产物的推断正确的是
反应产物的推断正确的是a.能与
 反应 b.含离子键、共价键 c.受热能分解产生无色气体
反应 b.含离子键、共价键 c.受热能分解产生无色气体Ⅱ.我国力争于2030年前做到碳达峰,2060年前实现碳中和,
 与
与 重整是
重整是 利用的研究热点之一、该重整反应体系主要涉及以下反应:
利用的研究热点之一、该重整反应体系主要涉及以下反应:a.


b.


c.
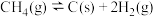

d.


e.


(4)根据盖斯定律,反应a的

(5)大气中的二氧化碳主要来自于煤、石油及其它含碳化合物的燃烧。已知
 时,相关物质的摩尔燃烧焓
时,相关物质的摩尔燃烧焓 数据如下表:
数据如下表:| 物质 |  | C(石墨,s) |  |
摩尔燃烧焓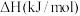 |  |  |  |
 时
时 和C(石墨,s)生成
和C(石墨,s)生成 的热化学方程式为
的热化学方程式为(6)已知

 ,当放出的热量为
,当放出的热量为 时,该反应转移电子的物质的量为
时,该反应转移电子的物质的量为 (用含m、n的代数式表示)。
(用含m、n的代数式表示)。
更新时间:2024-04-03 20:44:35
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】为推动实现碳中和的愿景,探索 资源化利用前景广阔。请按要求回答下列问题:
资源化利用前景广阔。请按要求回答下列问题:
(1)以 为基本原料可合成甲醇:
为基本原料可合成甲醇:
反应Ⅰ:

反应Ⅱ: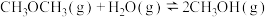

反应Ⅲ:用 (g)与
(g)与 (g)反应合成
(g)反应合成 (g),同时生成
(g),同时生成 (g)
(g)
写出反应Ⅲ的热化学方程式:___________ 。
(2)利用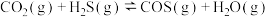 制备化工原料COS。
制备化工原料COS。
①在200℃时,将0.20mol 与0.30mol
与0.30mol  充入2.5L的空钢瓶中,4min达到平衡,体积分数
充入2.5L的空钢瓶中,4min达到平衡,体积分数 为20%。则
为20%。则
___________ ; (g)的平衡转化率
(g)的平衡转化率
___________ 平衡常数
___________ 。
②240℃重复试验,平衡后 ,该反应
,该反应
___________ 0.(填“ ”、“
”、“ ”或“
”或“ ”)
”)
(3)利用 催化加氢合成
催化加氢合成 。
。
①将过量 通入KOH溶液中充分反应,所得溶液在催化剂作用下,与
通入KOH溶液中充分反应,所得溶液在催化剂作用下,与 生成
生成 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
②其他条件不变, 的产率随温度的变化如下图所示。推测反应温度在40℃~60℃范围内,
的产率随温度的变化如下图所示。推测反应温度在40℃~60℃范围内, 的产率迅速上升可能的原因是
的产率迅速上升可能的原因是___________ 。

 资源化利用前景广阔。请按要求回答下列问题:
资源化利用前景广阔。请按要求回答下列问题:(1)以
 为基本原料可合成甲醇:
为基本原料可合成甲醇:反应Ⅰ:


反应Ⅱ:
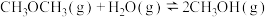

反应Ⅲ:用
 (g)与
(g)与 (g)反应合成
(g)反应合成 (g),同时生成
(g),同时生成 (g)
(g)写出反应Ⅲ的热化学方程式:
(2)利用
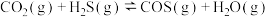 制备化工原料COS。
制备化工原料COS。①在200℃时,将0.20mol
 与0.30mol
与0.30mol  充入2.5L的空钢瓶中,4min达到平衡,体积分数
充入2.5L的空钢瓶中,4min达到平衡,体积分数 为20%。则
为20%。则
 (g)的平衡转化率
(g)的平衡转化率

②240℃重复试验,平衡后
 ,该反应
,该反应
 ”、“
”、“ ”或“
”或“ ”)
”)(3)利用
 催化加氢合成
催化加氢合成 。
。①将过量
 通入KOH溶液中充分反应,所得溶液在催化剂作用下,与
通入KOH溶液中充分反应,所得溶液在催化剂作用下,与 生成
生成 ,写出该反应的离子方程式:
,写出该反应的离子方程式:②其他条件不变,
 的产率随温度的变化如下图所示。推测反应温度在40℃~60℃范围内,
的产率随温度的变化如下图所示。推测反应温度在40℃~60℃范围内, 的产率迅速上升可能的原因是
的产率迅速上升可能的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热分别为285.8kJ·mol-1、283.0kJ·mol-1和726.5kJ·mol-1。回答下列问题:
(1)用太阳能分解100g水消耗的能量是_______ kJ。
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为____________ 。
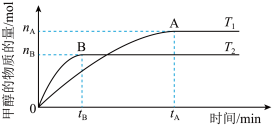
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如图所示(注:T1、T2均大于300℃);下列说法正确的是________ (填序号)。
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=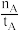 mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时 增大
增大
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为___________ 。
(5)在直接以甲醇为燃料电池中,电解质溶液为酸性,负极的反应式为_____________ 。理想状态下,该燃料电池消耗1molCH3OH所能产生的最大电能为702.1kJ,则该燃料电池的理论效率为___________ (燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)。

(1)用太阳能分解100g水消耗的能量是
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如图所示(注:T1、T2均大于300℃);下列说法正确的是
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=
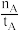 mol·L-1·min-1
mol·L-1·min-1②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时
 增大
增大(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为
(5)在直接以甲醇为燃料电池中,电解质溶液为酸性,负极的反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】甲醇(CH3OH)常温下为无色液体,是应用广泛的化工原料和前景乐观的燃料。
(1)已知:CH4(g)+H2O(g)⇌CO(g)+3H2(g) ∆H=+206.0kJ/mol-1
CH4(g)+H2O(g)⇌CH3OH(g)+H2(g) ∆H=+77.0kJ/mol-1
则CO和H2反应生成CH3OH(g)的热化学方程式是______________________ 。
(2)甲醇可用于合成3,5-二甲氧基苯酚,反应如下:
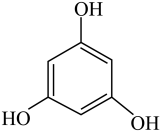 +2CH3OH
+2CH3OH
 +2H2O
+2H2O
反应结束后,先分离出甲醇,再加入乙醚,将获得的有机层(含少量氯化氢)进行洗涤,然后分离提纯得到产物。甲醇和3,5-二甲氧基苯酚的部分物理性质见表:
①分离出甲醇的操作是______________________ (填字母序号)。
a.蒸馏 b.分液 c.结晶
②洗涤时,可用于除去有机层中的氯化氢的试剂是______________________ (填字母序号)。
a.Na2CO3溶液 b.NaHCO3溶液 c.NaOH溶液
(3)甲醇可用于实验室制备丙炔酸甲酯(CH C—COOCH3,沸点为103~105℃)。
C—COOCH3,沸点为103~105℃)。
反应为:CH≡C—COOH+CH3OH CH≡C—COOCH3+H2O
CH≡C—COOCH3+H2O
实验步骤如下:
步骤1:在反应瓶中,加入14g丙炔酸、50mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
步骤2:蒸出过量的甲醇(装置如图所示)。

步骤3:反应液冷却后,依次用饱和NaCl溶液、5%Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯。
①仪器A的名称是______________ ,蒸馏烧瓶中加入碎瓷片的目的是_______________ 。
②步骤3中,用5%Na2CO3溶液洗涤,主要除去的物质是______________________ ;分离出有机相的操作名称为______________________ 。
③步骤4中,蒸馏时不能用水浴加热的原因是______________________ 。
(1)已知:CH4(g)+H2O(g)⇌CO(g)+3H2(g) ∆H=+206.0kJ/mol-1
CH4(g)+H2O(g)⇌CH3OH(g)+H2(g) ∆H=+77.0kJ/mol-1
则CO和H2反应生成CH3OH(g)的热化学方程式是
(2)甲醇可用于合成3,5-二甲氧基苯酚,反应如下:
 +2CH3OH
+2CH3OH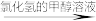
 +2H2O
+2H2O反应结束后,先分离出甲醇,再加入乙醚,将获得的有机层(含少量氯化氢)进行洗涤,然后分离提纯得到产物。甲醇和3,5-二甲氧基苯酚的部分物理性质见表:
| 物质 | 沸点/℃ | 熔点/℃ | 溶解性 |
| 甲醇 | 64.7 | -97.8 | 易溶于水 |
| 3,5-二甲氧基苯酚 | 172~175 | 33~36 | 易溶于甲醇、乙醚,微溶于水 |
①分离出甲醇的操作是
a.蒸馏 b.分液 c.结晶
②洗涤时,可用于除去有机层中的氯化氢的试剂是
a.Na2CO3溶液 b.NaHCO3溶液 c.NaOH溶液
(3)甲醇可用于实验室制备丙炔酸甲酯(CH
 C—COOCH3,沸点为103~105℃)。
C—COOCH3,沸点为103~105℃)。反应为:CH≡C—COOH+CH3OH
 CH≡C—COOCH3+H2O
CH≡C—COOCH3+H2O实验步骤如下:
步骤1:在反应瓶中,加入14g丙炔酸、50mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
步骤2:蒸出过量的甲醇(装置如图所示)。

步骤3:反应液冷却后,依次用饱和NaCl溶液、5%Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯。
①仪器A的名称是
②步骤3中,用5%Na2CO3溶液洗涤,主要除去的物质是
③步骤4中,蒸馏时不能用水浴加热的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
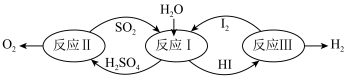
(1)已知:






反应I的热化学方程式:_______ 。
(2)反应I所得产物的溶液在碘过量时会自发分成两层。分离两层溶液的实验操作是_______ 。
(3)研究发现,通过电解方法实现反应I,既可减少碘的加入量,也可减少溶液后续纯化过程的能耗。写出通过电解法实现反应I时,阳极的电极反应式:_______ 。
(4)碘硫循环过程中反应I所制备出的HI浓度较低,必须对HI溶液进行浓缩。电解电渗析浓缩HI溶液的原理如下图所示,初始时阳极液和阴极液相同,溶液组成均为n(HI):n(H2O):n(I2)=1:6.8:2。
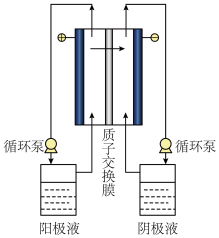
①电渗析过程中,阳极液中I2的浓度会_______ (填“增大”或“减小”)。
②结合化学用语,解释阴极区进行HI浓缩的原理_______ 。
(5)某科研小组采用双极膜电渗析法制备高浓度氢碘酸,工作原理如下图所示。

已知:双极膜在直流电场作用下可将水解离,在双极膜的两侧分别得到H+和OH-。
①X极是_______ (填“阳极”或“阴极”)。
②电解后,_______ 室获得较浓的氢碘酸(填“a”、“b”或“c”)。

(1)已知:






反应I的热化学方程式:
(2)反应I所得产物的溶液在碘过量时会自发分成两层。分离两层溶液的实验操作是
(3)研究发现,通过电解方法实现反应I,既可减少碘的加入量,也可减少溶液后续纯化过程的能耗。写出通过电解法实现反应I时,阳极的电极反应式:
(4)碘硫循环过程中反应I所制备出的HI浓度较低,必须对HI溶液进行浓缩。电解电渗析浓缩HI溶液的原理如下图所示,初始时阳极液和阴极液相同,溶液组成均为n(HI):n(H2O):n(I2)=1:6.8:2。

①电渗析过程中,阳极液中I2的浓度会
②结合化学用语,解释阴极区进行HI浓缩的原理
(5)某科研小组采用双极膜电渗析法制备高浓度氢碘酸,工作原理如下图所示。

已知:双极膜在直流电场作用下可将水解离,在双极膜的两侧分别得到H+和OH-。
①X极是
②电解后,
您最近一年使用:0次
【推荐2】实现碳达峰、碳中和是贯彻新发展理念的内在要求,因此二氧化碳的合理利用成为研究热点,有效方式之一就是二氧化碳直接加氢合成高附加值产品。
(1)一定条件下,可用二氧化碳加氢合成甲醇。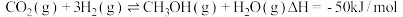 ,该反应经过以下步骤实现:
,该反应经过以下步骤实现:
Ⅰ.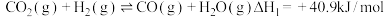
Ⅱ.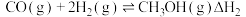
①求
②已知反应Ⅰ是整个反应的决速步,下列示意图中能体现上述反应能量变化的是___________ (填标号)。
A.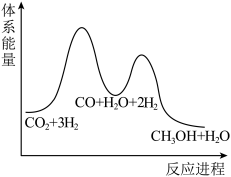
B.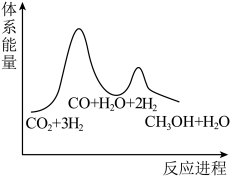
C.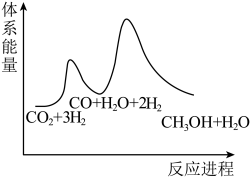
D.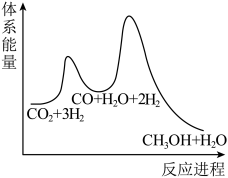
(2)一定条件下也可用二氧化碳加氢合成甲烷: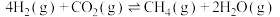 。
。
①在绝热恒容密闭容器中,一定能说明该反应达到平衡状态的是___________ (填字母)。
A.
B.相同时间内断裂 的数目与断裂
的数目与断裂 数目相等
数目相等
C.容器温度保持不变
D.当 与
与 物质的量之比保持
物质的量之比保持 不变
不变
一定温度下在 恒温恒容密闭容器中初始加入
恒温恒容密闭容器中初始加入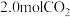 和一定量
和一定量 ,发生上述反应数据如下:
,发生上述反应数据如下:
②该温度下反应的化学平衡常数 为
为___________ 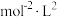
(3)一定条件下也可用二氧化碳加氢合成甲酸
①温度为 时,等物质的量的
时,等物质的量的 和
和 充入体积为
充入体积为 的恒容密闭容器中发生反应:
的恒容密闭容器中发生反应: 。实验测得:
。实验测得: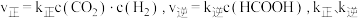 为速率常数。
为速率常数。 时,
时, 。
。
②温度从 到
到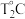 时,
时, ,则
,则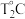 时平衡压强
时平衡压强___________ (填“ "“
"“ ”或“
”或“ ")
") 时平衡压强,理由是
时平衡压强,理由是___________ 。
(4)一定条件下可用二氧化碳提供电能,“溶解”水中的二氧化碳发生电化学反应,产生电能和氢气,其工作原理如图所示。
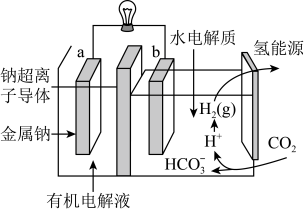
①左室有机电解液是有机溶剂加特定的盐加热制成,该装置的有机电解液___________ (填“能”或“不能”)用乙醇做溶剂。
②写出二氧化碳生成氢气的电极反应式:___________ 。
(1)一定条件下,可用二氧化碳加氢合成甲醇。
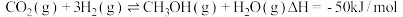 ,该反应经过以下步骤实现:
,该反应经过以下步骤实现:Ⅰ.
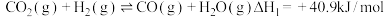
Ⅱ.
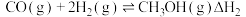
①求

②已知反应Ⅰ是整个反应的决速步,下列示意图中能体现上述反应能量变化的是
A.

B.

C.

D.

(2)一定条件下也可用二氧化碳加氢合成甲烷:
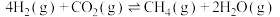 。
。①在绝热恒容密闭容器中,一定能说明该反应达到平衡状态的是
A.

B.相同时间内断裂
 的数目与断裂
的数目与断裂 数目相等
数目相等C.容器温度保持不变
D.当
 与
与 物质的量之比保持
物质的量之比保持 不变
不变一定温度下在
 恒温恒容密闭容器中初始加入
恒温恒容密闭容器中初始加入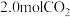 和一定量
和一定量 ,发生上述反应数据如下:
,发生上述反应数据如下: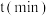 | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
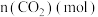 | 2.0 | 1.5 | 1.1 | 0.8 | 0.6 | 0.5 | 0.5 |
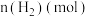 | 3.2 |
 为
为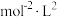
(3)一定条件下也可用二氧化碳加氢合成甲酸
①温度为
 时,等物质的量的
时,等物质的量的 和
和 充入体积为
充入体积为 的恒容密闭容器中发生反应:
的恒容密闭容器中发生反应: 。实验测得:
。实验测得: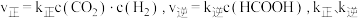 为速率常数。
为速率常数。 时,
时, 。
。②温度从
 到
到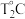 时,
时, ,则
,则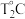 时平衡压强
时平衡压强 "“
"“ ”或“
”或“ ")
") 时平衡压强,理由是
时平衡压强,理由是(4)一定条件下可用二氧化碳提供电能,“溶解”水中的二氧化碳发生电化学反应,产生电能和氢气,其工作原理如图所示。

①左室有机电解液是有机溶剂加特定的盐加热制成,该装置的有机电解液
②写出二氧化碳生成氢气的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】汽车尾气作为空气污染的主要来源之一,其中含有大量的有害物质,包括CO、NOx、碳氢化合物和固体悬浮颗粒等。对汽车尾气的治理使环境工作者面临了巨大的挑战。试回答下列问题:
(1)用CH4催化还原NOx可以消除氮氧化物的污染。已知:
①CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ•mol-1
②CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ•mol-1
则由CH4将NO2完成还原成N2,生成CO2和水蒸气的热化学方程式是____________________ ;
(2)NOx也可被NaOH溶液吸收而生成NaNO3、NaNO2,已知某温度下,HNO2的电离常数Ka=9.7×10-4mol•L-1, 的水解常数为Kh=8.0×10-10mol•L-1,则该温度下水的离子积常数=
的水解常数为Kh=8.0×10-10mol•L-1,则该温度下水的离子积常数=______ (用含Ka、Kh的代数式表示),此时溶液的温度______ 25℃(“>”、“<”、“=”)。
(3)化工上利用CO合成甲醇,反应的热化学方程式为:CO(g)+2H2(g) CH3OH(g)△H=-90.8KJ•mol-1。不同温度下,CO的平衡转化率如右图所示:图中T1、T2、T3的高低顺序是
CH3OH(g)△H=-90.8KJ•mol-1。不同温度下,CO的平衡转化率如右图所示:图中T1、T2、T3的高低顺序是________ ,理由是______ 。 CH3OCH3(g)+H2O(g)。
CH3OCH3(g)+H2O(g)。
该反应的正反应为________ 反应(填“吸热”、“放热”),若起始是向容器Ⅰ中充入CH3OH 0.15mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向_____ 方向进行(填“正”、“逆”)。
(5)CH3OH燃料电池在便携式通讯设备、汽车等领域有着广泛的应用。已知电池工作时的总反应方程式为:2CH3OH+3O2=2CO2+4H2O,电池工作时的示意图如右图所示:_____ 电极区(填“M”、“N”),负极的电极反应式为________ 。
(1)用CH4催化还原NOx可以消除氮氧化物的污染。已知:
①CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ•mol-1
②CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ•mol-1
则由CH4将NO2完成还原成N2,生成CO2和水蒸气的热化学方程式是
(2)NOx也可被NaOH溶液吸收而生成NaNO3、NaNO2,已知某温度下,HNO2的电离常数Ka=9.7×10-4mol•L-1,
 的水解常数为Kh=8.0×10-10mol•L-1,则该温度下水的离子积常数=
的水解常数为Kh=8.0×10-10mol•L-1,则该温度下水的离子积常数=(3)化工上利用CO合成甲醇,反应的热化学方程式为:CO(g)+2H2(g)
 CH3OH(g)△H=-90.8KJ•mol-1。不同温度下,CO的平衡转化率如右图所示:图中T1、T2、T3的高低顺序是
CH3OH(g)△H=-90.8KJ•mol-1。不同温度下,CO的平衡转化率如右图所示:图中T1、T2、T3的高低顺序是
 CH3OCH3(g)+H2O(g)。
CH3OCH3(g)+H2O(g)。| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH | CH3OCH3 | H2O | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 207 | 0.20 | 0.090 | 0.090 |
(5)CH3OH燃料电池在便携式通讯设备、汽车等领域有着广泛的应用。已知电池工作时的总反应方程式为:2CH3OH+3O2=2CO2+4H2O,电池工作时的示意图如右图所示:

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某小组利用高锰酸钾与8mol/L盐酸反应制氯气并进行氯气性质的探究,实验装置如图所示:

请回答下列问题:
(1)装置F的名称是___________ 。
(2)B中制取Cl2的化学反应方程式为___________ 。
(3)根据相关实验现象就可以证明起漂白作用的不是氯气而是次氯酸,相关现象是_______ 。
(4)H处装置的作用是_______ 。
(5)实验室需要用12mol/L的浓盐酸来配制90mL8mol/L的盐酸,需该浓盐酸的体积为____ mL。
①所用的仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要的仪器是_______ 。
②对所配制的盐酸进行测定,发现其浓度偏大。配制过程中,下列各项操作可能引起该误差的原因为________ (填字母)。
A.用量筒量取浓盐酸时,仰视刻度线
B.容量瓶用蒸馏水洗涤后未经干燥
C.将稀释后的盐酸立即转入容量瓶后,并立即进行后面的实验操作
D.转移溶液时,不慎有少量溶液洒出
E.定容时,俯视容量瓶刻度线
F.颠倒摇匀后,发现液面低于刻度线,不作任何处置
G.加蒸馏水时不慎超过刻度线,用胶头滴管小心地吸去超出部分,使凹液面底部与刻度线相切
(6)卤素互化物是指不同卤素原子之间以共价键结合形成的化合物,XX′型卤素互化物与卤素单质结构相似、性质相近。右图是部分卤素单质和XX′型卤素互化物的沸点与其相对分子质量的关系图。它们的沸点随着相对分子质量的增大而升高,其原因是___________ 。试推测ICl的沸点所处的最小范围___________ 。


请回答下列问题:
(1)装置F的名称是
(2)B中制取Cl2的化学反应方程式为
(3)根据相关实验现象就可以证明起漂白作用的不是氯气而是次氯酸,相关现象是
(4)H处装置的作用是
(5)实验室需要用12mol/L的浓盐酸来配制90mL8mol/L的盐酸,需该浓盐酸的体积为
①所用的仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要的仪器是
②对所配制的盐酸进行测定,发现其浓度偏大。配制过程中,下列各项操作可能引起该误差的原因为
A.用量筒量取浓盐酸时,仰视刻度线
B.容量瓶用蒸馏水洗涤后未经干燥
C.将稀释后的盐酸立即转入容量瓶后,并立即进行后面的实验操作
D.转移溶液时,不慎有少量溶液洒出
E.定容时,俯视容量瓶刻度线
F.颠倒摇匀后,发现液面低于刻度线,不作任何处置
G.加蒸馏水时不慎超过刻度线,用胶头滴管小心地吸去超出部分,使凹液面底部与刻度线相切
(6)卤素互化物是指不同卤素原子之间以共价键结合形成的化合物,XX′型卤素互化物与卤素单质结构相似、性质相近。右图是部分卤素单质和XX′型卤素互化物的沸点与其相对分子质量的关系图。它们的沸点随着相对分子质量的增大而升高,其原因是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①~⑨九种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是________ (填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是____________ ,碱性最强的化合物的化学式是______________________________ 。
(3)最高价氧化物是两性氧化物的元素是__________ ;写出它的氧化物与氢氧化钠反应的离子方程式_________________________________________________ 。
(4)元素②形成的气态氢化物为_______________________ (填化学式),检验该气体的方法为________________ 。
(5)原子半径最大的是_______ (填元素符号),①②③三种元素气态氢化物稳定性由强到弱:____ >____ >____ (填化学式,下同)。
(6) ④和⑤⑩三种元素最高价氧化物的水化物的碱性由强到弱顺序的是:____ >____ >____ 。
(7)④⑨和⑩三种元素所形成的简单离子的半径大小次序是:_______ <_______ <________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑩ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ |
(1)在这些元素中,化学性质最不活泼的是
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)最高价氧化物是两性氧化物的元素是
(4)元素②形成的气态氢化物为
(5)原子半径最大的是
(6) ④和⑤⑩三种元素最高价氧化物的水化物的碱性由强到弱顺序的是:
(7)④⑨和⑩三种元素所形成的简单离子的半径大小次序是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2的离子化合物。
(1)写出Y2O2的电子式:_______ ,其中含有的化学键是_______ 。
(2)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是_______ (填化学式)。
(3)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是_______ (填化学式)。
(4)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式_______ 。
(1)写出Y2O2的电子式:
(2)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是
(3)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是
(4)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
您最近一年使用:0次



