前四周期元素X、Y、Z、W原子序数依次增大,X和Z同主族,基态Y原子核外电子的运动状态有9种,基态Z原子4p能级上有三个单电子,常温下W2是一种深红棕色液体。回答下列问题:
(1)基态W原子的价电子排布式为_______ ,基态X、Z原子核外电子的空间运动状态数之比为_______ 。
(2)同周期第一电离能小于X的元素有_______ 种。
(3)键角大小:XY3_______ ZY3(填“>”“=”或“<”,下同),原子半径大小:W_______ Z。
(4)ZY5中Z的价层电子对数为_______ 。
(1)基态W原子的价电子排布式为
(2)同周期第一电离能小于X的元素有
(3)键角大小:XY3
(4)ZY5中Z的价层电子对数为
更新时间:2024-04-09 12:39:43
|
相似题推荐
填空题
|
较易
(0.85)
【推荐2】1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
请回答下列问题。
(1)元素a中,含有1个质子和1个中子的核素的原子符号为_______ 。e的离子结构示意图为_______ ,元素 g在周期表中的位置为_______ 。
(2)仅由c、d组成,既含离子键又含非极性键的化合物的电子式为_______ 。
(3)非金属性,f_______ g(填“>”或“<”),能证明该结论的依据为_______ (列举一条)。
(4)写出三种简单离子a- 、d+、g- 半径由小到大的顺序:_______ (用相应的化学式表示)。
(5)写出h元素的低价氢氧化物露置在空气中发生反应的化学方程式_______ 。
| a | |||||||||||||||||
| b | c | ||||||||||||||||
| d | e | f | g | ||||||||||||||
h |
(1)元素a中,含有1个质子和1个中子的核素的原子符号为
(2)仅由c、d组成,既含离子键又含非极性键的化合物的电子式为
(3)非金属性,f
(4)写出三种简单离子a- 、d+、g- 半径由小到大的顺序:
(5)写出h元素的低价氢氧化物露置在空气中发生反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题。
(1)②表示的元素是___________ (填元素符号);
(2)①②⑤三种元素的原子半径从大到小排列为:___________ (填元素符号);
(3)③④两种元素的金属性强弱顺序为:③___________ ④(填“<”或“>”);
(4)③与②两种元素所形成化合物的阴阳离子个数比为___________ ;
(5)④和⑥两种元素组成的化合物中含有的化学键为___________ (填“离子键”或“共价键”)。
族 周期 | ⅠA | 0 | |||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | F | Ne | |||||
| 3 | ③ | Mg | ④ | Si | ⑤ | ⑥ | |||
(1)②表示的元素是
(2)①②⑤三种元素的原子半径从大到小排列为:
(3)③④两种元素的金属性强弱顺序为:③
(4)③与②两种元素所形成化合物的阴阳离子个数比为
(5)④和⑥两种元素组成的化合物中含有的化学键为
您最近一年使用:0次
【推荐1】请回答下列问题:
(1)基态氟原子核外9个电子,这些电子的电子云形状有___________ 种;氟原子有___________ 种不同能量的电子,价层电子的轨道表示式为___________ 。
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:___________ ;Cl-中有___________ 种运动状态不同的电子。
(3)某元素简化电子排布式为[Xe]4f46s2,其应在___________ 区。
(4)Li、B、H元素的电负性由大到小的排列顺序为___________ 。
(5)Li3N中氮以N3-存在,基态N3-的电子排布式为___________ ,外围电子排布为3d104s2的元素在周期表中的位置是 ___________ 。
(6)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4 ,呈正四面体结构。Ni(CO)4易溶于下列___________ 。
a.水 b.乙醇 c.C6H6(苯) d.NiSO4溶液
(1)基态氟原子核外9个电子,这些电子的电子云形状有
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:
(3)某元素简化电子排布式为[Xe]4f46s2,其应在
(4)Li、B、H元素的电负性由大到小的排列顺序为
(5)Li3N中氮以N3-存在,基态N3-的电子排布式为
(6)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4 ,呈正四面体结构。Ni(CO)4易溶于下列
a.水 b.乙醇 c.C6H6(苯) d.NiSO4溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】根据给出的原子或离子结构示意图,回答下列问题(填字母):
A.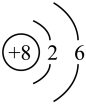 B.
B. C.
C.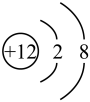 D.
D.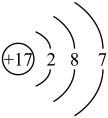
(1)电子层排布相同的是___________ 。
(2)属于同种元素的是_____________ 。
(3)属于金属元素的是___________ 。
(4)写出D参加化学反应后所得离子的结构示意图:__________ 。
A.
 B.
B. C.
C. D.
D.
(1)电子层排布相同的是
(2)属于同种元素的是
(3)属于金属元素的是
(4)写出D参加化学反应后所得离子的结构示意图:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】N、O、S的第一电离能(I1)大小为(I1N)>(I1O)>(I1S),原因是______________________ 。
您最近一年使用:0次
【推荐2】 有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下列问题:
有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下列问题:
(1)基态Co原子的价层电子排布图为_______ 。
(2) 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为_______ ;C、N、O、F的第一电离能由大到小的顺序为_______ 。
(3)碱金属离子镶入适合的冠醚空腔可形成特殊材料,两种冠醚结构如图1所示。
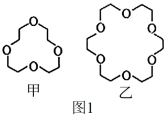
冠醚中O原子的杂化形式为_______ ;H、C、O的电负性由小到大的顺序为_______ 。
(4) 的晶胞如图2所示。处于面心的F形成正八面体空隙,Co处于体心,K处于顶点。
的晶胞如图2所示。处于面心的F形成正八面体空隙,Co处于体心,K处于顶点。

①每个晶胞中由K和F共同形成的正四面体空隙有_______ 个。
②晶胞的另一种表示中,Co处于各顶角位置,则K处于_______ 位置。
 有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下列问题:
有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下列问题:(1)基态Co原子的价层电子排布图为
(2)
 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为(3)碱金属离子镶入适合的冠醚空腔可形成特殊材料,两种冠醚结构如图1所示。

冠醚中O原子的杂化形式为
(4)
 的晶胞如图2所示。处于面心的F形成正八面体空隙,Co处于体心,K处于顶点。
的晶胞如图2所示。处于面心的F形成正八面体空隙,Co处于体心,K处于顶点。
①每个晶胞中由K和F共同形成的正四面体空隙有
②晶胞的另一种表示中,Co处于各顶角位置,则K处于
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,表中所列字母分别代表一种元素。试回答下列问题:
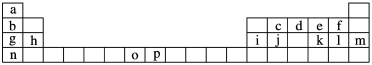
(1)①依据元素周期表的分区,元素c属于___________ 区。
②基态e离子的核外电子排布式是___________ 。
③基态g原子核外能量不同的电子有___________ 种。
④元素1的基态原子的核外电子共占据___________ 个原子轨道。
(2)将c、d、e、f四种元素按电负性由小到大的顺序排列___________ (用元素符号表示)。
(3)元素a和c可以构成多种化合物,苯就是其中的一种。以下有关苯分子中化学键的描述正确的是___________
(4)下列有关分子的空间结构,描述正确的是___________
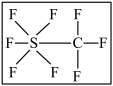
(5)据报道,大气中存在一种潜在的温室气体 (结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于
(结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于 的说法正确的是___________
的说法正确的是___________
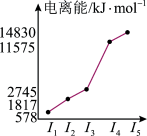
(6)表中所列的某主族元素的电离能情况如图所示,则该元素是___________ (填元素符号)。
(7)判断下列关于相关元素及元素组成的化合物的说法是否正确。(A—正确;B—错误)。
①玻璃纤维是合成纤维的一种,属于高分子材料。___________
②二氧化硫具有氧化性,可用于漂白纸浆。___________
③CaO能与 反应,可作工业废气的脱硫剂。
反应,可作工业废气的脱硫剂。___________
④制 时,用水或NaOH溶液吸收尾气。
时,用水或NaOH溶液吸收尾气。___________
(8)o、p两元素的部分电离能数据列于下表:
比较两元素的 、
、 可知,气态
可知,气态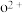 再失去一个电子比气态
再失去一个电子比气态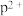 再失去一个电子难,其原因是
再失去一个电子难,其原因是___________

(1)①依据元素周期表的分区,元素c属于
②基态e离子的核外电子排布式是
③基态g原子核外能量不同的电子有
④元素1的基态原子的核外电子共占据
(2)将c、d、e、f四种元素按电负性由小到大的顺序排列
(3)元素a和c可以构成多种化合物,苯就是其中的一种。以下有关苯分子中化学键的描述正确的是___________
A.每个碳原子的一个 杂化轨道参与形成大π键 杂化轨道参与形成大π键 |
| B.每个碳原子的未参加杂化的2p轨道形成大π键 |
C.碳原子的3个 杂化轨道与其他碳原子形成2个σ键和1个π键 杂化轨道与其他碳原子形成2个σ键和1个π键 |
| D.碳原子的未参加杂化的2p轨道与其他碳原子的2p轨道成键 |
(4)下列有关分子的空间结构,描述正确的是___________
A. 分子中N原子处在3个H原子所组成的三角形的中心 分子中N原子处在3个H原子所组成的三角形的中心 |
B. 分子中C原子处在4个Cl原子所组成的四面体的中心 分子中C原子处在4个Cl原子所组成的四面体的中心 |
C. 分子中O原子处在2个H原子所连成的直线的中央 分子中O原子处在2个H原子所连成的直线的中央 |
D. 分子中P原子处在3个Cl原子所组成的三角形的中心 分子中P原子处在3个Cl原子所组成的三角形的中心 |
(5)据报道,大气中存在一种潜在的温室气体
 (结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于
(结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于 的说法正确的是___________
的说法正确的是___________
| A.分子中有σ键也有π键 |
B. 是s-pσ键 是s-pσ键 |
| C.分子中不是所有原子都满足8电子稳定结构 |
D.0.1mol 分子中电子数为8mol 分子中电子数为8mol |
(6)表中所列的某主族元素的电离能情况如图所示,则该元素是

(7)判断下列关于相关元素及元素组成的化合物的说法是否正确。(A—正确;B—错误)。
①玻璃纤维是合成纤维的一种,属于高分子材料。
②二氧化硫具有氧化性,可用于漂白纸浆。
③CaO能与
 反应,可作工业废气的脱硫剂。
反应,可作工业废气的脱硫剂。④制
 时,用水或NaOH溶液吸收尾气。
时,用水或NaOH溶液吸收尾气。(8)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p |
 | 717 | 759 |
 | 1509 | 1561 |
 | 3248 | 2957 |
 、
、 可知,气态
可知,气态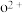 再失去一个电子比气态
再失去一个电子比气态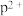 再失去一个电子难,其原因是
再失去一个电子难,其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据要求完成下列问题:
(1)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,试回答:该元素核外价电子排布图___ ,电子排布式_____ 。
(2)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:____ 、____ 、____ 。
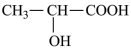
(3)下列分子中若有手性原子,请用“*”标出其手性碳原子。____
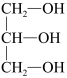
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)____ 。
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4____ H2SO3;HClO3____ HClO4;H3PO4___ H3PO3。
(6)根据价层电子对互斥理论判断下列问题:
NH3中心原子的杂化方式为___ 杂化,VSEPR构型为__ ,分子的立体构型为____ 。
(7)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于____ 。
(1)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,试回答:该元素核外价电子排布图
(2)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:
(3)下列分子中若有手性原子,请用“*”标出其手性碳原子。

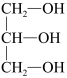
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4
(6)根据价层电子对互斥理论判断下列问题:
NH3中心原子的杂化方式为
(7)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】写出(1)~(4)原子的电子排布式,用价层电子对互斥模型推测(5)~(8)分子的空间构型。
(1)Li_______________ ;(2)K _______________ ;(3)Mg ________________ ;(4)Cl ______________ ;(5)CO2_______________ ;(6)SO2______________ ;(7)NH3_________________ ;(8)CH4_______________ 。
(1)Li
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】根据要求完成下列问题。
(1)下列数据,前者小于后者的是_______ (填序号)。
①键长:N—N和 ②键能:
②键能: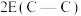 和
和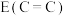
③键角: 和
和 ④键的极性:C—H和N—H
④键的极性:C—H和N—H
⑤沸点:邻羟基苯甲酸和对羟基苯甲酸 ⑥沸点: 和CO
和CO
(2)完成下表中的空白:
(1)下列数据,前者小于后者的是
①键长:N—N和
 ②键能:
②键能: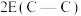 和
和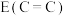
③键角:
 和
和 ④键的极性:C—H和N—H
④键的极性:C—H和N—H⑤沸点:邻羟基苯甲酸和对羟基苯甲酸 ⑥沸点:
 和CO
和CO(2)完成下表中的空白:
| 粒子 | VSEPR模型名称 | 分子(或离子)的空间结构 | 中心原子杂化轨道类型 |
| HCN | |||
 | |||
 |
您最近一年使用:0次



