Ⅰ、已知电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性:
(1)估计O元素的电负性数值范围________ <X<________
(2)下列物质属于离子化合物的是________ ,属于共价化合物的有________ 。
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
Ⅱ、下表列出了①~⑨九种元素在周期表中的位置:
(3)基态②原子的核外电子有___________ 种空间运动状态。
(4)元素⑦的基态原子价层电子轨道表示式为___________________________ 。
(5)按气态氢化物的稳定性由弱到强的顺序排列,④⑥⑦的简单氢化物稳定性:________ (写氢化物的化学式)。
(6)写出元素⑤形成的单质在氧气中燃烧的化学方程式:___________________ 。
(7)③的简单氢化物与其最高价氧化物的水化物反应的离子方程式:___________________________________ 。
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | X | 2.1 | 2.5 | 1.8 |
(2)下列物质属于离子化合物的是
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
Ⅱ、下表列出了①~⑨九种元素在周期表中的位置:
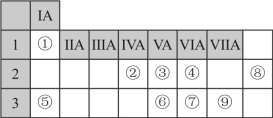
(3)基态②原子的核外电子有
(4)元素⑦的基态原子价层电子轨道表示式为
(5)按气态氢化物的稳定性由弱到强的顺序排列,④⑥⑦的简单氢化物稳定性:
(6)写出元素⑤形成的单质在氧气中燃烧的化学方程式:
(7)③的简单氢化物与其最高价氧化物的水化物反应的离子方程式:
更新时间:2024-04-10 17:43:07
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下面是元素周期表的简略框架图。
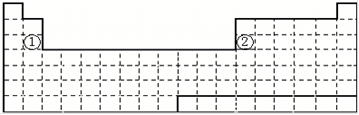
(1)请在元素周期表中画出金属元素与非金属元素的分界线______ 。按电子排布,可把元素划分成5个区,不全是金属元素的区为_______ 。
(2)表中元素①、②原子的最外层电子的电子排布式分别为_______ 、_______ ;比较元素①与元素②的下列性质(填写“>”或“<”)。
原子半径:①_______ ②、电负性:①_______ ②、金属性:①_______ ②。
(3)某短周期元素最高正价为+7,其原子结构示意图为_______ 。
(4)根据氢元素最高正价与最低负价的绝对值相等,你认为可把氢元素放在周期表中的_______ 族;有人建议将氢元素排在元素周期表的ⅦA族,请你写出支持这一观点的1个化学事实_______ 。

(1)请在元素周期表中画出金属元素与非金属元素的分界线
(2)表中元素①、②原子的最外层电子的电子排布式分别为
原子半径:①
(3)某短周期元素最高正价为+7,其原子结构示意图为
(4)根据氢元素最高正价与最低负价的绝对值相等,你认为可把氢元素放在周期表中的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】表为元素周期表的一部分,a、b、c……为其中几种元素。回答下列问题:
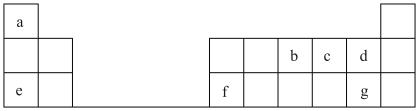
(1)写出b在元素周期表中的位置_______ 。
(2)元素d和g的气态氢化物中,更稳定的是_______ (写化学式)。
(3)元素d、e、g中原子半径由大到小的顺序为_______ (用元素符号表示)。
(4)元素e、g形成的化合物的电子式为_______ ,所含化学键类型为_______ 。
(5)a、c、e三种元素形成化合物的水溶液与g的最高价氧化物对应水化物反应的离子方程式:_______ 。

(1)写出b在元素周期表中的位置
(2)元素d和g的气态氢化物中,更稳定的是
(3)元素d、e、g中原子半径由大到小的顺序为
(4)元素e、g形成的化合物的电子式为
(5)a、c、e三种元素形成化合物的水溶液与g的最高价氧化物对应水化物反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,元素①-⑦是短周期的主族元素,请参照元素①-⑥在表中的位置,回答下列问题:
(1)写出⑥在元素周期表中的位置_____ 。
(2)②的气态氢化物的沸点____ ⑥的气态氢化物的沸点。(填大于、小于或等于)
(3)④的最高价氧化物与③的最高价氧化物对应的水化物的水溶液反应的离子方程式为
_____ 。
(4)①和⑤形成的化合物是化工行业已合成的一种硬度很大、熔点很高的晶体,若已知在此化合物中各元素均处于其最高或最低价态,据此推断:该化合物的化学式可能是_____ , 与该化合物晶体类型相同的是______ (请用相应的编号填写)。
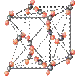

A B C
(5)由①和③形成的化合物甲和乙,甲受到撞击会分解生成一种固体单质和一种气体单质,此反应中反应物、固体单质和气体单质的物质的量之比是2:2:3;乙中加入过量的盐酸后生成两种盐,在其中一种盐中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体。则化合物甲的化学式为_____ ,化合物乙与过量盐酸反应的化学方程式为_____ 。
| ① | ② | |||||
| ③ | ④ | ⑤ | ⑥ | ⑦ |
(1)写出⑥在元素周期表中的位置
(2)②的气态氢化物的沸点
(3)④的最高价氧化物与③的最高价氧化物对应的水化物的水溶液反应的离子方程式为
(4)①和⑤形成的化合物是化工行业已合成的一种硬度很大、熔点很高的晶体,若已知在此化合物中各元素均处于其最高或最低价态,据此推断:该化合物的化学式可能是



A B C
(5)由①和③形成的化合物甲和乙,甲受到撞击会分解生成一种固体单质和一种气体单质,此反应中反应物、固体单质和气体单质的物质的量之比是2:2:3;乙中加入过量的盐酸后生成两种盐,在其中一种盐中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体。则化合物甲的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硬铝(含少量铜、镁、锰和硅)有良好的机械性能,是制造飞机的理想材料。
(1)写出硅原子最外层电子排布式__________ ;短周期元素A与硅元素同主族,能与氧元素组成化合物AO2,写出AO2的电子式:__________ 。
(2)上述硬铝中所含的主族元素的原子半径由大到小的顺序为:__________ 。
(3)请阐述硬铝是制造飞机的理想材料的原因有:__________ 、__________ 。
(4)工业上可用镁真空炼铷,方程式为2RbCl+Mg MgCl2+2Rb(g),对于此反应能够进行正确的解释是
MgCl2+2Rb(g),对于此反应能够进行正确的解释是 __________ 。
a.Rb比Mg金属性强
b.MgCl2的热稳定性比RbCl 弱
c.高温下Mg2+得电子能力比Rb+弱
d.Rb的沸点比Mg低,当把Rb(g)抽走时,平衡向正反应方向移动
(1)写出硅原子最外层电子排布式
(2)上述硬铝中所含的主族元素的原子半径由大到小的顺序为:
(3)请阐述硬铝是制造飞机的理想材料的原因有:
(4)工业上可用镁真空炼铷,方程式为2RbCl+Mg
 MgCl2+2Rb(g),对于此反应能够进行正确的解释是
MgCl2+2Rb(g),对于此反应能够进行正确的解释是 a.Rb比Mg金属性强
b.MgCl2的热稳定性比RbCl 弱
c.高温下Mg2+得电子能力比Rb+弱
d.Rb的沸点比Mg低,当把Rb(g)抽走时,平衡向正反应方向移动
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮是地球上极为丰富的元素。回答下列问题:
(1)氮化锂( )晶体中氮以
)晶体中氮以 存在,基态
存在,基态 核外电子排布式为
核外电子排布式为______ ,基态 核外电子占据的最高能级电子的电子云轮廓图形状为
核外电子占据的最高能级电子的电子云轮廓图形状为______ 。
(2)胸腺嘧啶是构成DNA的一种含氮碱基,结构简式如图所示。______ 。
②其分子中σ键和π键的数目之比为______ 。
③该胸腺嘧啶中含有官能团的名称______ 。
(3)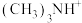 和
和 可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂
可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂______ (填“大”或“小”), 的空间结构为
的空间结构为______ 。
(4) 与
与 形成化合物的晶胞如图所示,与同一个
形成化合物的晶胞如图所示,与同一个 最近且等距的
最近且等距的 有
有______ 个。
(1)氮化锂(
 )晶体中氮以
)晶体中氮以 存在,基态
存在,基态 核外电子排布式为
核外电子排布式为 核外电子占据的最高能级电子的电子云轮廓图形状为
核外电子占据的最高能级电子的电子云轮廓图形状为(2)胸腺嘧啶是构成DNA的一种含氮碱基,结构简式如图所示。
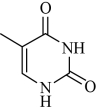
②其分子中σ键和π键的数目之比为
③该胸腺嘧啶中含有官能团的名称
(3)
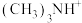 和
和 可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂
可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂 的空间结构为
的空间结构为(4)
 与
与 形成化合物的晶胞如图所示,与同一个
形成化合物的晶胞如图所示,与同一个 最近且等距的
最近且等距的 有
有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表中实线是元素周期表的部分边界,其中上边界并未用实线画出。
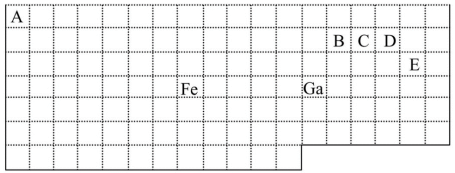
根据信息回答下列问题:
(1)基态Ga原子的最外层电子排布式为_________________ 。
(2)铁元素位于元素周期表的________ 区;Fe和CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为__________ 。
(3)已知:原子数目和价电子总数均相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO互为等电子体的分子和离子分别为_______ 和______ (填化学式)。
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有__________ 。
(5)根据VSEPR模型预测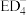 的空间构型为
的空间构型为__________ 。

根据信息回答下列问题:
(1)基态Ga原子的最外层电子排布式为
(2)铁元素位于元素周期表的
(3)已知:原子数目和价电子总数均相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO互为等电子体的分子和离子分别为
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有
(5)根据VSEPR模型预测
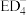 的空间构型为
的空间构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】应用
①判断元素的金属性和非金属性强弱
i.金属的电负性一般_______ 1.8,非金属的电负性一般_______ 1.8,而位于非金属三角区边界的“类金属”(如锗、锑等)的电负性则在_______ 左右,它们既有金属性,又有非金属性。
ii.金属元素的电负性_______ ,金属元素越活泼;非金属元素的电负性_______ ,非金属元素越活泼。
②判断元素的化合价
i.电负性数值小的元素在化合物中吸引电子的能力_______ ,元素的化合价为_______ 。
ii.电负性数值大的元素在化合物中吸引电子的能力_______ ,元素的化合价为_______ 。
③判断化合物的类型

如H的电负性为2.1,Cl的电负性为3.0,Cl的电负性与H的电负性之差为3.0-2.1=0.9<1.7,故HCl为共价化合物;如Al的电负性为1.5,Cl的电负性与Al的电负性之差为3.0-1.5=1.5<1.7,因此AlCl3为共价化合物;同理,BeCl2也是共价化合物。
注意:电负性之差大于1.7的元素不一定都形成离子化合物,如F的电负性与H的电负性之差为1.9,但HF为共价化合物。
①判断元素的金属性和非金属性强弱
i.金属的电负性一般
ii.金属元素的电负性
②判断元素的化合价
i.电负性数值小的元素在化合物中吸引电子的能力
ii.电负性数值大的元素在化合物中吸引电子的能力
③判断化合物的类型

如H的电负性为2.1,Cl的电负性为3.0,Cl的电负性与H的电负性之差为3.0-2.1=0.9<1.7,故HCl为共价化合物;如Al的电负性为1.5,Cl的电负性与Al的电负性之差为3.0-1.5=1.5<1.7,因此AlCl3为共价化合物;同理,BeCl2也是共价化合物。
注意:电负性之差大于1.7的元素不一定都形成离子化合物,如F的电负性与H的电负性之差为1.9,但HF为共价化合物。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
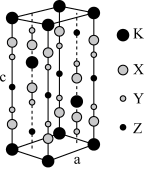
【推荐2】光刻技术需要利用深紫激光,我国是唯一掌握通过非线性光学晶体变频来获得深紫外激光技术的国家。目前唯一实用化的晶体是氟代硼铍酸钾晶体 KBBF(KBe2BO3F2),实验室可用 BeO、KBF4和 B2O3 在 700℃左右灼烧获得氟代硼铍酸钾晶体(晶胞如下图所示,其中 K 原子已经给出,氧原子略去),并放出 BF3气体。回答下列问题:
(1)基态钾原子的核外电子排布式为___________ ,能量最高的电子的电子云轮廓图形状为___________ 。
(2)BF3的空间构型为___________ ,与其互为等电子体的阴离子为___________ (填一种即可)。
(3)氟代硼铍酸钾晶体 KBBF(KBe2BO3F2)组成元素中电负性最大的元素和电负性最小的元素组成的物质为___________ 。
(4)KBF4中心 B 原子的杂化方式为___________ 杂化。
(5) 三卤化硼的性质如下:
BF3、BCl3、BBr3、BI3的沸点逐渐升高的原因是:___________ 。
(6)指出图中代表硼原子的字母为___________ ,该KBBF晶体的晶胞参数分别为a pm 和 c pm,α=β=γ=90°,则晶体密度为___________ g·cm-3(M 代表 KBBF 的摩尔质量,NA表示阿伏加德罗常数的值,列出计算式)。

(1)基态钾原子的核外电子排布式为
(2)BF3的空间构型为
(3)氟代硼铍酸钾晶体 KBBF(KBe2BO3F2)组成元素中电负性最大的元素和电负性最小的元素组成的物质为
(4)KBF4中心 B 原子的杂化方式为
(5) 三卤化硼的性质如下:
| BF3 | BCl3 | BBr3 | BI3 | |
| 熔点/℃ | -127. | | -107 | -46 | 49.9 |
| 沸点/℃ | -99 | 12.5 | 91.3 | 210. |
BF3、BCl3、BBr3、BI3的沸点逐渐升高的原因是:
(6)指出图中代表硼原子的字母为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)氯原子核外有________ 种不同运动状态的电子;基态溴原子的价电子排布式为_______ ;比较氟、氯、溴单质熔点的高低并说明理由___________ 。
(2)HF极易溶于水的原因是______ 。
(3)已知高碘酸有两种形式,化学式分别为H5IO6(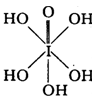 )和HIO4,前者为 五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6
)和HIO4,前者为 五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6______ HIO4。(填“>”、“<”或“=”)
(4)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为_____ ,中心原子的杂化类型为_____ 。
(5)[LiC60]PF6与NaCl具有类似的晶胞结构([LiC60]+表示1个Li+位于1个C60内部)。[LiC60]PF6晶体中包含的化学键有_____________ (多选,填字母);
A.金属键 B.离子键 C.极性键 D.非极性键 E.范德华力
已知[LiC60]PF6晶体晶胞边长为a nm,计算[LiC60]PF6晶体的密度为_______ g·cm-3(用含a、NA的式子表示)。
(2)HF极易溶于水的原因是
(3)已知高碘酸有两种形式,化学式分别为H5IO6(
 )和HIO4,前者为 五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6
)和HIO4,前者为 五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6(4)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为
(5)[LiC60]PF6与NaCl具有类似的晶胞结构([LiC60]+表示1个Li+位于1个C60内部)。[LiC60]PF6晶体中包含的化学键有
A.金属键 B.离子键 C.极性键 D.非极性键 E.范德华力
已知[LiC60]PF6晶体晶胞边长为a nm,计算[LiC60]PF6晶体的密度为
您最近一年使用:0次



