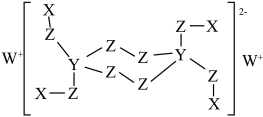
我国科学家最近成功合成了世界首个五氮阴离子盐 ,其化学式为
,其化学式为 ,从结构角度分析,
,从结构角度分析, 中两种阳离子的不同之处为
中两种阳离子的不同之处为
 ,其化学式为
,其化学式为 ,从结构角度分析,
,从结构角度分析, 中两种阳离子的不同之处为
中两种阳离子的不同之处为| A.中心原子的杂化轨道类型 | B.中心原子的价层电子对数 |
| C.空间结构 | D.共价键类型 |
更新时间:2024-04-21 08:26:44
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加德罗常数的值,下列说法正确的是
A.18 g 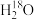 中含有的中子数为10NA 中含有的中子数为10NA |
| B.42 g环己烷中含有σ键的数目为9NA |
| C.标准状况下,2.24 L SO3中含有的分子数为0.1NA |
D.22 g CO2与足量NaOH溶液反应,所得溶液 的个数为0.5NA 的个数为0.5NA |
您最近一年使用:0次
【推荐2】某种含二价铜微料 催化剂可用于汽车尾气脱硝,催化机理如图1,反应历程中不同状态物质体系所含的能量如图2。
催化剂可用于汽车尾气脱硝,催化机理如图1,反应历程中不同状态物质体系所含的能量如图2。


下列说法正确的是
 催化剂可用于汽车尾气脱硝,催化机理如图1,反应历程中不同状态物质体系所含的能量如图2。
催化剂可用于汽车尾气脱硝,催化机理如图1,反应历程中不同状态物质体系所含的能量如图2。

下列说法正确的是
A. 可加快脱硝速率,提高平衡转化率 可加快脱硝速率,提高平衡转化率 |
| B.状态②到状态③的变化过程中有极性键的断裂与形成 |
| C.状态④到状态⑤的变化过程决定了整个历程的反应速率 |
| D.在图1所示历程中铜元素的化合价未发生变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列分子或离子中,构型不为 直线型的是
A.I | B.I | C.CS2 | D.BeCl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】氢、氧、碳、氮是构成地球和整个宇宙的重要元素,是元素中的“四大天王”,下列和它们有关的化合物的说法不正确的是
A.HCN、NH3、NO 空间构型各不相同,中心原子的杂化方式有三种 空间构型各不相同,中心原子的杂化方式有三种 |
| B.CO2和C2H4中,碳原子杂化方式相同,结构中碳原子都呈双键 |
| C.H2O、CH4、H3O+VSEPR模型相同,空间构型不同 |
| D.金刚石、C60互为同素异形体,碳原子具有不同的杂化方式 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.键能:H-O>H-S,因此H2O的沸点高于H2S的沸点 |
| B.原子轨道具有一定的伸展方向,所形成的共价键都具有方向性 |
| C.杂化轨道可用于形成σ键和容纳未参与成键的孤电子对,不能用于形成π键 |
| D.电负性越大,非金属性越强,第一电离能也越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是( )
| A.sp2杂化表示s轨道的1个电子和p轨道的2个电子进行杂化 |
| B.1s22s12p1是激发态原子的电子排布式 |
| C.M能层中的原子轨道数目为3 |
| D.一个电子从3p能级跃迁到3s能级,产生的原子光谱为吸收光谱 |
您最近一年使用:0次

 2NH3的微观历程如图所示。下列说法正确的是(
2NH3的微观历程如图所示。下列说法正确的是(