含氮化合物在工农业生产中有着十分重要的作用。铵盐、硝酸盐、尿素等可作植物生长的“食物”。但含氮化合物在生产和使用过程中产生的氮氧化物易造成光化学污染和硝酸型酸雨。所以氮氧化物需无害化处理,目前根据氮氧化物的来源处理的主流方法如下:
(1)方法一:工业废气(含 、
、 )利用石灰乳吸收,既能净化尾气,又能获得应用广泛的
)利用石灰乳吸收,既能净化尾气,又能获得应用广泛的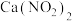 。
。
①写出该反应的方程式:___________ 。
②工业处理废气时,采用吸收塔,将废气从吸收塔底部通入,石灰乳从吸收塔顶部喷淋。这样操作的优点是:___________ 。
(2)方法二:“三元催化”是安装在汽车排气系统中最重要的机外净化装置。其工作原理是利用加装催化剂铑( )将尾气中三种主要的有害物质转化为无害物质,该反应的过程示意图如下:
)将尾气中三种主要的有害物质转化为无害物质,该反应的过程示意图如下:___________ 过程(填“吸热”或“放热”),还原产物为___________ ,当生成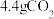 时,转移电子
时,转移电子___________  。
。
②请用文字描述过程I和过程II___________ 。
(1)方法一:工业废气(含
 、
、 )利用石灰乳吸收,既能净化尾气,又能获得应用广泛的
)利用石灰乳吸收,既能净化尾气,又能获得应用广泛的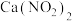 。
。①写出该反应的方程式:
②工业处理废气时,采用吸收塔,将废气从吸收塔底部通入,石灰乳从吸收塔顶部喷淋。这样操作的优点是:
(2)方法二:“三元催化”是安装在汽车排气系统中最重要的机外净化装置。其工作原理是利用加装催化剂铑(
 )将尾气中三种主要的有害物质转化为无害物质,该反应的过程示意图如下:
)将尾气中三种主要的有害物质转化为无害物质,该反应的过程示意图如下: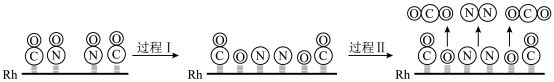
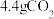 时,转移电子
时,转移电子 。
。②请用文字描述过程I和过程II
更新时间:2024-04-25 22:44:23
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】农业生产离不开空气、水、土壤和肥料,保护土壤资源,防止土壤污染,改良土壤酸碱性是保证社会可持续发展的重要工作。
(1)土壤酸化的原因很多,主要有:矿物风化过程中产生的无机酸或大量二氧化碳;土壤中强酸弱碱盐的水解;无机肥料残留酸根;酸雨的影响;土壤胶体吸附的H+被其他阳离子交换;微生物、细菌在利用土壤有机物时,会产生二氧化碳和多种有机酸,或者将土壤中的NH3转化为亚硝酸和硝酸,将硫化物转化为硫酸。
①土壤中主要含有的强酸弱碱盐:铝盐、铁盐等,写出其中一个水解方程式:_______ 。
②在通气良好的土壤中,氧体系控制氧化还原反应,使多种物质呈氧化态,土壤中 的氧化是在亚硝酸细菌和硝酸细菌作用下完成,写出反应离子方程式。
的氧化是在亚硝酸细菌和硝酸细菌作用下完成,写出反应离子方程式。_______ ;_______ 。
(2)土壤呈碱性的原因与酸化原因大致相反,包括强碱弱酸盐的水解,尿素的过度使用,土壤所吸附的OH-、Na+等被其他离子交换或土壤中有机物中的氮被微生物分解生成氨的氨化过程。
①过度使用尿素[CO(NH2)2]会使土壤碱化的原因是(用化学方程式表示):_______ 。
②改良土壤碱性的其中一种方法是使用石膏,其原理是(用化学反应方程式表示):_______ 。
(1)土壤酸化的原因很多,主要有:矿物风化过程中产生的无机酸或大量二氧化碳;土壤中强酸弱碱盐的水解;无机肥料残留酸根;酸雨的影响;土壤胶体吸附的H+被其他阳离子交换;微生物、细菌在利用土壤有机物时,会产生二氧化碳和多种有机酸,或者将土壤中的NH3转化为亚硝酸和硝酸,将硫化物转化为硫酸。
①土壤中主要含有的强酸弱碱盐:铝盐、铁盐等,写出其中一个水解方程式:
②在通气良好的土壤中,氧体系控制氧化还原反应,使多种物质呈氧化态,土壤中
 的氧化是在亚硝酸细菌和硝酸细菌作用下完成,写出反应离子方程式。
的氧化是在亚硝酸细菌和硝酸细菌作用下完成,写出反应离子方程式。(2)土壤呈碱性的原因与酸化原因大致相反,包括强碱弱酸盐的水解,尿素的过度使用,土壤所吸附的OH-、Na+等被其他离子交换或土壤中有机物中的氮被微生物分解生成氨的氨化过程。
①过度使用尿素[CO(NH2)2]会使土壤碱化的原因是(用化学方程式表示):
②改良土壤碱性的其中一种方法是使用石膏,其原理是(用化学反应方程式表示):
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素及其化合物的应用广泛,回答下列问题:
(1)碘盐中含有KIO3,KIO3中碘元素的化合价是____________ 。
(2)84消毒液的有效成分是____________ (填“NaCl”或“NaClO”)。
(3)高温下Fe2O3与CO反应是工业上炼铁的原理,该原理的化学反应方程式为____________ ,反应中Fe2O3做________ (填“氧化剂”或“还原剂”)。
(4)实验室用NaOH溶液吸收含SO2的尾气,该反应的离子方程式为____________ ,SO2属于____________ (填“酸性氧化物”或“碱性氧化物”),SO2能使品红溶液褪色,说明SO2具有的性质是____________ 。
(1)碘盐中含有KIO3,KIO3中碘元素的化合价是
(2)84消毒液的有效成分是
(3)高温下Fe2O3与CO反应是工业上炼铁的原理,该原理的化学反应方程式为
(4)实验室用NaOH溶液吸收含SO2的尾气,该反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼(
)、钼( )、镍(
)、镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
)等元素的氧化物,一种回收利用工艺的部分流程如下:

已知:25℃时, 的
的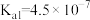 ,
, ;
;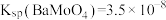 ;
;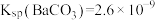 ;该工艺中,
;该工艺中,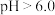 时,溶液中
时,溶液中 元素以
元素以 的形态存在。
的形态存在。
(1)“焙烧”中,有 生成,其中
生成,其中 元素的化合价为
元素的化合价为_______ 。
(2)“沉铝”中,生成的沉淀X为_______ 。
(3)“沉钼”中, 为7.0.则生成
为7.0.则生成 的离子方程式为
的离子方程式为_______ 。
(4)①滤液III中,主要存在的钠盐有 和Y,Y为
和Y,Y为_______ 。
②往滤液III中添加适量 固体后,通入足量
固体后,通入足量____ (填化学式)气体,再通入足量 ,可析出Y。
,可析出Y。
(5)高纯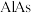 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止
(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止 刻蚀液与下层
刻蚀液与下层 (砷化镓)反应。
(砷化镓)反应。
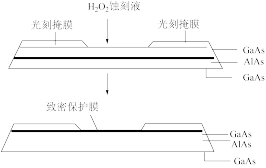
①该氧化物为_______ 。
②已知: 和
和 同族,
同族, 和N同族。在
和N同族。在 与上层
与上层 的反应中,
的反应中, 元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为
元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为_______ 。
 )、钼(
)、钼( )、镍(
)、镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时,
 的
的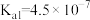 ,
, ;
;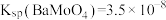 ;
;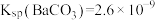 ;该工艺中,
;该工艺中,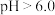 时,溶液中
时,溶液中 元素以
元素以 的形态存在。
的形态存在。(1)“焙烧”中,有
 生成,其中
生成,其中 元素的化合价为
元素的化合价为(2)“沉铝”中,生成的沉淀X为
(3)“沉钼”中,
 为7.0.则生成
为7.0.则生成 的离子方程式为
的离子方程式为(4)①滤液III中,主要存在的钠盐有
 和Y,Y为
和Y,Y为②往滤液III中添加适量
 固体后,通入足量
固体后,通入足量 ,可析出Y。
,可析出Y。(5)高纯
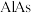 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止
(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止 刻蚀液与下层
刻蚀液与下层 (砷化镓)反应。
(砷化镓)反应。
①该氧化物为
②已知:
 和
和 同族,
同族, 和N同族。在
和N同族。在 与上层
与上层 的反应中,
的反应中, 元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为
元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有反应:
A.2H2O2 H2O+O2↑
H2O+O2↑
B.Fe+H2SO4=FeSO4+H2↑
C.Na2CO3·10H2O与NH4NO3反应制作冷敷袋
D.2KOH+H2SO4=K2SO4+2H2O
(1)上述四个反应过程中能量变化符合如图甲的是_______ (填序号)。
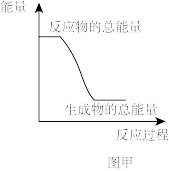
(2)上述四个反应中可用于设计成如图乙的原电池的反应是_______ (填反应序号)。根据该原电池回答下列问题:
①负极反应式为_______ ;正极发生_______ (填“氧化”或“还原”)反应。
②当导线中有2mol电子通过时,理论上发生的变化是_______ (填序号)。
a.溶液增重56g b.溶液增重54g c.析出1g H2 d.析出11.2L H2(标准状况)

(3)FeCl3常用于腐蚀印刷电路铜板(2FeCl3+Cu=2FeCl2+CuCl2),请将此反应设计成原电池,请根据图乙画出该原电池的装置图,注明电极材料,电解质溶液,电子流向。_______
A.2H2O2
 H2O+O2↑
H2O+O2↑ B.Fe+H2SO4=FeSO4+H2↑
C.Na2CO3·10H2O与NH4NO3反应制作冷敷袋
D.2KOH+H2SO4=K2SO4+2H2O
(1)上述四个反应过程中能量变化符合如图甲的是

(2)上述四个反应中可用于设计成如图乙的原电池的反应是
①负极反应式为
②当导线中有2mol电子通过时,理论上发生的变化是
a.溶液增重56g b.溶液增重54g c.析出1g H2 d.析出11.2L H2(标准状况)

(3)FeCl3常用于腐蚀印刷电路铜板(2FeCl3+Cu=2FeCl2+CuCl2),请将此反应设计成原电池,请根据图乙画出该原电池的装置图,注明电极材料,电解质溶液,电子流向。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学反应可视为旧键断裂和新键形成的过程。已知拆开1molH—H键、1molCl—Cl键、1molH—Cl键分别需要吸收的能量为436.4kJ、242.7kJ、431.8kJ。
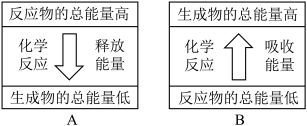
H2可以在Cl2中安静地燃烧。上图能表示该反应能量变化的是图___________ (填“A”或“B”)。由H2和Cl2反应生成1molHCl需要___________ (填“放出”或“吸收”)___________ kJ的热量。

H2可以在Cl2中安静地燃烧。上图能表示该反应能量变化的是图
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮、硫等非金属元素及其化合物在生产生活中应用广泛。请回答下列问题:
(1)键能是指在将1mol理想气体分子AB拆开为中性气态原子A和B所需的能量。
已知下列化学键的键能如下表:
写出1mol气态肼(H2N一NH2)在氧气中燃烧生成氮气和气态水的热化学方程式___________ 。
(2)已知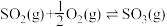 反应过程的能量变化如图所示:
反应过程的能量变化如图所示:
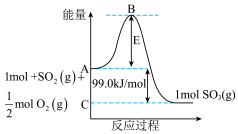
①图中E表示:___________ 。
②又知 ,请根据上图求出反应
,请根据上图求出反应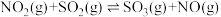 的△H=
的△H=___________ kJ·mol-1。
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用标注。
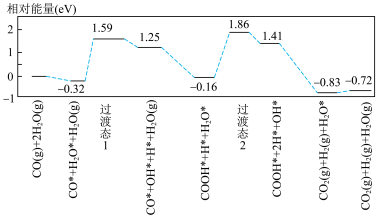
可知水煤气变换的△H___________ 0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)E正=___________ eV,写出该步骤的化学方程式___________ 。
(1)键能是指在将1mol理想气体分子AB拆开为中性气态原子A和B所需的能量。
已知下列化学键的键能如下表:
| 化学键 |  | O=O | N-N | N-H | O-H |
| 键能/kJ·mol-1 | 946 | 497 | 193 | 391 | 463 |
(2)已知
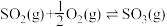 反应过程的能量变化如图所示:
反应过程的能量变化如图所示:
①图中E表示:
②又知
 ,请根据上图求出反应
,请根据上图求出反应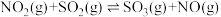 的△H=
的△H=(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用标注。

可知水煤气变换的△H
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】被誉为“太空金属”的钛(Ti),在自然界中主要以金红石(TiO2)的形式存在。由于金红石熔点高,为金属Ti的直接制备带来了困难。在工业上常常采用将其先转化成熔沸点较低的TiCl4后再进行还原的方法。金红石转化成TiCl4的反应方程式如下:TiO2 + 2C + 2Cl2═ TiCl4 + 2CO
(1)用双线桥法标出上述化学方程式的电子转移情况_______________ ;
(2)指出该反应的氧化剂__________ ,氧化产物__________ ;
(3)当消耗标准状况下Cl2 11.2L时,则转移的电子数为__________ 。
(1)用双线桥法标出上述化学方程式的电子转移情况
(2)指出该反应的氧化剂
(3)当消耗标准状况下Cl2 11.2L时,则转移的电子数为
您最近半年使用:0次
【推荐2】回答下列问题:
I.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是___________ (填序号)。
(2)某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与 反应产生
反应产生 促进藻类快速生长。
促进藻类快速生长。
该反应说明氧化性:NaClO___________  (填“>”或“<”),当参加反应的NaClO和
(填“>”或“<”),当参加反应的NaClO和 的物质的量之比为1∶1时,该反应的还原产物为
的物质的量之比为1∶1时,该反应的还原产物为___________ 。
Ⅱ.高铁酸钠( )(其中氧元素是-2价)是一种新型的净水剂,可以通过下述反应制取:
)(其中氧元素是-2价)是一种新型的净水剂,可以通过下述反应制取:
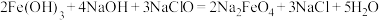
(3)①用双线桥法在化学方程式中标出电子转移的情况。___________
②请完成方程式的配平:___________
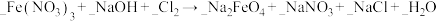
Ⅲ.汽车剧烈碰撞时,安全气囊中发生反应 。
。
(4)若氧化产物比还原产物多1.75 mol,则转移的电子数为___________ ( 为阿伏加德罗常数的值),被氧化的N原子的物质的量为
为阿伏加德罗常数的值),被氧化的N原子的物质的量为___________ 。
I.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究
 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是| 序号 | 实验 | 实验现象 |
| 1 | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去;b.有大量气泡产生 |
| 2 | 向5% 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 反应产生
反应产生 促进藻类快速生长。
促进藻类快速生长。该反应说明氧化性:NaClO
 (填“>”或“<”),当参加反应的NaClO和
(填“>”或“<”),当参加反应的NaClO和 的物质的量之比为1∶1时,该反应的还原产物为
的物质的量之比为1∶1时,该反应的还原产物为Ⅱ.高铁酸钠(
 )(其中氧元素是-2价)是一种新型的净水剂,可以通过下述反应制取:
)(其中氧元素是-2价)是一种新型的净水剂,可以通过下述反应制取: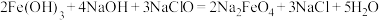
(3)①用双线桥法在化学方程式中标出电子转移的情况。
②请完成方程式的配平:
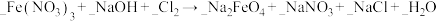
Ⅲ.汽车剧烈碰撞时,安全气囊中发生反应
 。
。(4)若氧化产物比还原产物多1.75 mol,则转移的电子数为
 为阿伏加德罗常数的值),被氧化的N原子的物质的量为
为阿伏加德罗常数的值),被氧化的N原子的物质的量为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氧化还原反应在生产生活中有广泛的应用,中国传统文化中有广泛记载。
(1)“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及到蜡烛与 的燃烧反应,反应生成
的燃烧反应,反应生成 和
和 ,该反应一定是___________。
,该反应一定是___________。
(2)“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为: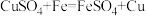 。该反应中被氧化的元素是
。该反应中被氧化的元素是___________ (填元素符号,下同),化合价降低的元素是___________ 。
(3)宋代《洗冤集录》中记载有“银针探毒”,其原理是: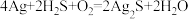 。该反应的还原剂是
。该反应的还原剂是___________ (填化学式,下同),还原产物是___________ 。用双线桥法表示该反应中转移电子数及氧化反应和还原反应:___________ 。
(4)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: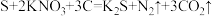 。该反应中,氧化剂是
。该反应中,氧化剂是___________ (填化学式,下同),氧化产物是___________ 。在上述反应中若有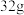 硫单质完全反应,被硫单质氧化的单质C的质量是
硫单质完全反应,被硫单质氧化的单质C的质量是___________ g。
(1)“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及到蜡烛与
 的燃烧反应,反应生成
的燃烧反应,反应生成 和
和 ,该反应一定是___________。
,该反应一定是___________。| A.化合反应 | B.分解反应 | C.氧化还原反应 | D.置换反应 |
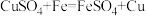 。该反应中被氧化的元素是
。该反应中被氧化的元素是(3)宋代《洗冤集录》中记载有“银针探毒”,其原理是:
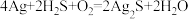 。该反应的还原剂是
。该反应的还原剂是(4)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
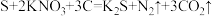 。该反应中,氧化剂是
。该反应中,氧化剂是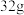 硫单质完全反应,被硫单质氧化的单质C的质量是
硫单质完全反应,被硫单质氧化的单质C的质量是
您最近半年使用:0次



