已知A、B、C、D、E是中学化学常见的几种元素,原子序数依次增大。
其结构或性质信息如下表所示:
(1)A元素位于___________ 区,A、B、C三种元素原子第一电离能由大到小顺序为:___________ (用元素符号填空);
(2)B、C、D三种元素原子电负性由大到小顺序为:___________ (用元素符号填空); 分子的空间构型:
分子的空间构型:___________ ;
(3)化合物EC、ED其化学键的离子键百分数较大的化合物为:___________ 。(用化学式填空)
其结构或性质信息如下表所示:
| 元素 | 结构或者信息 |
| A | 基态A原子p能级上有两个未成对电子 |
| B | 基态B原子中有7个运动状态不同的电子 |
| C | C元素是地壳中含量最高的元素 |
| D | 基态D的价层电子排布是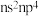 |
| E | 基态E原子次外层全充满,最外层电子数为1 |
(2)B、C、D三种元素原子电负性由大到小顺序为:
 分子的空间构型:
分子的空间构型:(3)化合物EC、ED其化学键的离子键百分数较大的化合物为:
更新时间:2024/04/29 11:37:47
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7价。回答下列问题:
(1)元素X原子结构示意图为_______ 。
(2)元素Y的最高价氧化物的电子式为_______ ;Y的最简单氢化物与O2在碱性条件可以形成原电池,该电池负极的电极反应为_______ 。
(3)元素Z在元素周期表中的位置是_______ ,其简单氢化物的沸点比同主族相邻元素的氢化物的沸点_______ (填“低”、“高”或“相等”),其原因为_______ 。
(4)ZW3常温下呈液态,可与水反应生成一种具有漂白性的酸和一种碱性气体,反应的化学方程式为_______ 。
(1)元素X原子结构示意图为
(2)元素Y的最高价氧化物的电子式为
(3)元素Z在元素周期表中的位置是
(4)ZW3常温下呈液态,可与水反应生成一种具有漂白性的酸和一种碱性气体,反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有四种短周期元素A、B、C、D,它们的核电荷数依次增大。A与C,B与D分别是同主族元素。B、D质子数之和是A、C质子数之和的2倍。这四种元素中A、C、D的单质均可在B的单质中燃烧。
(1)A的元素名称是________ ,C的元素符号是________ 。
(2)D元素位于元素周期表的第______ 周期第______ 族。
(3)C元素的单质在B的单质中燃烧的产物的化学式是________ 。
(1)A的元素名称是
(2)D元素位于元素周期表的第
(3)C元素的单质在B的单质中燃烧的产物的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】R、W、X、Y是原子序数依次增大的四种短周期元素。R最常见同位素的原子核中不含中子。W与X可形成两种稳定的化合物: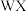 和
和 。工业革命以来,人类使用的化石燃料在燃烧过程中将大量
。工业革命以来,人类使用的化石燃料在燃烧过程中将大量 排入大气,在一定程度导致地球表面平均温度升高。Y与X是同一主族的元素,且在元素周期表中与X相邻。
排入大气,在一定程度导致地球表面平均温度升高。Y与X是同一主族的元素,且在元素周期表中与X相邻。
(1)W的原子结构示意图是_____ 。
(2) 的电子式是
的电子式是_____ 。
(3) 、
、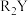 中,稳定性较高的是
中,稳定性较高的是_____ (填化学式)。
(4)Se与Y是同一主族的元素,且在元素周期表中与Y相邻。
①根据元素周期律,下列推断正确的是_____ (填字母序号)。
A. 的最高正化合价为
的最高正化合价为 价
价
B. 的还原性比
的还原性比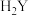 强
强
C. 的酸性比
的酸性比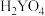 强
强
②Y最高价氧化物对应水化物可与 反应生成一种酸式盐,试写出该酸式盐在水溶液中的电离方程式为
反应生成一种酸式盐,试写出该酸式盐在水溶液中的电离方程式为_____ 。
③ 在一定条件下可与
在一定条件下可与 溶液反应,生成一种正盐和水,该正盐化学式为
溶液反应,生成一种正盐和水,该正盐化学式为_____ 。
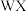 和
和 。工业革命以来,人类使用的化石燃料在燃烧过程中将大量
。工业革命以来,人类使用的化石燃料在燃烧过程中将大量 排入大气,在一定程度导致地球表面平均温度升高。Y与X是同一主族的元素,且在元素周期表中与X相邻。
排入大气,在一定程度导致地球表面平均温度升高。Y与X是同一主族的元素,且在元素周期表中与X相邻。(1)W的原子结构示意图是
(2)
 的电子式是
的电子式是(3)
 、
、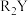 中,稳定性较高的是
中,稳定性较高的是(4)Se与Y是同一主族的元素,且在元素周期表中与Y相邻。
①根据元素周期律,下列推断正确的是
A.
 的最高正化合价为
的最高正化合价为 价
价B.
 的还原性比
的还原性比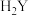 强
强C.
 的酸性比
的酸性比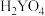 强
强②Y最高价氧化物对应水化物可与
 反应生成一种酸式盐,试写出该酸式盐在水溶液中的电离方程式为
反应生成一种酸式盐,试写出该酸式盐在水溶液中的电离方程式为③
 在一定条件下可与
在一定条件下可与 溶液反应,生成一种正盐和水,该正盐化学式为
溶液反应,生成一种正盐和水,该正盐化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】R、X、Y、Z是周期表前四周期元素,原子序数依次增大。R是宇宙中含量最多的元素,X、Y、Z三种元素的基态原子内层所有能级均已填满电子。X元素的基态原子的核外电子分布在三个能级上,且每个能级上排布了相同的电子数。Y与X同周期,且Y与X的基态原子中未成对电子数相同。Z的周期数比X的周期数多2,Z的基态原子最外层只有1个电子。回答下列问题:
(1)Z元素的价电子排布式为____________ 。
(2)R2Y可与Z的正二价离子形成一种复杂离子[Z(R2Y)4]2+,[Z(R2Y)4]2+的几何构型是______ ;将[Z(R2Y)4]2+与硫酸根形成的盐溶液装入试管中,逐滴加入氨水直至过量,出现的实验现象是______________ 。
(3)X与R可形成一种化学式为X3R4的不稳定化合物,是一种活性中间体,X3R4分子中3个X原子成直线排列,中间的X原子的杂化轨道类型为_____ 杂化。当X3R4分子中的4个R原子被其他4个不同种类元素的原子取代时,形成的新分子___ (填“具有“或”不具有”)手性。
(4)下列排列方式中,通常条件下Z的晶体的堆积方式是______ (填序号)。Z的晶体中,Z原子的配位数为________ 。
A.ABCABCABC B.ABABABABAB C.ABBAABBA D.ABCCBCABCCBA
(5)Z与F(氟)形成的一种化合物的晶胞结构如右图所示,若晶体密度为ag.cm-3,则Z与F(氟)最近距离为______ pm(阿伏伽德罗常数用NA表示,列出计算表达式,不用化简,1 pm=1. 0×10-12 m)。

(1)Z元素的价电子排布式为
(2)R2Y可与Z的正二价离子形成一种复杂离子[Z(R2Y)4]2+,[Z(R2Y)4]2+的几何构型是
(3)X与R可形成一种化学式为X3R4的不稳定化合物,是一种活性中间体,X3R4分子中3个X原子成直线排列,中间的X原子的杂化轨道类型为
(4)下列排列方式中,通常条件下Z的晶体的堆积方式是
A.ABCABCABC B.ABABABABAB C.ABBAABBA D.ABCCBCABCCBA
(5)Z与F(氟)形成的一种化合物的晶胞结构如右图所示,若晶体密度为ag.cm-3,则Z与F(氟)最近距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】下表为长式周期表的一部分,其中的编号代表对应的元素。试填空。
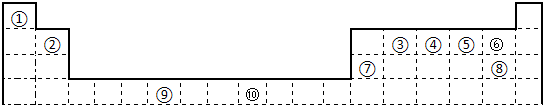
(1)写出上表中元素⑨原子的外围电子排布式________________________ 。
(2)元素③与⑧形成的化合物中元素③的杂化方式为:_______ 杂化,其形成的化合物的晶体类型是:_________________ 。
(3)元素④、⑤的第一电离能大小顺序是:____ >____ (用元素符号表示);元素④与元素①形成的X分子的空间构型为:___________ 。请写出与N3—互为等电子体的分子或离子的化学式__________ ,__________ (各写一种)。
(4)在测定①与⑥形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是:_______________________ 。
(5)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质,写出元素②的氢氧化物与NaOH溶液反应的化学方程式_____________ 。
(6)元素⑩在一定条件下形成的晶体的基本结构单元如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为:_________ 。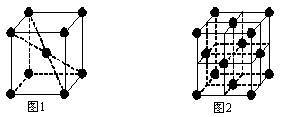

(1)写出上表中元素⑨原子的外围电子排布式
(2)元素③与⑧形成的化合物中元素③的杂化方式为:
(3)元素④、⑤的第一电离能大小顺序是:
(4)在测定①与⑥形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是:
(5)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质,写出元素②的氢氧化物与NaOH溶液反应的化学方程式
(6)元素⑩在一定条件下形成的晶体的基本结构单元如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为:

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氨硼烷( )是一种具有研究价值的固体储氢材料。
)是一种具有研究价值的固体储氢材料。
已知: 含氢19.5%,白色晶体,熔点为104℃。可溶于水和甲醇等溶剂中。常温常压下能够稳定存在。在催化剂存在的情况下,
含氢19.5%,白色晶体,熔点为104℃。可溶于水和甲醇等溶剂中。常温常压下能够稳定存在。在催化剂存在的情况下, 能够快速与水反应。
能够快速与水反应。
(1)基态N原子的核外电子排布的轨道表示式为_______ 。
(2)B的第一电离能低于Be,可能的原因是_______ 。
(3) 分子结构示意图如图1,其中N-H为
分子结构示意图如图1,其中N-H为_______ 键(填序号,下同),N-B为_______ 键。
a.配位键 b.非极性键 c. 键 d.
键 d. 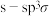 键
键 在某种催化剂表面与
在某种催化剂表面与 反应的释氢机理如图2。写出理论上
反应的释氢机理如图2。写出理论上 与
与 完全反应的总反应的离子方程式:
完全反应的总反应的离子方程式:_______ 。 在低温高压条件下为正交晶系结构,
在低温高压条件下为正交晶系结构, 的
的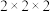 超晶胞结构如图3所示(超晶胞内含有16个氨硼烷分子,
超晶胞结构如图3所示(超晶胞内含有16个氨硼烷分子,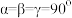 )。氨硼烷晶体的密度为
)。氨硼烷晶体的密度为_______ g·m 。
。
(已知:1pm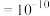 cm;
cm; 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
 )是一种具有研究价值的固体储氢材料。
)是一种具有研究价值的固体储氢材料。已知:
 含氢19.5%,白色晶体,熔点为104℃。可溶于水和甲醇等溶剂中。常温常压下能够稳定存在。在催化剂存在的情况下,
含氢19.5%,白色晶体,熔点为104℃。可溶于水和甲醇等溶剂中。常温常压下能够稳定存在。在催化剂存在的情况下, 能够快速与水反应。
能够快速与水反应。元素 | H | B | N |
电负性 | 2.1 | 2.0 | 3.0 |
(1)基态N原子的核外电子排布的轨道表示式为
(2)B的第一电离能低于Be,可能的原因是
(3)
 分子结构示意图如图1,其中N-H为
分子结构示意图如图1,其中N-H为a.配位键 b.非极性键 c.
 键 d.
键 d. 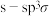 键
键
 在某种催化剂表面与
在某种催化剂表面与 反应的释氢机理如图2。写出理论上
反应的释氢机理如图2。写出理论上 与
与 完全反应的总反应的离子方程式:
完全反应的总反应的离子方程式:
 在低温高压条件下为正交晶系结构,
在低温高压条件下为正交晶系结构, 的
的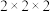 超晶胞结构如图3所示(超晶胞内含有16个氨硼烷分子,
超晶胞结构如图3所示(超晶胞内含有16个氨硼烷分子,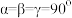 )。氨硼烷晶体的密度为
)。氨硼烷晶体的密度为 。
。(已知:1pm
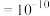 cm;
cm; 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
您最近一年使用:0次
【推荐1】一种新型漂白剂(结构如图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,Z电子只有一种自旋取向;W、Y、Z的最外层电子数之和等于X的最外层电子数,X基态原子核外有两个单电子,W、X对应的简单离子核外电子排布相同。

回答下列问题:
(1)写出元素Y在周期表中的位置是:_______ ,所属分区是:_____ 。
(2)写出元素X简单离子的核外电子排布式:________ 。
(3)元素X基态原子核外电子的运动状态有_____ 种,占据的原子轨道有____ 个。
(4)W、X、Y电负性由大到小的顺序是_______ (用元素符号表示)。
(5)试解释W的第一电离能大于 的第一电离能的原因:
的第一电离能的原因:___________ 。

回答下列问题:
(1)写出元素Y在周期表中的位置是:
(2)写出元素X简单离子的核外电子排布式:
(3)元素X基态原子核外电子的运动状态有
(4)W、X、Y电负性由大到小的顺序是
(5)试解释W的第一电离能大于
 的第一电离能的原因:
的第一电离能的原因:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是________ ,B是________ ,E是_________ 。
(2) 写出C元素基态原子的电子排布式_________________________ 。
(3)写出D元素原子的价电子排布图____________________ 。
(4) 元素B与D的电负性的大小关系是___________ ,C与E的第一电离能的大小关系是___________ 。(填“>”、“<”或“=”)
(1)A是
(2) 写出C元素基态原子的电子排布式
(3)写出D元素原子的价电子排布图
(4) 元素B与D的电负性的大小关系是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】磷酸氯喹在细胞水平上能有效抑制新型冠状病毒(SARS-CoV-2)的感染。磷酸氯喹的结构如图所示,据此回答下列问题。_____ 。
(2)C、N、O三种元素电负性从大到小的顺序为_____ ;第一电离能I1(P)_____ I1(Cl)(填“>”或“<”)。
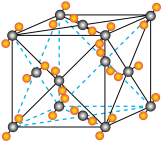
(3)钴的一种化合物的晶胞结构如图所示,已知A点的原子坐标参数为(0,0,0),B点为( ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为_____ 。_____ (用化学式表示)。_____ 。

(2)C、N、O三种元素电负性从大到小的顺序为
(3)钴的一种化合物的晶胞结构如图所示,已知A点的原子坐标参数为(0,0,0),B点为(
 ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为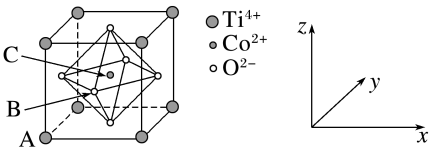

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如图,As原子的杂化方式为_______ ,雌黄和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4并放出H2S气体,SnCl4的结构与SiCl4相似,其分子的空间结构为_______ 。

(2)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间结构为_______ ,C原子的杂化方式为_______ ;明代宋应星所著的《天工开物》中记载了利用C和ZnCO3进行火法炼锌的反应,反应中还生成一种具有还原性的气体,请写出上述的化学方程式:_______ 。
(3)某绿色农药结构简式如图,回答下列问题:

分子中编号为①的碳原子和与其成键的另外几个原子构成的空间结构为_______ ;试比较CO2、H2O、CCl4三种分子的键角_______ (按由大到小顺序排列)。
(1)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如图,As原子的杂化方式为

(2)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间结构为
(3)某绿色农药结构简式如图,回答下列问题:

分子中编号为①的碳原子和与其成键的另外几个原子构成的空间结构为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】2022年,比亚迪推出最新型的磷酸铁锂“刀片电池”,该电池具有能量密度更大,安全性更高的特点。电池的正极活性材料是 。请回答下列问题:
。请回答下列问题:
(1)元素Li在元素周期表中的位置__________ ,与Li元素处于同一主族,且能与氧气反应生成两种氧化物,该元素的基态原子电子排布式是__________ ,具有非极性共价键的氧化物的电子式为__________ 。
(2)基态 原子中含有
原子中含有__________ 个单电子,最高能级的能级符号是__________ 。基态 最外层有
最外层有__________ 个原子轨道。
(3)正极活性材料 中
中 中心原子的杂化类型是
中心原子的杂化类型是__________ , 的空间构型是
的空间构型是__________ 。
(4) 能形成很多种配位化合物,
能形成很多种配位化合物,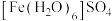 配合物的名称是
配合物的名称是__________ 。 与
与 可以形成
可以形成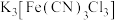 配合物,其中提供孤电子对的元素是
配合物,其中提供孤电子对的元素是__________ 。
 。请回答下列问题:
。请回答下列问题:(1)元素Li在元素周期表中的位置
(2)基态
 原子中含有
原子中含有 最外层有
最外层有(3)正极活性材料
 中
中 中心原子的杂化类型是
中心原子的杂化类型是 的空间构型是
的空间构型是(4)
 能形成很多种配位化合物,
能形成很多种配位化合物,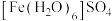 配合物的名称是
配合物的名称是 与
与 可以形成
可以形成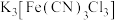 配合物,其中提供孤电子对的元素是
配合物,其中提供孤电子对的元素是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩。
(1)基态砷原子的电子排布式为_________ ;砷与溴的第一电离能较大的是_________ 。
(2)AsH3是无色稍有大蒜味气体。AsH3的沸点高于PH3,其主要原因是_________ 。
(3)Na3AsO4可作杀虫剂。AsO43-的空间构型为_________ ,与其互为等电子体的一种分子为__________ 。

(4)某砷的氧化物俗称“砒霜”,其分子结构如右图所示。该化合物的分子式为_________ ,As原子采取___________ 杂化。
(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与_______ 个Ga相连,As与Ga之间存在的化学键有________ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键 E.配位键 F.金属键 G.极性键
(1)基态砷原子的电子排布式为
(2)AsH3是无色稍有大蒜味气体。AsH3的沸点高于PH3,其主要原因是
(3)Na3AsO4可作杀虫剂。AsO43-的空间构型为

(4)某砷的氧化物俗称“砒霜”,其分子结构如右图所示。该化合物的分子式为
(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与
A.离子键 B.σ键 C.π键 D.氢键 E.配位键 F.金属键 G.极性键
您最近一年使用:0次



