砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩。
(1)基态砷原子的电子排布式为_________ ;砷与溴的第一电离能较大的是_________ 。
(2)AsH3是无色稍有大蒜味气体。AsH3的沸点高于PH3,其主要原因是_________ 。
(3)Na3AsO4可作杀虫剂。AsO43-的空间构型为_________ ,与其互为等电子体的一种分子为__________ 。

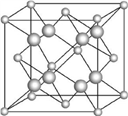
(4)某砷的氧化物俗称“砒霜”,其分子结构如右图所示。该化合物的分子式为_________ ,As原子采取___________ 杂化。
(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与_______ 个Ga相连,As与Ga之间存在的化学键有________ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键 E.配位键 F.金属键 G.极性键
(1)基态砷原子的电子排布式为
(2)AsH3是无色稍有大蒜味气体。AsH3的沸点高于PH3,其主要原因是
(3)Na3AsO4可作杀虫剂。AsO43-的空间构型为

(4)某砷的氧化物俗称“砒霜”,其分子结构如右图所示。该化合物的分子式为
(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与
A.离子键 B.σ键 C.π键 D.氢键 E.配位键 F.金属键 G.极性键
11-12高三上·江苏南京·阶段练习 查看更多[1]
(已下线)2012届江苏省南京市四校高三12月月考化学试卷
更新时间:2016-12-09 02:31:42
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】【化学一选修3:物质结构与性质】
某原料经测定主要含有A、B、C、D、E五种原子序数依次增大的前四周期元素,其相关信息如下:
请回答下列问题(用A、B、C、D、E所对应的元素符号作答):
(1) B、C、D第一电离能由大到小的顺序为_____ 。
(2) E的二价离子的电子排布式为_____ 。
(3) A2B2D4常用作除锈剂,该分子中B的杂化方式为_____ ;1 mol A2B2D4分子中含有σ键与π键的数目之比为_____ 。
(4) 与化合物BD互为等电子体的阴离子的化学式为_____ (任写一种)。
(5) B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是___ 。
(6) 一种E和金(Au)形成的合金晶体具有面心立方最密堆积结构,其晶胞中E原子处于面心,Au原子处于顶点,则该合金中E原子与Au原子的个数之比为___ ;若相临两个Au原子的最短距离为a厘米,则该合金的密度为_____ g/cm3。又知上述晶体具有储氢功能,氢原子可进入到由E原子与Au原子构成的四面体空隙中。若将E原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(见图)的结构相似,该晶体储氢后的化学式应为_____ 。
某原料经测定主要含有A、B、C、D、E五种原子序数依次增大的前四周期元素,其相关信息如下:
| 元素 | 元素性质或原子结构 |
| A | 周期表中原子半径最小的元素 |
| B | 原子核外有三种不同的能级且各个能级所填充的电子数相同 |
| C | 最外层p轨道半充满 |
| D | 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 |
| E | 位于ds区且原子的最外层电子数与A的相同 |
请回答下列问题(用A、B、C、D、E所对应的元素符号作答):
(1) B、C、D第一电离能由大到小的顺序为
(2) E的二价离子的电子排布式为
(3) A2B2D4常用作除锈剂,该分子中B的杂化方式为
(4) 与化合物BD互为等电子体的阴离子的化学式为
(5) B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是
(6) 一种E和金(Au)形成的合金晶体具有面心立方最密堆积结构,其晶胞中E原子处于面心,Au原子处于顶点,则该合金中E原子与Au原子的个数之比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】学科融合是现代发展的大趋势,化学家利用氮族元素、VIII族元素和氧族元素合成了具有具有特定功能的晶体。
(1)第VIII族元素中的Fe、Co、 Ni都是常见金属,Co 的价电子排布式为_______ ,Fe3+比Fe2+稳定的原因是_______ 。
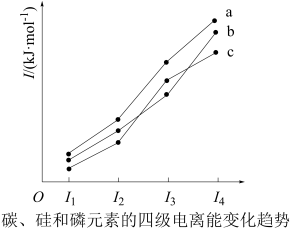
(2)P与Br可形成多种化合物,下图表示磷、硅、碳的四级电离变化趋势,其中表示磷元素的曲线是_______ (填标号),PBr3的空间结构为_______ ,PBr5为阴阳离子比为1:1的导电熔体,阴阳离子均带一个单位电荷,阴离子为单核微粒,其中P原子的杂化轨道类型为_______ 。
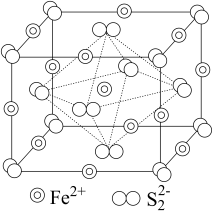
(3)FeS2晶体的晶胞如图所示。晶胞边长为a nm、FeS2相对分子质量为M,阿伏加德罗常数的值为NA其晶体密度的计算表达式为_______ g·cm-3;晶胞中Fe2+位于 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为_______ nm。
(1)第VIII族元素中的Fe、Co、 Ni都是常见金属,Co 的价电子排布式为
(2)P与Br可形成多种化合物,下图表示磷、硅、碳的四级电离变化趋势,其中表示磷元素的曲线是

(3)FeS2晶体的晶胞如图所示。晶胞边长为a nm、FeS2相对分子质量为M,阿伏加德罗常数的值为NA其晶体密度的计算表达式为
 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
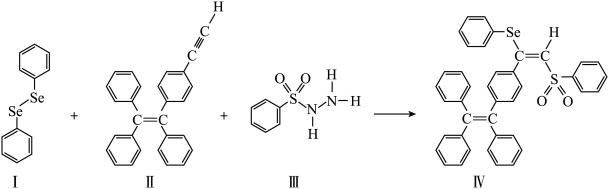
【推荐3】硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料、生物医学等领域引起广泛关注。一种含Se的新型AIE分子IV的合成路线如图:
(1)Se与S同族,基态硒原子价电子排布式为_____ 。
(2) 的沸点低于H2O,其原因是
的沸点低于H2O,其原因是_____ 。
(3)关于I~III三种反应物,下列说法正确的有_____ (填标号)。
A.I中仅有σ键
B.I中的Se-Se为非极性共价键
C.II易溶于水
D.III中原子的杂化轨道类型有sp与sp2
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_____ 。
(5)研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒,SeO 的空间结构为
的空间结构为_____ 。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
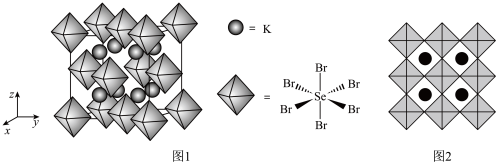
①X的化学式为_____ 。
②设X的最简式的式量为Mr,晶体密度为ρg•cm-3,则X中相邻K之间的最短距离为_____ nm(列出计算式,NA为阿伏加德罗常数的值)。

(1)Se与S同族,基态硒原子价电子排布式为
(2)
 的沸点低于H2O,其原因是
的沸点低于H2O,其原因是(3)关于I~III三种反应物,下列说法正确的有
A.I中仅有σ键
B.I中的Se-Se为非极性共价键
C.II易溶于水
D.III中原子的杂化轨道类型有sp与sp2
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有
(5)研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒,SeO
 的空间结构为
的空间结构为(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为
②设X的最简式的式量为Mr,晶体密度为ρg•cm-3,则X中相邻K之间的最短距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】硒是人体不可缺少的微量元素,铈是稀土元素中丰度最大的元素,它们的化合物在生产、生活中有着广泛的应用。回答下列问题:

(1)基态Se原子的核外价电子轨道表示式为_____ 。
(2)“依布硒”是一种有机硒化物,具有良好的抗炎活性,其结构简式如图1所示。“依布硒”中 原子的杂化类型为
原子的杂化类型为_____ ,元素Se、O、N的第一电离能由大到小的顺序为_____ 。
(3)硒的某种链状聚合氧化物结构如图2所示,其化学式为_____ 。
(4)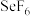 与
与 具有相似的结构,室温时,
具有相似的结构,室温时,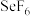 是一种气体。沸点高低:
是一种气体。沸点高低: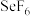
_____  (填“>”或“<”或“=”),原因是
(填“>”或“<”或“=”),原因是_____ 。
(5)二硫键和二硒键是重要的光响应动态共价键,其光响应原理如图3所示。已知光的波长与其能量成反比,则图中实现光响应的波长:
_____  (填“”或“”或“”)。
(填“”或“”或“”)。

(6)二氧化铈( )氧载体具有良好的储氧放氧能力,可用于甲烷化学链重整,其原理如下图所示。
)氧载体具有良好的储氧放氧能力,可用于甲烷化学链重整,其原理如下图所示。

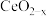 中
中
_____ , 和
和 个数比为
个数比为_____ 。

(1)基态Se原子的核外价电子轨道表示式为
(2)“依布硒”是一种有机硒化物,具有良好的抗炎活性,其结构简式如图1所示。“依布硒”中
 原子的杂化类型为
原子的杂化类型为(3)硒的某种链状聚合氧化物结构如图2所示,其化学式为
(4)
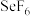 与
与 具有相似的结构,室温时,
具有相似的结构,室温时,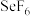 是一种气体。沸点高低:
是一种气体。沸点高低: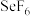
 (填“>”或“<”或“=”),原因是
(填“>”或“<”或“=”),原因是(5)二硫键和二硒键是重要的光响应动态共价键,其光响应原理如图3所示。已知光的波长与其能量成反比,则图中实现光响应的波长:

 (填“”或“”或“”)。
(填“”或“”或“”)。
(6)二氧化铈(
 )氧载体具有良好的储氧放氧能力,可用于甲烷化学链重整,其原理如下图所示。
)氧载体具有良好的储氧放氧能力,可用于甲烷化学链重整,其原理如下图所示。
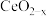 中
中
 和
和 个数比为
个数比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氮及其化合物广泛存在于自然界中。回答下列问题:
(1)写出N原子的电子排布式_____________ 。在基态14N原子中,核外存在___________ 个未成对电子。
(2)原子第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,C、N、O原子的第一电离能由大到小的顺序为_______________ 。
(3)氮气和氢气在一定条件下可合成氨,氨分子中氮原子的杂化方式为_____________ 杂化。
(4)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8K,主要原因是_________ 。
(5)X的+1价阳离子中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是________ ,X离子与N3-形成的化合物化学式为____________ 。
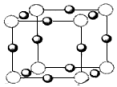
(6)假设X+的半径为a cm,N3-的半径为b cm,且X+与N3-都是紧密接触的刚性小球,则该氮化物的密度为_____________ g.cm-3。
(1)写出N原子的电子排布式
(2)原子第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,C、N、O原子的第一电离能由大到小的顺序为
(3)氮气和氢气在一定条件下可合成氨,氨分子中氮原子的杂化方式为
(4)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8K,主要原因是
(5)X的+1价阳离子中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是

(6)假设X+的半径为a cm,N3-的半径为b cm,且X+与N3-都是紧密接触的刚性小球,则该氮化物的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】不锈钢的种类很多,其中一种铁元素以外,还含有较多的Cr(铬)、Ni(镍)、Mo(钼),少量的Si(硅)、C(碳),微量的S(硫)、P(磷)。
(1)上述元素中属于第三周期且第一电离能从大到小排列的是_______
(2)Mo(钼)处于第五周期,且与Cr(铬)元素位于同一族,则基态Mo(钼)原子的外围电子(价电子)排布式是_______ 。
(3)CH4的沸点比SiH4低,原因是_______ 。
(4)镍元素能形成多种配合物,配离子[Ni(CN)4]2—中不含有的是____ (填选项编号)。
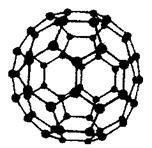
(5)碳元素有多种单质,其中C60分子有独特的球形结构:C60分子中原子轨道杂化类型是_______ 。
(6)碳的另一种单质石墨呈层状结构,有一碳镁新型材料就是在石墨碳原子层间加入镁原子层,两层俯视图:
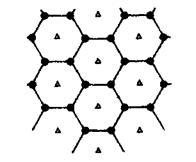
该材料的化学式为_______ 。
A. 离子键 B. 配位键 C. σ键 D. π键E.氢键
(1)上述元素中属于第三周期且第一电离能从大到小排列的是
(2)Mo(钼)处于第五周期,且与Cr(铬)元素位于同一族,则基态Mo(钼)原子的外围电子(价电子)排布式是
(3)CH4的沸点比SiH4低,原因是
(4)镍元素能形成多种配合物,配离子[Ni(CN)4]2—中不含有的是
(5)碳元素有多种单质,其中C60分子有独特的球形结构:C60分子中原子轨道杂化类型是

(6)碳的另一种单质石墨呈层状结构,有一碳镁新型材料就是在石墨碳原子层间加入镁原子层,两层俯视图:

该材料的化学式为
A. 离子键 B. 配位键 C. σ键 D. π键E.氢键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】杂环化合物数量巨大、种类丰富、性能多样、应用广泛。
(1)由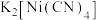 、
、 和吡嗪(
和吡嗪( 可用pyz表示)反应制得晶体,其化学式为
可用pyz表示)反应制得晶体,其化学式为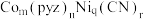 ,四方晶胞结构如图所示。基态Co原子的简化电子排布式为
,四方晶胞结构如图所示。基态Co原子的简化电子排布式为_______ ,C、N、O的第二电离能由大到小顺序为_______ ,晶体中 与
与 的配位数之比为
的配位数之比为_______ ,上述制得晶体的化学方程式为_______ 。 )分子中存在
)分子中存在 离域
离域 键,氮原子的杂化方式
键,氮原子的杂化方式_______ ;吡嗪的熔点_______ (填“大于”、“等于”、“小于”)哒嗪( );哒嗪在水中的溶解度大于苯的原因
);哒嗪在水中的溶解度大于苯的原因_______ 。
(3)休克尔规则可用于判断共轭结构的环状有机化合物是否有芳香性。若参与构成共轭 键电子的个数为
键电子的个数为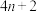 ,其中n为自然数,则此化合物就具有芳香性。下列物质中C、N、O均采用
,其中n为自然数,则此化合物就具有芳香性。下列物质中C、N、O均采用 杂化,其中具有芳香性的是
杂化,其中具有芳香性的是_______ 。
(1)由
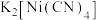 、
、 和吡嗪(
和吡嗪( 可用pyz表示)反应制得晶体,其化学式为
可用pyz表示)反应制得晶体,其化学式为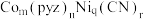 ,四方晶胞结构如图所示。基态Co原子的简化电子排布式为
,四方晶胞结构如图所示。基态Co原子的简化电子排布式为 与
与 的配位数之比为
的配位数之比为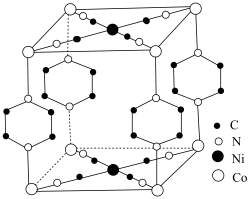
 )分子中存在
)分子中存在 离域
离域 键,氮原子的杂化方式
键,氮原子的杂化方式 );哒嗪在水中的溶解度大于苯的原因
);哒嗪在水中的溶解度大于苯的原因(3)休克尔规则可用于判断共轭结构的环状有机化合物是否有芳香性。若参与构成共轭
 键电子的个数为
键电子的个数为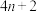 ,其中n为自然数,则此化合物就具有芳香性。下列物质中C、N、O均采用
,其中n为自然数,则此化合物就具有芳香性。下列物质中C、N、O均采用 杂化,其中具有芳香性的是
杂化,其中具有芳香性的是a. 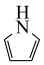 b.
b.  c.
c.  d.
d.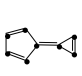
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】黄铜矿(CuFeS2)是最重要的铜矿,全世界三分之二的铜是由它提炼的。
铜矿冶炼过程中发生的反应有:2CuFeS2+O2=Cu2S+2FeS+SO2 ;2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S=6Cu+SO2
回答下列问题:
(1)Cu属于_____ 区的元素,黄铜矿中铜离子基态外围电子排布式为_____________ 。
(2)铜矿冶炼过程中产生的SO2可用于生产硫酸,SO2的空间构型为___________ ,中心原子的杂化方式为__________ 。冶炼过程还产生了Cu2S 、Cu2O,其中熔点较高的是______________ ,原因是_______________ 。
(3)黄铜矿不溶于稀硫酸,但可以溶解在稀硝酸中,硝酸将其中的铁、硫元素氧化到高价态,可以用黄血盐K4[Fe(CN)6]检验Fe3+的存在,1 mol K4[Fe(CN)6]中含有的σ键的数目为_______________ 。
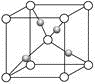
(4)Cu2O晶体的晶胞如图所示,晶胞的密度为ρ g/cm3,阿伏伽德罗常数的值为NA,则Cu原子配位数为__________ ,最近的两个O原子之间的距离为____________ nm。
铜矿冶炼过程中发生的反应有:2CuFeS2+O2=Cu2S+2FeS+SO2 ;2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S=6Cu+SO2
回答下列问题:
(1)Cu属于
(2)铜矿冶炼过程中产生的SO2可用于生产硫酸,SO2的空间构型为
(3)黄铜矿不溶于稀硫酸,但可以溶解在稀硝酸中,硝酸将其中的铁、硫元素氧化到高价态,可以用黄血盐K4[Fe(CN)6]检验Fe3+的存在,1 mol K4[Fe(CN)6]中含有的σ键的数目为
(4)Cu2O晶体的晶胞如图所示,晶胞的密度为ρ g/cm3,阿伏伽德罗常数的值为NA,则Cu原子配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】回答下列问题:
(1)①基态Ni原子价层电子的电子排布图为_______ 。
②含有4个水分子的醋酸镍[Ni(C2H3O2)2·4H2O]构型为八面体,则中心Ni原子的配位数为_______ 。
(2)富马酸 结构中,碳原子的杂化类型是
结构中,碳原子的杂化类型是_______ ,其中元素的电负性由大到小排序为_______ 。
(3)NaBH4是有机合成中常用的还原剂,BH 离子的空间构型为
离子的空间构型为_______ ,与BH 互为等电子体的一种阳离子为
互为等电子体的一种阳离子为_______ (填离子符号), NaBH4中存在_______ (填字母)。
A.离子键 B.σ键 C. π键 D.氢键
(4)OF2的熔、沸点低于Cl2O,原因是_______ 。
(5)TiO2通过氮掺杂反应生成TiO2-aNb,表示如图。

①立方晶系TiO2晶胞参数如图甲所示,其晶体的密度为_______ g/cm3
②图乙TiO2-aNb晶体中a=_______ 。
(1)①基态Ni原子价层电子的电子排布图为
②含有4个水分子的醋酸镍[Ni(C2H3O2)2·4H2O]构型为八面体,则中心Ni原子的配位数为
(2)富马酸
 结构中,碳原子的杂化类型是
结构中,碳原子的杂化类型是(3)NaBH4是有机合成中常用的还原剂,BH
 离子的空间构型为
离子的空间构型为 互为等电子体的一种阳离子为
互为等电子体的一种阳离子为A.离子键 B.σ键 C. π键 D.氢键
(4)OF2的熔、沸点低于Cl2O,原因是
(5)TiO2通过氮掺杂反应生成TiO2-aNb,表示如图。

①立方晶系TiO2晶胞参数如图甲所示,其晶体的密度为
②图乙TiO2-aNb晶体中a=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D、E、F、G是原子序数依次增大的前四周期元素,其中A是最轻的元素;B元素基态原子的最外层有2个未成对电子;D元素原子的价层电子排布式为 ;E元素的原子只有两种形状的电子云,最外层只有一种自旋方向的电子;F元素原子有5个未成对电子;G元素基态的正三价离子的3d轨道为半充满状态。请回答下列问题:
;E元素的原子只有两种形状的电子云,最外层只有一种自旋方向的电子;F元素原子有5个未成对电子;G元素基态的正三价离子的3d轨道为半充满状态。请回答下列问题:
(1)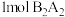 分子中有
分子中有_______  个
个 键、
键、_______  个
个 键。
键。
(2)比较熔沸点:BD_______ (填“高于”、“低于”或“等于”) 原因是
原因是_______ 。
(3)基态E原子中电子占据的最高能级的原子轨道形状为_______ ,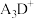 的立体构型为
的立体构型为_______ 。
(4)F是正常机体必需的微量元素之一,它构成体内若干种有重要作用的酶。F在元素周期表中的位置为_______ ,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子更难的原因是
再失去一个电子更难的原因是_______ 。
 ;E元素的原子只有两种形状的电子云,最外层只有一种自旋方向的电子;F元素原子有5个未成对电子;G元素基态的正三价离子的3d轨道为半充满状态。请回答下列问题:
;E元素的原子只有两种形状的电子云,最外层只有一种自旋方向的电子;F元素原子有5个未成对电子;G元素基态的正三价离子的3d轨道为半充满状态。请回答下列问题:(1)
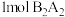 分子中有
分子中有 个
个 键、
键、 个
个 键。
键。(2)比较熔沸点:BD
 原因是
原因是(3)基态E原子中电子占据的最高能级的原子轨道形状为
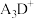 的立体构型为
的立体构型为(4)F是正常机体必需的微量元素之一,它构成体内若干种有重要作用的酶。F在元素周期表中的位置为
 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子更难的原因是
再失去一个电子更难的原因是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】丁位辛内酯H(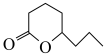 )可作为一种食品香料。其合成路线为:
)可作为一种食品香料。其合成路线为:
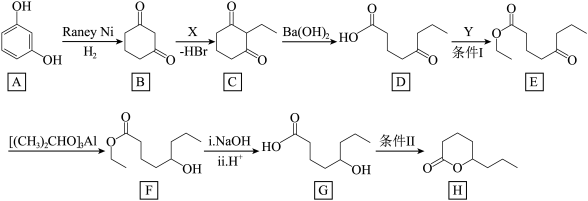
回答下列问题:
(1)A的化学名称是___________ 。A的两种同分异构体结构分别为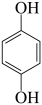 (M)和
(M)和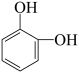 (N),其沸点M
(N),其沸点M___________ N(填“高于”或“低于”)。
(2)写出反应D→E的化学方程式___________ 。
(3)E具有的官能团名称是___________ 。
(4)反应B→C中,X的结构简式为___________ 。
(5)E→F的反应类型是___________ 。
(6)Q是B的同分异构体,满足下列条件的Q的结构共有___________ 种(不考虑同一碳原子上存在两个双键的情况)。
①Q中不含环和三键;②能与NaOH溶液反应但不能与NaHCO3溶液反应;③不能发生银镜反应
若Q有下列转化关系: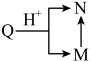 一定条件下氧化,则Q的结构简式是
一定条件下氧化,则Q的结构简式是___________ 。
 )可作为一种食品香料。其合成路线为:
)可作为一种食品香料。其合成路线为:
回答下列问题:
(1)A的化学名称是
 (M)和
(M)和 (N),其沸点M
(N),其沸点M(2)写出反应D→E的化学方程式
(3)E具有的官能团名称是
(4)反应B→C中,X的结构简式为
(5)E→F的反应类型是
(6)Q是B的同分异构体,满足下列条件的Q的结构共有
①Q中不含环和三键;②能与NaOH溶液反应但不能与NaHCO3溶液反应;③不能发生银镜反应
若Q有下列转化关系:
 一定条件下氧化,则Q的结构简式是
一定条件下氧化,则Q的结构简式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】化学物质结构与性质按要求回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________形象化描述;在基态14C原子中,核外存在___________对自旋相反的电子。
(2)在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接___________个六元环,六元环中最多有___________个C原子在同一平面,一个金刚石晶胞平均占有碳原子个数为___________。
(3)与N2互为等电子体的分子是___________,该分子的电子式为___________。
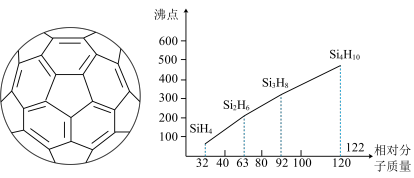
(4)已知C60分子结构如图所示:该笼状分子是由多个正六边形和正五边形组成的,面体的顶点数V、面数F及棱数E间关系为:V+F-E=2,则此分子中共有___________个正五边形。
(5)硅烷(SinH2n+2)的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是___________。

(6) NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为___________ cm(用含有a的代数式表示),在一定温度下NiO晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为___________g(氧离子的半径为1.40×10-10m )。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________形象化描述;在基态14C原子中,核外存在___________对自旋相反的电子。
(2)在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接___________个六元环,六元环中最多有___________个C原子在同一平面,一个金刚石晶胞平均占有碳原子个数为___________。
(3)与N2互为等电子体的分子是___________,该分子的电子式为___________。
(4)已知C60分子结构如图所示:该笼状分子是由多个正六边形和正五边形组成的,面体的顶点数V、面数F及棱数E间关系为:V+F-E=2,则此分子中共有___________个正五边形。
(5)硅烷(SinH2n+2)的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是___________。


(6) NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为___________ cm(用含有a的代数式表示),在一定温度下NiO晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为___________g(氧离子的半径为1.40×10-10m )。
您最近一年使用:0次



