由γ-羟基丁酸生成γ-丁内酯的反应为HOCH2CH2CH2COOH
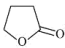 +H2O
+H2O  H<0,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间变化的数据如图所示:
H<0,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间变化的数据如图所示:
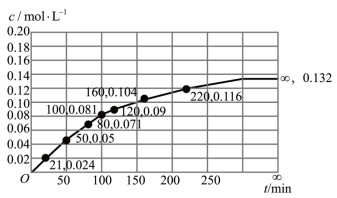
A.在50~80min内,以γ-丁内酯的浓度变化表示的反应速率为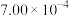 mol/(L⋅min) mol/(L⋅min) |
B.在25℃时,该反应的平衡常数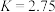 |
| C.加水降低γ-羟基丁酸的初始浓度,γ-羟基丁酸的平衡转化率减小 |
| D.使用非水溶剂并通过共沸回流移除体系中的水,有助于提高γ-丁内酯的平衡产率 |
2024·黑龙江·模拟预测 查看更多[1]
(已下线)化学(新七省高考卷02)(14+4模式)-2024年高考押题预测卷
更新时间:2024-05-01 21:40:10
|
相似题推荐
单选题
|
较难
(0.4)
名校
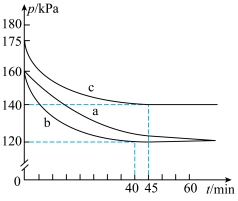
【推荐1】煤燃烧排放的烟气含有SO2和NOx,对烟气进行脱硫、脱硝,对环境保护有着重要意义。在脱硫实验中发生反应: 2CO(g) + SO2(g)  2CO2(g)+S(s) ΔH<0,在体积为 2 L的恒容密闭容器中,通入2.2 molCO和1 mol SO2,在不同条件下进行反应时体系的总压强随时间的变化如图所示。下列说法错误的是
2CO2(g)+S(s) ΔH<0,在体积为 2 L的恒容密闭容器中,通入2.2 molCO和1 mol SO2,在不同条件下进行反应时体系的总压强随时间的变化如图所示。下列说法错误的是
 2CO2(g)+S(s) ΔH<0,在体积为 2 L的恒容密闭容器中,通入2.2 molCO和1 mol SO2,在不同条件下进行反应时体系的总压强随时间的变化如图所示。下列说法错误的是
2CO2(g)+S(s) ΔH<0,在体积为 2 L的恒容密闭容器中,通入2.2 molCO和1 mol SO2,在不同条件下进行反应时体系的总压强随时间的变化如图所示。下列说法错误的是
| A.与a相比,c可能改变的条件为升高温度 |
| B.a和b的化学平衡常数相等 |
| C.b对应40min达到平衡,则在0~40min内用CO表示的平均反应速率为0.02mol·L-1·min-1 |
| D.a达到平衡时,SO2的转化率小于CO的转化率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在1 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
下列说法错误的是
 M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.10 | 0.10 | 0.09 |
② | 800 | 0.20 | 0.20 | 0.10 |
③ | 800 | 0.20 | 0. 30 | a |
④ | 900 | 0.10 | 0.15 | b |
| A.实验①中,若5 min时测得n(M) =0.05 mol,则0至5 min时间内,用N表示的平均反应速率v(N) =0.01 mol/( L·min) |
| B.实验②中,该反应的平衡常数K=1.0 |
| C.实验③中,达到平衡时,X的转化率为60% |
| D.实验④中,达到平衡时,b>0.06 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】为了探究反应速率的影响因素,某同学通过碳酸钙与稀盐酸的反应,绘制出收集到的 CO2体积与反应时间的关系图(0-t1、t1-t2、t2-t3的时间间隔相等)。下列说法正确的是

A.0-t1时间段,CO2的化学反应速率 v= mol/(L·min) mol/(L·min) |
| B.t1-t2与 0-t1比较,反应速率加快的原因可能是产生的 CO2气体增多 |
| C.t2-t4时间段,反应速率逐渐减慢的原因可能是盐酸浓度减小 |
| D.在 t4 后,收集到的气体的体积不再增加说明碳酸钙消耗完全 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】一定条件下,在容积为2 L的恒容密闭容器中通入2 mol  发生反应
发生反应 ,一定温度下,测得
,一定温度下,测得 的转化率随时间的变化曲线如图所示,在60 min时反应达到平衡状态。
的转化率随时间的变化曲线如图所示,在60 min时反应达到平衡状态。

下列说法错误的是
 发生反应
发生反应 ,一定温度下,测得
,一定温度下,测得 的转化率随时间的变化曲线如图所示,在60 min时反应达到平衡状态。
的转化率随时间的变化曲线如图所示,在60 min时反应达到平衡状态。
下列说法错误的是
| A.a点处的逆反应速率小于b点处的正反应速率 |
B.0~10 min内, 的平均反应速率 的平均反应速率 |
C.其他条件不变,若在恒压条件下发生反应,平衡时 的转化率大于50% 的转化率大于50% |
D.60 min后,保持温度不变,向该容器中再通入0.5 mol  和1 mol 和1 mol  ,则反应逆向进行 ,则反应逆向进行 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】反应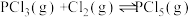 在容积为10L的密闭容器中进行。起始时PCl3和Cl2均为0.2mol,反应在不同条件下进行,反应体系的总压强随时间的变化如图所示。由图像不能得出的结论是
在容积为10L的密闭容器中进行。起始时PCl3和Cl2均为0.2mol,反应在不同条件下进行,反应体系的总压强随时间的变化如图所示。由图像不能得出的结论是

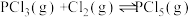 在容积为10L的密闭容器中进行。起始时PCl3和Cl2均为0.2mol,反应在不同条件下进行,反应体系的总压强随时间的变化如图所示。由图像不能得出的结论是
在容积为10L的密闭容器中进行。起始时PCl3和Cl2均为0.2mol,反应在不同条件下进行,反应体系的总压强随时间的变化如图所示。由图像不能得出的结论是
| A.a、b、c三者的反应速率v(PCl5):b>c>a |
| B.反应b可能是加入催化剂 |
| C.该反应是放热反应 |
| D.由a图像得出的平衡常数Kc=10 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】CO2催化加氢是碳中和的重要手段之一,以下是CO2加氢时发生的两个主要反应:
反应Ⅰ:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H1
CH4(g)+2H2O(g) △H1
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) △H2>0
CO(g)+H2O(g) △H2>0
在体积为1L的两个恒容密闭容器中分别按表中所示充入一定量的CO2和H2,平衡体系中δ(CO)和δ(CH4)[ ]随温度变化关系如图所示。
]随温度变化关系如图所示。
反应Ⅰ:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H1
CH4(g)+2H2O(g) △H1反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2>0
CO(g)+H2O(g) △H2>0在体积为1L的两个恒容密闭容器中分别按表中所示充入一定量的CO2和H2,平衡体系中δ(CO)和δ(CH4)[
 ]随温度变化关系如图所示。
]随温度变化关系如图所示。| 容器 | 起始物质的量/mol | |
| CO2 | H2 | |
| 甲 | 0.1 | 0.3 |
| 乙 | 1 | 3 |

| A.△H1<0 |
| B.曲线d表示乙容器中δ(CO)随温度的变化 |
C.590℃时反应10min,某容器中 。反应Ⅱ的v(正)<v(逆) 。反应Ⅱ的v(正)<v(逆) |
| D.M点对应H2的总转化率为66.7% |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下[已知N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1]。下列说法正确的是
2NH3(g) ΔH=-92.4kJ·mol-1]。下列说法正确的是
 2NH3(g) ΔH=-92.4kJ·mol-1]。下列说法正确的是
2NH3(g) ΔH=-92.4kJ·mol-1]。下列说法正确的是| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
| NH3的浓度(mol·L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A.2c1>c3 | B.a=b | C.2p2<p3 | D.α1+α3<1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】利用 和
和 反应生成
反应生成 的过程中主要涉及的反应如下:
的过程中主要涉及的反应如下:
反应Ⅰ 
反应Ⅱ 
向密闭容器中充入一定量 和
和 发生上述反应,保持温度和容器体积一定,平衡时
发生上述反应,保持温度和容器体积一定,平衡时 和
和 的转化率、
的转化率、 和
和 的产率及随起始
的产率及随起始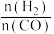 的变化情况如下图所示。
的变化情况如下图所示。
[ 的产率
的产率 的选择性
的选择性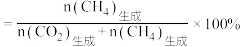 ]。
]。
下列说法
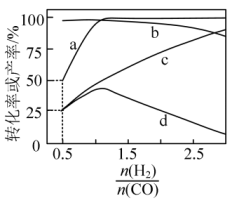
| A.当容器内气体总压强保持不变时,反应Ⅰ、Ⅱ均达到平衡状态 |
B.曲线 表示 表示 的产率随 的产率随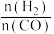 的变化 的变化 |
C.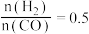 ,反应达平衡时, ,反应达平衡时, 的选择性为 的选择性为 |
D.随着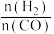 增大, 增大, 的选择性先增大后减小 的选择性先增大后减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:① ;②
;② ,反应①的速率可表示为
,反应①的速率可表示为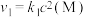 ,反应②的速率可表示为
,反应②的速率可表示为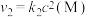 (
( 、
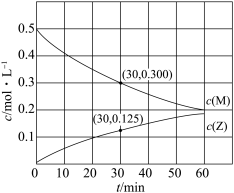
、 为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是
为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是
 ;②
;② ,反应①的速率可表示为
,反应①的速率可表示为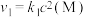 ,反应②的速率可表示为
,反应②的速率可表示为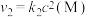 (
( 、
、 为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是
为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是
| A.0~30min内,Y的平均反应速率为2.5×10-3mol·L-1·min-1 |
B.反应开始后,当 保持不变时,说明反应达到平衡状态 保持不变时,说明反应达到平衡状态 |
| C.如果反应能进行到底,反应结束时37.5%的M转化为Y |
| D.反应①的活化能比反应②的活化能大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】将X(g)和Y(g)以1:1体积比通入到2L的恒容密闭容器中进行反应:X(g)+3Y(g) 2Z(g),得到如下三组数据:
2Z(g),得到如下三组数据:
下列说法正确的是( )
 2Z(g),得到如下三组数据:
2Z(g),得到如下三组数据:| 实验组 | 温度/ | 起始X的量/mol | 平衡时Z的量/mol | 达到平衡的时间/min |
| I | 600 | 5.0 | 2.0 | 30 |
| II | 900 | 3.0 | 1.0 | 10 |
| III | 600 | 3.0 | 1.2 | 10 |
A.实验I中,在 内,Y的平均速率为 内,Y的平均速率为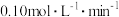 |
| B.当混合气体的密度保持不变时,反应达到平衡状态 |
| C.当 c(X):c(Y)=1:3时,反应达到平衡状态 |
| D.比较实验Ⅱ、Ⅲ,说明Ⅲ可能使用了更高效的催化剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
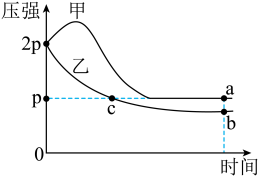
【推荐2】向体积均为1L的两恒容容器中分别充入2molX和1molY发生反应: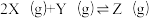
 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
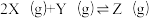
 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
| A.△H>0 | B.气体的总物质的量:na>nc |
| C.a点平衡常数:K<12 | D.反应速率:Va正>Vb正 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在一定温度下,将气体X与气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X( g)+Y( g)⇌2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表:下列说法正确的是( )
| t∕min | 2 | 4 | 7 | 9 |
| n(Y)∕mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A.反应前4min的平均反应速率υ(Z)=0.0125mol•L-1•min-1 |
| B.其他条件不变,降低温度,反应达到新平衡前υ(逆)>υ(正) |
| C.其他条件不变,再向体系中冲入1L氦气,使体系压强增大,则υ(逆)与υ(正)同等程度增大 |
| D.该温度下此反应的平衡常数K=1.44 |
您最近一年使用:0次



