向体积均为1L的两恒容容器中分别充入2molX和1molY发生反应: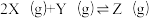
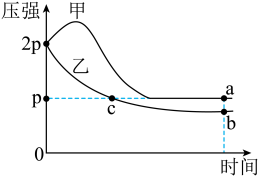
 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
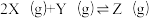
 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
| A.△H>0 | B.气体的总物质的量:na>nc |
| C.a点平衡常数:K<12 | D.反应速率:Va正>Vb正 |
更新时间:2024-03-12 16:04:30
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】我国提出“CO2排放力争于2023年前达到峰值,努力争取2060年前实现碳中和”。研发CO2的利用技术,降低空气中CO2的含量是实现该目标的重要途径。
(1)下面是用H2捕捉CO2时发生的两个反应:
I.CO2(g)+4H2(g) CH4(g)+2H2O(g) ∆H1
CH4(g)+2H2O(g) ∆H1
II.CO2(g)+H2(g) CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2
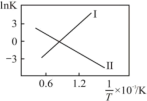
①反应I、II的lnK随1/T的变化如图所示,则ΔH2___________ 0(填“>”“<”或“=”)0;有利于反应I自发进行的温度是___________ (填“高温”或“低温”)。___________ ,而速率仍然增大的可能原因是___________ ___________ ,反应II的平衡常数Kp为___________ (保留两位有效数字)。[已知:CH4的选择性=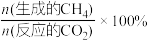 ]
]
(2)利用化学链将高炉废气中的CO2转化为CO的示意图如下。___________ ,该化学链的总反应是___________ 。
(1)下面是用H2捕捉CO2时发生的两个反应:
I.CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ∆H1
CH4(g)+2H2O(g) ∆H1II.CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2①反应I、II的lnK随1/T的变化如图所示,则ΔH2
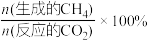 ]
](2)利用化学链将高炉废气中的CO2转化为CO的示意图如下。

您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】以二氧化碳和氢气为原料制取乙醇的反应为:2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1︰3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是( )
CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1︰3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是( )
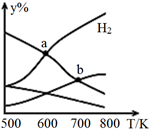
 CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1︰3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是( )
CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1︰3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是( )
| A.a点的平衡常数小于b点 |
| B.b点,υ正(CO2)=υ逆(H2O) |
| C.a点,H2和H2O物质的量相等 |
| D.其他条件恒定,充入更多H2,乙醇的物质的量分数增大 |
您最近一年使用:0次
【推荐1】将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s) ⇌2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列见表,下列说法错误的是
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3 mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A.达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量增大 |
| B.当混合气体平均相对分子质量为26时说明该反应已达平衡 |
| C.根据表中数据,计算25.0 ℃时分解的浓度平衡常数约为1.6×10-8 mol3/L3 |
| D.若保持温度和容器体积不变,平衡后再充入n(NH3)∶n(CO2)=2∶1,则再次达到平衡时c(NH3)不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】中国科学家首次用 改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:
改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:
③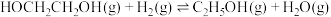
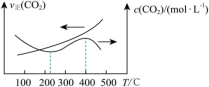
其他条件相同时,相同时间内温度对产物选择性的影响结果如图。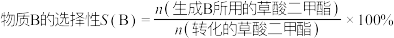
ii.450~500K,反应③的平衡常数远大于反应①和反应②的平衡常数
下列说法不正确 的是
 改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:
改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:①

③
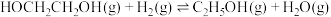
其他条件相同时,相同时间内温度对产物选择性的影响结果如图。

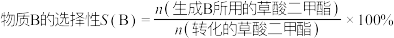
ii.450~500K,反应③的平衡常数远大于反应①和反应②的平衡常数
下列说法
| A.制乙二醇适宜的温度范围是470~480K |
| B.实验条件下反应③的活化的最高,升温更有利于反应③ |
| C.减压可提高乙二醇的平衡产率 |
D.铜基催化剂用 改性后反应速率增大,可以降低反应所需的压强 改性后反应速率增大,可以降低反应所需的压强 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】 时,向容积为2L的恒容密闭容器中充入一定量的CO和
时,向容积为2L的恒容密闭容器中充入一定量的CO和 ,发生如下反应:
,发生如下反应: 。反应过程中测定的部分数据见下表:
。反应过程中测定的部分数据见下表:
下列说法正确的是
 时,向容积为2L的恒容密闭容器中充入一定量的CO和
时,向容积为2L的恒容密闭容器中充入一定量的CO和 ,发生如下反应:
,发生如下反应: 。反应过程中测定的部分数据见下表:
。反应过程中测定的部分数据见下表: 反应时间 | 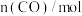 | 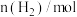 |
| 0 | 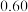 | 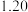 |
| 20 | 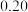 | |
| 30 |  |
A.反应在 内的平均速率为 内的平均速率为 |
B.保持其他条件不变,升高温度,平衡时 ,则反应的 ,则反应的 |
C.保持其他条件不变,再向平衡体系中同时通入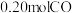 、 、 、 、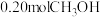 ,达到新平衡前 ,达到新平衡前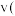 正 正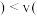 逆 逆 |
D.相同温度下,若起始时向容器中充入 ,达到平衡时 ,达到平衡时 转化率大于 转化率大于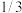 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
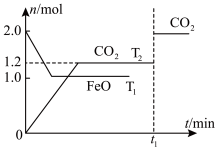
【推荐2】一定条件下,在2L密闭容器中加入等物质的量的FeO和CO,发生下列反应: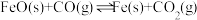 ,在
,在 温度下,物质的量n随时间t变化的曲线如图所示,下列叙述不正确的是
温度下,物质的量n随时间t变化的曲线如图所示,下列叙述不正确的是
 ,在
,在 温度下,物质的量n随时间t变化的曲线如图所示,下列叙述不正确的是
温度下,物质的量n随时间t变化的曲线如图所示,下列叙述不正确的是
| A.平衡前,随着反应的进行,容器内气体的平均相对分子质量逐渐增大 |
B.平衡时,增大压强, 的浓度增大 的浓度增大 |
C.该反应的 , , 、 、 对应的平衡常数 对应的平衡常数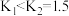 |
| D.t1时刻的改变可能是加入了催化剂,也可能是加入了氮气 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】一定温度下,在3个容积均为1.0 L的恒容密闭容器中发生反应:PCl5 (g)  PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是
 PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是| 容器编号 | 物质的起始浓度/(mol·L-1) | 物质的平衡浓度/(mol·L-1) | ||
 | 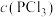 | 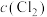 | 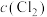 | |
| Ⅰ | 0.4 | 0 | 0 | 0.2 |
| Ⅱ | 0.6 | 0 | 0.2 | |
| Ⅲ | 0.8 | 0 | 0 | |
A.反应达到平衡时,容器I中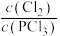 比容器Ⅱ中的小 比容器Ⅱ中的小 |
| B.反应达到平衡时,容器I与容器Ⅱ中的总压强之比为3︰4 |
C.反应达到平衡时,容器Ⅲ中 的体积分数小于 的体积分数小于 |
| D.反应达到平衡时,容器Ⅲ中0.4mol/L<c(PCl5)<0.8 mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】温度为T时,向2.0 L恒容密闭容器中充入2.0 mol X,反应X(g)  Y(g)+Z(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
Y(g)+Z(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
下列说法不正确的是
 Y(g)+Z(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
Y(g)+Z(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:| t/s | 0 | 50 | 150 | 250 | 350 |
| n(Y)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
| A.反应在前250 s的平均速率为v(Y)=0.000 8 mol·L-1·s-1 |
| B.保持其他条件不变,升高温度,平衡时c(Y)=0.21 mol·L-1,则反应的ΔH>0 |
| C.相同温度下,起始时向容器中充入4.0 mol Y、4.0 mol Z,达到平衡时,则此反应的化学平衡常数为1/20 |
| D.相同温度下,若起始时向容器中充入2.0 mol X、0.40 mol Y和0.80 mol Z,则达到平衡前v(正)>v(逆) |
您最近一年使用:0次

 X和2
X和2 ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是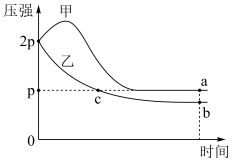


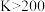
 cC(g) + dD(g) ,达到平衡后,测得C气体的浓度为0.5mol/L。恒温下,将密闭容器的体积缩小为1/2 ,再达平衡时,测得C气体的浓度为0.9mol/L。则下列叙述
cC(g) + dD(g) ,达到平衡后,测得C气体的浓度为0.5mol/L。恒温下,将密闭容器的体积缩小为1/2 ,再达平衡时,测得C气体的浓度为0.9mol/L。则下列叙述 cZ(g)
cZ(g) 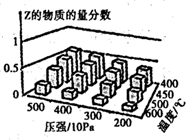
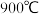 时,向
时,向 恒容密闭容器中充入
恒容密闭容器中充入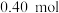 乙苯,发生反应:
乙苯,发生反应: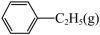

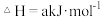 。
。
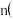 乙苯
乙苯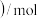


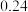




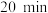 ,
,
 乙苯
乙苯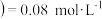 ,则
,则
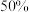
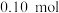 乙苯、
乙苯、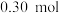 苯乙烯和
苯乙烯和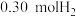 ,达到平衡前
,达到平衡前


