硫脲(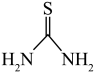 )可用作橡胶的硫化促进剂、金属矿物的浮选剂。测定工业样品中硫脲的质量分数的方法:称取
)可用作橡胶的硫化促进剂、金属矿物的浮选剂。测定工业样品中硫脲的质量分数的方法:称取 g样品,加水溶解配成250mL溶液,取25mL溶液于锥形瓶中,加入稀硫酸酸化,用
g样品,加水溶解配成250mL溶液,取25mL溶液于锥形瓶中,加入稀硫酸酸化,用 酸性
酸性 标准溶液滴定,滴定至终点时消耗标准溶液
标准溶液滴定,滴定至终点时消耗标准溶液 mL[已知滴定时发生反应:
mL[已知滴定时发生反应: ,假设杂质不参与反应]。下列叙述正确的是
,假设杂质不参与反应]。下列叙述正确的是
| A.硫脲中硫元素的化合价为+2 |
| B.滴定时碳、氮元素发生氧化反应 |
C.样品中硫脲的质量分数可表示为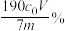 |
| D.若滴定管中滴定前有气泡,滴定后无气泡,会使测定结果偏小 |
更新时间:2024-05-03 13:22:23
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】25℃时,向盛有50mLpH=2的HA溶液的绝热容器中加入pH =13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示。下列叙述正确的是
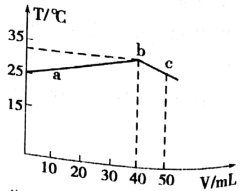

| A.a→b 的过程中,混合溶液中可能存在:c(A-)=c(Na+)=c(H+) =c(OH-) |
| B.HA的物质的量浓度为0.01mol/L |
| C.b点时,溶液中存在:c(Na+)>c(A-)>c(OH-)>c(H+) |
| D.b→c的过程中,温度降低的原因是溶液中发生了吸热反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】 时,等体积两种一元酸
时,等体积两种一元酸 和
和 分别用等浓度的
分别用等浓度的 溶液滴定,滴定曲线如图所示。下列说法正确的是
溶液滴定,滴定曲线如图所示。下列说法正确的是
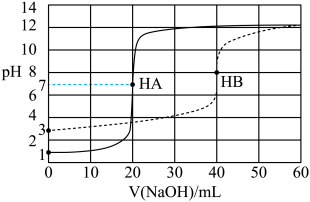
 时,等体积两种一元酸
时,等体积两种一元酸 和
和 分别用等浓度的
分别用等浓度的 溶液滴定,滴定曲线如图所示。下列说法正确的是
溶液滴定,滴定曲线如图所示。下列说法正确的是
A.起始浓度: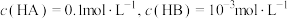 |
| B.酸性:HA>HB |
C.用 溶液滴定 溶液滴定 可用甲基橙作指示剂 可用甲基橙作指示剂 |
D.酸 的电离度 的电离度 约为 约为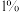 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】向10 mL 0.1mol/L二元弱酸H2A溶液中滴加0.1mol/L NaOH 溶液,溶液中各组分物质的量分数δ(X) [δ(X)=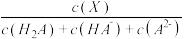 ]随pH的变化如图所示。下列叙述错误的是
]随pH的变化如图所示。下列叙述错误的是
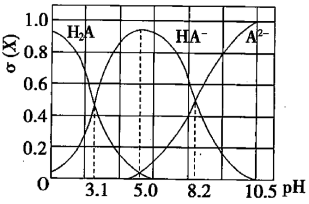
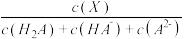 ]随pH的变化如图所示。下列叙述错误的是
]随pH的变化如图所示。下列叙述错误的是
| A.Ka1(H2A) 为10-3.1 |
| B.pH=5.0时,c(Na+)>c(HA-)>c(H+)>c(OH-) >c(A2-) |
| C.pH=8.2时,c (Na+) +c(H+) =c(OH-) +3c(A2-) |
| D.pH 由5.0 调至10.5 时,主要反应的离子方程式为HA-+OH-=A2-+H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确的是
| A.用盐酸标准溶液测定NaOH溶液浓度滴定实验中,滴定前无气泡而滴定后有气泡,会使测定值偏高 |
| B.将地下钢管与直流电源的正极相连,用来保护钢管 |
| C.已知在101KPa下,1gH2燃烧生成水蒸气放出121kJ热量,其热化学方程式为:2H2(g)+O2(g)=2H2O(g) △H=-484 kJ·mol-1 |
| D.25℃,101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ·mol-1,表示稀H2SO4与KOH 溶液反应的中和热的热化学方程式为:H2SO4(aq)+2KOH(aq)=K2SO4(aq)+2H2O(l)△H=-114.6kJ·mol-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】室温下,称取一定质量的邻苯二甲酸氢钾置于锥形瓶中,加入一定体积蒸馏水将其溶解,然后用待测的NaOH溶液进行滴定。已知:室温下,邻苯二甲酸(用H2X表示)在水溶液中含X微粒(H2X、HX−、X2−)的分布分数随pH变化的关系曲线如图所示。
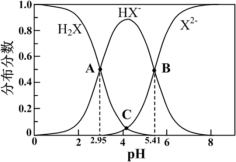
下列有关说法正确的是

下列有关说法正确的是
| A.滴定时,所用的指示剂为甲基橙 |
| B.取NaOH溶液的滴定管洗涤后未进行润洗即用于装液并滴定,则测定的NaOH溶液浓度偏低 |
| C.室温下,0.10 mol•L−1邻苯二甲酸氢钾溶液呈碱性 |
| D.根据图中信息,可计算出C点pH为4.5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】测定水的总硬度一般采用配位滴定法,即在pH=10的氨性溶液中,以铬黑 作为指示剂,用EDTA(乙二胺四乙酸)标准溶液直接滴定水中的Ca2+、Mg2+测定中涉及的反应有:①M2+ (金属离子)+Y4-(EDTA)=MY2-;
作为指示剂,用EDTA(乙二胺四乙酸)标准溶液直接滴定水中的Ca2+、Mg2+测定中涉及的反应有:①M2+ (金属离子)+Y4-(EDTA)=MY2-;
②M2++EBT(铬黑T,蓝色)=MEBT(酒红色);
③MEBT+Y4-(EDTA)=MY2-+EBT。下列说法正确的是
 作为指示剂,用EDTA(乙二胺四乙酸)标准溶液直接滴定水中的Ca2+、Mg2+测定中涉及的反应有:①M2+ (金属离子)+Y4-(EDTA)=MY2-;
作为指示剂,用EDTA(乙二胺四乙酸)标准溶液直接滴定水中的Ca2+、Mg2+测定中涉及的反应有:①M2+ (金属离子)+Y4-(EDTA)=MY2-;②M2++EBT(铬黑T,蓝色)=MEBT(酒红色);
③MEBT+Y4-(EDTA)=MY2-+EBT。下列说法正确的是
| A.配合物MEBT的稳定性大于MY2- |
| B.在滴定过程中眼睛要随时观察滴定管中液面的变化 |
| C.达到滴定终点的现象是溶液恰好由酒红色变为蓝色,且半分钟内不恢复原色 |
| D.实验时装有EDTA标准液的滴定管只用蒸馏水洗涤而未用标准液润洗,测定结果将偏小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】25℃时,体积均为25.00mL,浓度均为0.0100mol•L-1的HA、H3B溶液分别用0.0100mol•L-1NaOH溶液滴定,溶液的pH随V(NaOH)变化曲线如图所示,下列说法正确的是()
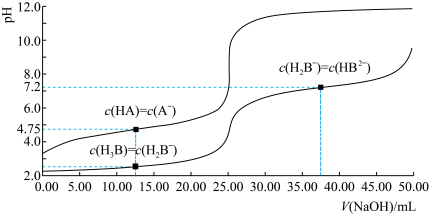

| A.25℃时,0.0100mol•L-1Na2HB溶液的pH>7 |
| B.向HA溶液中滴加NaOH溶液至中性,c(A-)<c(HA) |
| C.NaOH溶液滴定HA溶液应选甲基橙作指示剂 |
| D.25℃时,H2B-离子的水解常数的数量级为10-3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】化学兴趣小组同学进行某补血剂中铁元素含量测定的实验操作如下:
①取10片补血剂样品,研磨,溶解除去不溶物(不损耗铁元素),并配制成100mL待测溶液;
②量取25.00mL待测溶液于锥形瓶中;
③用酸化的c mol/L 溶液滴定至终点,记录消耗
溶液滴定至终点,记录消耗 溶液体积,重复一到两次实验。平均消耗
溶液体积,重复一到两次实验。平均消耗 溶液V mL。下列说法不正确的是
溶液V mL。下列说法不正确的是
①取10片补血剂样品,研磨,溶解除去不溶物(不损耗铁元素),并配制成100mL待测溶液;
②量取25.00mL待测溶液于锥形瓶中;
③用酸化的c mol/L
 溶液滴定至终点,记录消耗
溶液滴定至终点,记录消耗 溶液体积,重复一到两次实验。平均消耗
溶液体积,重复一到两次实验。平均消耗 溶液V mL。下列说法不正确的是
溶液V mL。下列说法不正确的是| A.步骤①研磨是为了溶解时加快溶解速率 |
| B.步骤②待测溶液装入锥形瓶中,不需要加入指示剂 |
C.步骤③c mol/L  溶液应装入酸式滴定管 溶液应装入酸式滴定管 |
| D.每片补血剂中铁元素的质量为1.12cVg |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】某兴趣小组用甲苯与干燥氯气在光照下反应制取一氯化苄,并按以下步骤测定所得粗产品的纯度:
I.称取0.255g粗产品,与25 mL 4.00 mol·L-1氢氧化钠水溶液在100 mL圆底烧瓶中混合,加热回流1小时,发生反应: C6H5CH2Cl+ NaOH=C6H5CH2OH+NaCl。
II.将混合液冷至室温,加入25.00 mL 0.1000 mol·L-1硝酸银水溶液。
Ⅲ.用0.1000 mol·L-1NH4SCN水溶液滴定剩余的硝酸银,以硫酸铁铵为指示剂,消耗了6.75 mL,发生反应: NH4SCN+ AgNO3= AgSCN↓+NH4NO3。
下列说法错误的是
A.步骤II存在错误。
B.达滴定终点时,溶液血红色褪去
C.若试剂和操作无误,则粗产品纯度为90.6%
D. 测定结果会高于样品中一氯化苄的实际含量
I.称取0.255g粗产品,与25 mL 4.00 mol·L-1氢氧化钠水溶液在100 mL圆底烧瓶中混合,加热回流1小时,发生反应: C6H5CH2Cl+ NaOH=C6H5CH2OH+NaCl。
II.将混合液冷至室温,加入25.00 mL 0.1000 mol·L-1硝酸银水溶液。
Ⅲ.用0.1000 mol·L-1NH4SCN水溶液滴定剩余的硝酸银,以硫酸铁铵为指示剂,消耗了6.75 mL,发生反应: NH4SCN+ AgNO3= AgSCN↓+NH4NO3。
下列说法错误的是
A.步骤II存在错误。
B.达滴定终点时,溶液血红色褪去
C.若试剂和操作无误,则粗产品纯度为90.6%
D. 测定结果会高于样品中一氯化苄的实际含量
您最近一年使用:0次



