元素周期律反映了元素性质随原子序数递增的周期性变化规律。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最强的是___________ (填碱的化学式)。
(2)碱金属元素中,137Cs和133Cs之间的关系是互为___________ ,金属钾的氧化物有多种,写出K2O2与CO2反应的化学方程式:___________ 。
(3)可根据元素周期律推测元素的某些性质。如已知卤族元素的性质递变规律,可推知元素砹(At)形成的氢化物HAt的稳定性___________ HI的稳定性(填“大于”或“小于”),AgAt___________ 溶于水(填“易”或“难”)。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最强的是
(2)碱金属元素中,137Cs和133Cs之间的关系是互为
(3)可根据元素周期律推测元素的某些性质。如已知卤族元素的性质递变规律,可推知元素砹(At)形成的氢化物HAt的稳定性
更新时间:2024-05-07 16:25:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。
并检验其纯度的实验流程如图所示。

回答下列问题:
(1)生成 的化学方程式为
的化学方程式为_______ 。钠在空气中燃烧现象为_______ 。
(2)样液中加入 后产生一种无色无味的气体单质,该气体的名称为
后产生一种无色无味的气体单质,该气体的名称为_______ 。
(3)写出 与
与 反应的方程式
反应的方程式_______ 。已知白色沉淀为 ,说明
,说明 样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是
样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是_______ 。
 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。
并检验其纯度的实验流程如图所示。
回答下列问题:
(1)生成
 的化学方程式为
的化学方程式为(2)样液中加入
 后产生一种无色无味的气体单质,该气体的名称为
后产生一种无色无味的气体单质,该气体的名称为(3)写出
 与
与 反应的方程式
反应的方程式 ,说明
,说明 样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是
样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学与生活密切相关。用方程式回答下列问题:
(1)Fe2(SO4)3溶液能导电是因为有自由移动的离子,写出电离方程式_______ 。
(2)氯气可用于饮用水的消毒,其原因是_______ 。
(3)Na2O2常用于解决潜艇的供氧问题。Na2O2降低潜艇内CO2浓度的原因是_______ 。
(4)NaHCO3可用于治疗胃酸(胃酸主要是盐酸)过多,其原因是(用离子方程式)_______ 。
(5)金属钠可用于除去有机溶剂(如苯、醚等)中的少许水分,有关反应的化学方程式是_______ 。
(6)钠很活泼,一定条件下,它能置换出TiCl4中Ti,写出该反应的化学方程式_______ 。
(7)标出下列反应电子转移的方向和数目_______ 。
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
并指出氧化产物与还原产物的物质的量之比是_______ 。
(1)Fe2(SO4)3溶液能导电是因为有自由移动的离子,写出电离方程式
(2)氯气可用于饮用水的消毒,其原因是
(3)Na2O2常用于解决潜艇的供氧问题。Na2O2降低潜艇内CO2浓度的原因是
(4)NaHCO3可用于治疗胃酸(胃酸主要是盐酸)过多,其原因是(用离子方程式)
(5)金属钠可用于除去有机溶剂(如苯、醚等)中的少许水分,有关反应的化学方程式是
(6)钠很活泼,一定条件下,它能置换出TiCl4中Ti,写出该反应的化学方程式
(7)标出下列反应电子转移的方向和数目
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
并指出氧化产物与还原产物的物质的量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有6.0gCO和CO2的混合气体,在标准状况下其体积为4.48L。请回答下列问题:
(1)该混合气体的平均摩尔质量为_________ 。
(2)将混合气体依次通过过量的溶液中,装置如图所示,最后收集在气球中(体积在标准状况下测定)。

①NaOH溶液中发生的离子反应方程式_________ 。
②气球的体积为_________  (忽略气球弹性的影响)。
(忽略气球弹性的影响)。
③若将混合气体通入足量的Na2O2中,转移的电子数为_________ (用NA表示)。
(1)该混合气体的平均摩尔质量为
(2)将混合气体依次通过过量的溶液中,装置如图所示,最后收集在气球中(体积在标准状况下测定)。

①NaOH溶液中发生的离子反应方程式
②气球的体积为
 (忽略气球弹性的影响)。
(忽略气球弹性的影响)。③若将混合气体通入足量的Na2O2中,转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在元素周期表第三周期中,置换酸中氢能力最强的元素的元素符号为_____ ,最高价氧化物对应水化物的酸性最强的化合物的化学式是__________ ,碱性最强的化合物的化学式是__________ ,显两性的氢氧化物的化学式是__________ ,该两性氢氧化物与盐酸、氢氧化钠溶液分别反应的离子方程式为__________________ 、_________________ ,原子半径最大的金属元素的名称是________ ,离子半径最小的离子结构示意图是________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
(1)①的元素符号是__________
(2)②和⑥两种元素的原子半径大小关系:_________ (填“>”或“<”);
(3)③和⑤两种元素的金属性强弱关系:________ (填“>”或“<”);
(4)④的单质与⑥的最高价氧化物对应的水化物的稀溶液反应的离子方程式:__________ 。
| ⅠA | 0 | ||||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | B | ① | ② | Ne | |||||
| 3 | ③ | ④ | ⑤ | Si | ⑥ | ||||
(1)①的元素符号是
(2)②和⑥两种元素的原子半径大小关系:
(3)③和⑤两种元素的金属性强弱关系:
(4)④的单质与⑥的最高价氧化物对应的水化物的稀溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表为元素周期表的一-部分,用化学用语回答下列问题。
(1)⑧的原子结构示意图为______ 。
(2)②③④按原子半径由大到小的顺序排列为_______ (用元素符号表示)。
(3)⑤⑥⑦的最高价氧化物的水化物碱性最强的是_______ (填化学式)。
(4)③的气态氢化物与其最高价氧化物的水化物反应生成的盐属于_____ (填 “共价化合物”或“离子化合物”)。
(5)①④⑩三种元素能形成原子数目比为1 :1:1的共价化合物,它的电子式为_____ 。
(6)欲比较④和⑨两种元素的非金属性强弱,可以作为验证依据的是____ (填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气反应的难易程度
C.比较这两种元素氧化物的水化物的酸性
D.比较这两种元素气态氢化物的稳定性
主族 周期 | I | II | III | IV | V | VI | VII |
一 | ① | ||||||
二 | ② | ③ | ④ | ||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)⑧的原子结构示意图为
(2)②③④按原子半径由大到小的顺序排列为
(3)⑤⑥⑦的最高价氧化物的水化物碱性最强的是
(4)③的气态氢化物与其最高价氧化物的水化物反应生成的盐属于
(5)①④⑩三种元素能形成原子数目比为1 :1:1的共价化合物,它的电子式为
(6)欲比较④和⑨两种元素的非金属性强弱,可以作为验证依据的是
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气反应的难易程度
C.比较这两种元素氧化物的水化物的酸性
D.比较这两种元素气态氢化物的稳定性
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下表是ⅥA族部分元素的相关性质。
请回答下列问题:
(1)硒的熔点范围可能是______________________ 。
(2)碲的化合价可能有______________________ 。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是________ (填化学式)。
(4)氢硒酸有较强的________ (填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生的化学方程式为_______________________________________ 。
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
________ Al2Te3+( ) ===2Al(OH)3↓+________ H2Te↑
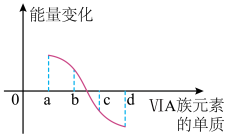
(6)氧族元素单质与H2反应过程中的能量变化如图所示,其中a、b、c、d分别表示氧族中某一元素的单质。则b代表________ ,d代表________ (均写单质名称)。
元素 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1 390 |
| 主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热 化合 | 加热 难化合 | 不能直 接化合 |
请回答下列问题:
(1)硒的熔点范围可能是
(2)碲的化合价可能有
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是
(4)氢硒酸有较强的
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
(6)氧族元素单质与H2反应过程中的能量变化如图所示,其中a、b、c、d分别表示氧族中某一元素的单质。则b代表

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】元素周期表被认为是“科学共同的语言”,它的发现使化学学习和研究变得有规律可循。其简洁有序的背后,是众多科学家艰苦奋斗的结果。下图是元素周期表的一部分。请按要求回答下列问题:

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了元素砷。砷在周期表中的位置是______ 。我国“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。原子半径:Ga______ As(填“>”或“<”)。
(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。碳和硅元素简单气态氢化物稳定性更强的是______ 。碳的最高价氧化物的电子式为______ 。
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硒元素和溴元素最高价氧化物水化物酸性较强的是______ (填化学式)。
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。往 溶液中滴入过量氨水,写出该反应的离子方程式
溶液中滴入过量氨水,写出该反应的离子方程式______ 。
(5)经研究,发现可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期IA族。有关“类钫”的预测正确的是______。

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了元素砷。砷在周期表中的位置是
(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。碳和硅元素简单气态氢化物稳定性更强的是
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硒元素和溴元素最高价氧化物水化物酸性较强的是
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。往
 溶液中滴入过量氨水,写出该反应的离子方程式
溶液中滴入过量氨水,写出该反应的离子方程式(5)经研究,发现可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期IA族。有关“类钫”的预测正确的是______。
| A.“类钫”在化合物中显+1价 | B.“类钫”单质具有强氧化性 |
| C.“类钫”最高价氧化物对应的水化物为弱碱 | D.“类钫”单质能与冷水剧烈反应 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为__________ 。
(2)Na的原子结构示意图为_________ ,Na在氧气中完全燃烧所得产物的电子式为________ 。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点________ (填“高”或“低”)。
②月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为:_________ 。
③MgO与炭粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收, 则生成的盐为__________ (写化学式)。
(4)月壤中含有丰富的3He,月壤中提炼1kg3He,同时可得6000kgH2和700 kg N2,若以所得H2和N2为原料经一系列反应最多可生产碳酸氢铵________ kg。
(1)3He是高效核能原料,其原子核内中子数为
(2)Na的原子结构示意图为
(3)MgCl2在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点
②月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为:
③MgO与炭粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收, 则生成的盐为
(4)月壤中含有丰富的3He,月壤中提炼1kg3He,同时可得6000kgH2和700 kg N2,若以所得H2和N2为原料经一系列反应最多可生产碳酸氢铵
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填空。
(1)写出表示含有8个质子,10个中子的原子的化学符号:_______ 。
(2)根据下列微粒回答问题: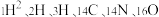 。
。
①以上6种微粒共有_______ 种核素,_______ 种元素。
②互为同位素的是_______ 。
③质量数相等的是_______ ,中子数相等的是_______ 。
(3)相同物质的量的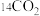 与
与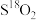 的质量之比为
的质量之比为_______ ;中子数之比为_______ ;电子数之比为_______ 。
(4)质量相同的 和
和 与足量钠反应,放出的气体在标准状况下的体积之比为
与足量钠反应,放出的气体在标准状况下的体积之比为_______ 。
(1)写出表示含有8个质子,10个中子的原子的化学符号:
(2)根据下列微粒回答问题:
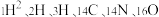 。
。①以上6种微粒共有
②互为同位素的是
③质量数相等的是
(3)相同物质的量的
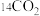 与
与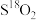 的质量之比为
的质量之比为(4)质量相同的
 和
和 与足量钠反应,放出的气体在标准状况下的体积之比为
与足量钠反应,放出的气体在标准状况下的体积之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将某文献资料上记载的相对原子质量数据摘录如下:
试完成下列问题:
(1)34.969是表示___________ ;
(2)35.453是表示___________ ;
(3)35是表示___________ ;
(4)35.485是表示___________ ;
(5)24.23%是表示___________ ;
(6)列出求算35.453的算式___________ ;
(7)列出求算35.485的算式___________ 。
| 35Cl | 34.969 | 75.77% | 35Cl | 35 | 75.77% |
| 37Cl | 36.966 | 24.23% | 37Cl | 37 | 24.23% |
| 平均 | 35.453 | 平均 | 35.485 | ||
试完成下列问题:
(1)34.969是表示
(2)35.453是表示
(3)35是表示
(4)35.485是表示
(5)24.23%是表示
(6)列出求算35.453的算式
(7)列出求算35.485的算式
您最近一年使用:0次



