氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为原料,经过一系列反应可以得到 和
和 ,流程如图所示。请回答下列问题:
,流程如图所示。请回答下列问题: 分子为
分子为__________ (填“极性”或“非极性”)分子,该分子中F—B—F键角是______ 。
(2) 和过量NaF作用可生成
和过量NaF作用可生成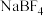 ,
, 的空间结构为
的空间结构为_________ ,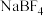 中
中______ (填“含有”或“不含”)配位键。
(3)与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为_________ ,层间作用力为________ 。
 和
和 ,流程如图所示。请回答下列问题:
,流程如图所示。请回答下列问题:
 分子为
分子为(2)
 和过量NaF作用可生成
和过量NaF作用可生成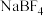 ,
, 的空间结构为
的空间结构为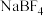 中
中(3)与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为
更新时间:2024-05-09 18:28:13
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)计算下列分子或离子中带“•”原子的价电子对数。
①C Cl4______ ②B eCl2______ ③B Cl3______ ④P Cl3_____ 。
(2)计算下列微粒中带“•”原子的孤电子对数。
①H2S ______ ②P Cl5______ ③B F3______ ④N H3______ 。
(3)用价层电子对互斥模型推测下列分子或离子的立体构型。
①H2Se______ ;②NH
______ ;③BBr3______ ;④CHCl3______ ;⑤SiF4_____ 。
(1)计算下列分子或离子中带“•”原子的价电子对数。
①
(2)计算下列微粒中带“•”原子的孤电子对数。
①H2
(3)用价层电子对互斥模型推测下列分子或离子的立体构型。
①H2Se

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)某元素的基态原子最外层电子排布式为nsnnpn+2,则n=_______ ;基态原子中能量最高的是_______ 电子。
(2)基态铬与氮原子的未成对电子数之比为_______ 。
(3)已知砷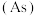 元素原子的最外层电子排布是4s22p3,其最高价氧化物的化学式是
元素原子的最外层电子排布是4s22p3,其最高价氧化物的化学式是_______ ,AsH3的 模型名称
模型名称_______ ,分子的立体构型名称为_______ ,含有的共价键为_______ (填“极性键”或“非极性键”)
(1)某元素的基态原子最外层电子排布式为nsnnpn+2,则n=
(2)基态铬与氮原子的未成对电子数之比为
(3)已知砷
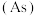 元素原子的最外层电子排布是4s22p3,其最高价氧化物的化学式是
元素原子的最外层电子排布是4s22p3,其最高价氧化物的化学式是 模型名称
模型名称
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)铁在元素周期表中的位置为_____ ,基态铁原子有个未成对电子_____ ,三价铁离子的电子排布式为_____ 。
(2)基态Si原子中,电子占据的最高能层符号_____ ,该能层具有的原子轨道数为_____ ;铝元素的原子核外共有_____ 种不同运动状态的电子、_____ 种不同能级的电子。
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_____ 形象化描述。在基态14C原子中,核外存在_____ 对自旋相反的电子。
(4)中国古代四大发明之一——黑火药,它的爆炸反应为:2KNO3+3C+S K2S+N2↑+3CO2↑,除S外,上述元素的电负性从大到小依次为
K2S+N2↑+3CO2↑,除S外,上述元素的电负性从大到小依次为_____ ,第一电离能从大到小依次为_____ 。
(5)有以下物质:①HF,②Cl2,③H2O,④N2,⑤C2H4,⑥CH4,⑦H2,⑧H2O2,⑨HCN(H—C≡N),⑩Ar,既有σ键又有π键的是______ ;含有由两个原子的s轨道重叠形成的σ键的是______ ;不存在化学键的是______ 。
(6)在BF3分子中,F—B—F的键角是______ ,硼原子的杂化轨道类型为______ ,BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为______ 。
(2)基态Si原子中,电子占据的最高能层符号
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(4)中国古代四大发明之一——黑火药,它的爆炸反应为:2KNO3+3C+S
 K2S+N2↑+3CO2↑,除S外,上述元素的电负性从大到小依次为
K2S+N2↑+3CO2↑,除S外,上述元素的电负性从大到小依次为(5)有以下物质:①HF,②Cl2,③H2O,④N2,⑤C2H4,⑥CH4,⑦H2,⑧H2O2,⑨HCN(H—C≡N),⑩Ar,既有σ键又有π键的是
(6)在BF3分子中,F—B—F的键角是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】四原子分子的空间结构
大多数四原子分子采取_______ 形和_______ 形两种空间结构。
大多数四原子分子采取
| 化学式 | 电子式 | 结构式 | 键角 | 空间结构模型 | 空间结构名称 |
| CH2O | 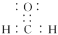 | 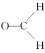 | 约 | 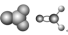 | |
| NH3 | 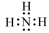 | 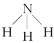 | 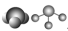 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】完成下列填空
(1)下列常见物质的空间结构呈直线形的是___________ ,呈平面三角形的是___________ 。中心原子轨道采取sp3杂化的是___________ ,采取sp2杂化的是___________ 。
①BF3 ②CO2 ③NH3 ④CCl4 ⑤HC≡CH
(2)NF3是微电子工业中种优良的等离子蚀刻气体,利用杂化轨道理论解释其空间结构是三角锥形:___________ 。
(3)某小组进行如下操作,观察到下列现象:
步骤1:向AgNO3溶液中逐滴滴加氨水,产生白色沉淀;
步骤2:继续滴加,沉淀消失,溶液变澄清。
①澄清溶液中含[Ag(NH3)2]+,其中含有的化学键类型有___________ 。
a.σ键 b.配位键 c.氢键
②已知:Ag++NH3•H2O AgOH↓+NH
AgOH↓+NH ,利用平衡移动原理解释步骤2的现象
,利用平衡移动原理解释步骤2的现象___________ 。
(1)下列常见物质的空间结构呈直线形的是
①BF3 ②CO2 ③NH3 ④CCl4 ⑤HC≡CH
(2)NF3是微电子工业中种优良的等离子蚀刻气体,利用杂化轨道理论解释其空间结构是三角锥形:
(3)某小组进行如下操作,观察到下列现象:
步骤1:向AgNO3溶液中逐滴滴加氨水,产生白色沉淀;
步骤2:继续滴加,沉淀消失,溶液变澄清。
①澄清溶液中含[Ag(NH3)2]+,其中含有的化学键类型有
a.σ键 b.配位键 c.氢键
②已知:Ag++NH3•H2O
 AgOH↓+NH
AgOH↓+NH ,利用平衡移动原理解释步骤2的现象
,利用平衡移动原理解释步骤2的现象
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu2O。
(1) 基态核外电子排布式为
基态核外电子排布式为________ 。
(2) 的空间构型为
的空间构型为________ (用文字描述); 与
与 反应能生成
反应能生成 ,
, 中的配位原子为
中的配位原子为________ (填元素符号)。
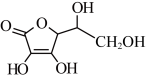
(3)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为________ ;推测抗坏血酸在水中的溶解性:________ (填“难溶于水”或“易溶于水”)。
(1)
 基态核外电子排布式为
基态核外电子排布式为(2)
 的空间构型为
的空间构型为 与
与 反应能生成
反应能生成 ,
, 中的配位原子为
中的配位原子为(3)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
(1)H2O的沸点(100℃)比H2S的沸点(-61℃)高,原因:____ 。
(2)乙炔分子中σ键与π键的个数比为____ 。
(3)乳酸CH3-CH(OH)-COOH____ (填“有”或“无”)手性分子。
(4)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,该元素核外价电子 排布图____ 。
(5)指出配合物K3[Co(CN)6]中的中心离子、配体及其配位数:____ 、____ 、____ 。
(6)SiO2的晶体类型:____ ,在加热融化时克服____ (填作用力名称)。
(1)H2O的沸点(100℃)比H2S的沸点(-61℃)高,原因:
(2)乙炔分子中σ键与π键的个数比为
(3)乳酸CH3-CH(OH)-COOH
(4)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,该元素核外
(5)指出配合物K3[Co(CN)6]中的中心离子、配体及其配位数:
(6)SiO2的晶体类型:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】已知: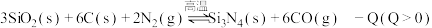 ,在反应条件下,向
,在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:
(1)氮原子的核外电子排布式:_______ ;硅原子核外电子的运动状态有_______ 种。
(2)上述反应混合物中的极性分子是_______ ,写出非极性分子的电子式_______ 。
(3)将 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列_______ 。
(4)氧原子核外电子有_______ 种能量不同的轨道。 属于
属于_______ 晶体。
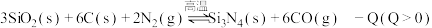 ,在反应条件下,向
,在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:(1)氮原子的核外电子排布式:
(2)上述反应混合物中的极性分子是
(3)将
 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列(4)氧原子核外电子有
 属于
属于
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】将几种物质在水和四氯化碳中的溶解情况填入下表:
其原因是_______ 。
| 葡萄糖 | 磷酸 | 碘 | 苯 | |
| (1)水 | ||||
| (2)四氯化碳 |
其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,表中所列的字母分别代表一种元素。
试回答下列问题(注意:每问中的字母代号为上表中的字母代号,并非为元素符号)
(1)N的单质和水蒸气反应能生成固体X,则I的单质与X反应的化学方程式_______ 。
(2)D的气态氢化物的VSEPR模型的名称为_______ 。
(3)由A、C、D形成的ACD分子中,σ键和π键个数比=_______________ 。
(4)要证明太阳上是否含有R 元素,可采用的方法是__________________________ 。
(5)元素M的化合物(ME2L2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。回答问题:
①ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是_________ (填“极性”或“非极性”)分子。
②将N和O的单质用导线连接后插入D的最高价氧化物对应的水化物浓溶液中,可制成原电池,则组成负极材料的元素的外围电子轨道表示式为______________________ 。
(6)往O2+溶液中加入氨水,形成蓝色沉淀,继续加入氨水,难溶物溶解变成蓝色透明溶液,写出沉淀溶解的离子方程式_____ 。
(7)若F 、K两种元素形成的化合物中中心原子的价电子全部参与成键,则该化合物的空间构型的名称为___ 。
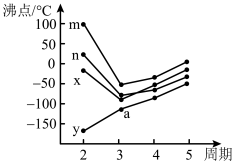
(8)如图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,则E的氢化物所在的折线是__ (填m、n、x或y)。
(9)1183 K以下纯N晶体的基本结构单元如 所示,1183 K以上转变为
所示,1183 K以上转变为 所示结构的基本结构单元。在1183 K以下的晶体中,空间利用率为
所示结构的基本结构单元。在1183 K以下的晶体中,空间利用率为____ ;在1183 K以上的晶体中,与N原子等距离且最近的N原子数为____ ,晶体堆积方式的名称为_____ 。
| A | |||||||||||||||||
| B | C | D | E | F | T | ||||||||||||
| G | H | I | J | K | L | ||||||||||||
| M | N | O | |||||||||||||||
试回答下列问题(注意:每问中的字母代号为上表中的字母代号,并非为元素符号)
(1)N的单质和水蒸气反应能生成固体X,则I的单质与X反应的化学方程式
(2)D的气态氢化物的VSEPR模型的名称为
(3)由A、C、D形成的ACD分子中,σ键和π键个数比=
(4)要证明太阳上是否含有R 元素,可采用的方法是
(5)元素M的化合物(ME2L2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。回答问题:
①ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是
②将N和O的单质用导线连接后插入D的最高价氧化物对应的水化物浓溶液中,可制成原电池,则组成负极材料的元素的外围电子轨道表示式为
(6)往O2+溶液中加入氨水,形成蓝色沉淀,继续加入氨水,难溶物溶解变成蓝色透明溶液,写出沉淀溶解的离子方程式
(7)若F 、K两种元素形成的化合物中中心原子的价电子全部参与成键,则该化合物的空间构型的名称为
(8)如图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,则E的氢化物所在的折线是

(9)1183 K以下纯N晶体的基本结构单元如
 所示,1183 K以上转变为
所示,1183 K以上转变为 所示结构的基本结构单元。在1183 K以下的晶体中,空间利用率为
所示结构的基本结构单元。在1183 K以下的晶体中,空间利用率为
您最近一年使用:0次





 分子中,羰基碳原子与甲基碳原子成键时所采取的杂化方式分别为
分子中,羰基碳原子与甲基碳原子成键时所采取的杂化方式分别为

