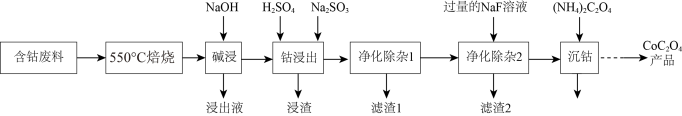
草酸钴是制作氧化钴和金属钴的原料,一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、ZnO、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下:
②ZnO与Al2O3化学性质相似,既能溶于强酸又能溶于强碱
(1)“550℃焙烧”的目的是_______ 。
(2)“浸出液”的主要成分是_______ 。
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为_______ 。
(4)“净化除杂1”过程中,先在40 ~ 50℃加入H2O2,控制温度不能太高的原因是_______ ,H2O2的作用是_______ (用离子方程式表示)。
(5)在空气中焙烧CoC2O4生成Co3O4和一种气体,请写出该反应的化学方程式:_______ 。
②ZnO与Al2O3化学性质相似,既能溶于强酸又能溶于强碱
(1)“550℃焙烧”的目的是
(2)“浸出液”的主要成分是
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为
(4)“净化除杂1”过程中,先在40 ~ 50℃加入H2O2,控制温度不能太高的原因是
(5)在空气中焙烧CoC2O4生成Co3O4和一种气体,请写出该反应的化学方程式:
更新时间:2024-05-09 23:14:33
|
相似题推荐
【推荐1】亚硝酰硫酸(NOSO4H)纯品为棱形结晶,溶于硫酸,遇水易分解,常用于制染料。SO2和浓硝酸在浓硫酸存在时可制备NOSO4H,反应原理为:SO2 + HNO3 = SO3 + HNO2、SO3 + HNO2 = NOSO4H。
(1)亚硝酰硫酸(NOSO4H)的制备。
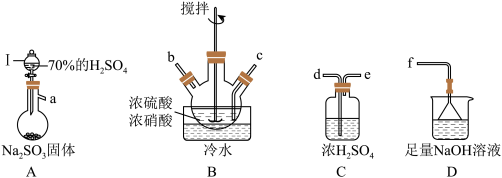
①仪器I的名称为______________ ,打开其旋塞后发现液体不下滴,可能的原因是_________________ 。
②按气流从左到右的顺序,上述仪器的连接顺序为__________________ (填仪器接口字母,部分仪器可重复使用)。
③A中反应的方程式为___________ 。
④B中“冷水”的温度一般控制在20℃,温度不宜过高或过低的原因为________ 。
(2)亚硝酰硫酸(NOSO4H)纯度的测定。
称取1.500 g产品放入250 mL的碘量瓶中,并加入100.00 mL浓度为0.1000 mol·L-1的KMnO4标准溶液和10 mL 25%的H2SO4,摇匀;用0.5000 mol·L-1的Na2C2O4标准溶液滴定,滴定前读数1.02 mL, 到达滴定终点时读数为31.02 mL。
已知:i:□KMnO4 + □NOSO4H + □______ = □K2SO4 + □MnSO4 + □HNO3 + □H2SO4
ii:2KMnO4 + 5Na2C2O4 + 8H2SO4 = 2MnSO4 +10CO2↑+ 8H2O
①完成反应i的化学方程式:_____________
□KMnO4 + □NOSO4H + □______ = □K2SO4 + □MnSO4 + □HNO3 + □H2SO4
②滴定终点的现象为____________________ 。
③产品的纯度为__________________ 。
(1)亚硝酰硫酸(NOSO4H)的制备。

①仪器I的名称为
②按气流从左到右的顺序,上述仪器的连接顺序为
③A中反应的方程式为
④B中“冷水”的温度一般控制在20℃,温度不宜过高或过低的原因为
(2)亚硝酰硫酸(NOSO4H)纯度的测定。
称取1.500 g产品放入250 mL的碘量瓶中,并加入100.00 mL浓度为0.1000 mol·L-1的KMnO4标准溶液和10 mL 25%的H2SO4,摇匀;用0.5000 mol·L-1的Na2C2O4标准溶液滴定,滴定前读数1.02 mL, 到达滴定终点时读数为31.02 mL。
已知:i:□KMnO4 + □NOSO4H + □______ = □K2SO4 + □MnSO4 + □HNO3 + □H2SO4
ii:2KMnO4 + 5Na2C2O4 + 8H2SO4 = 2MnSO4 +10CO2↑+ 8H2O
①完成反应i的化学方程式:
□KMnO4 + □NOSO4H + □______ = □K2SO4 + □MnSO4 + □HNO3 + □H2SO4
②滴定终点的现象为
③产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】ClO2是一种优良的消毒剂,浓度过高时易发生分解,常将其制成NaClO2固体,以便运输和贮存。过氧化氢法制备NaClO2固体的实验装置如图所示。

已知:
2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
2ClO2+H2O2+2NaOH=2NaClO2+O2↑+2H2O
ClO2熔点-59 ℃、沸点11 ℃;H2O2沸点150 ℃
请回答:
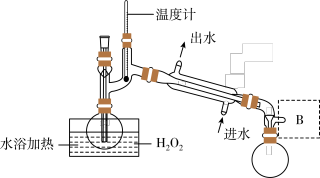
(1)仪器A的作用是_______ ;冰水浴冷却的目的是_______ ,_______ (写两种)。
(2)空气流速过快或过慢,均降低NaClO2产率,试解释其原因_______ 。
(3)Cl-存在时会催化ClO2的生成。反应开始时在三颈烧瓶中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气。该过程可能经两步反应完成,将其补充完整:①_______ (用离子方程式表示),②H2O2+Cl2=2Cl-+O2+2H+。
(4)H2O2浓度对反应速率有影响。通过如图所示装置将少量30% H2O2溶液浓缩至40%,B处应增加一个设备。该设备的作用是_______ ,馏出物是_______ 。

已知:
2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
2ClO2+H2O2+2NaOH=2NaClO2+O2↑+2H2O
ClO2熔点-59 ℃、沸点11 ℃;H2O2沸点150 ℃
请回答:
(1)仪器A的作用是
(2)空气流速过快或过慢,均降低NaClO2产率,试解释其原因
(3)Cl-存在时会催化ClO2的生成。反应开始时在三颈烧瓶中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气。该过程可能经两步反应完成,将其补充完整:①
(4)H2O2浓度对反应速率有影响。通过如图所示装置将少量30% H2O2溶液浓缩至40%,B处应增加一个设备。该设备的作用是

您最近一年使用:0次
【推荐3】钴产品的湿法生产中会生成大量的铜锰渣,主要含有CuO、MnO2,还含有少量的Co2O3、Fe2O3、Al2O3、CaO、MgO等。以铜锰渣为原料制备Cu2(OH)2CO3和MnCO3的工艺流程如下图所示:

已知:相关金属离子形成氢氧化物沉淀的pH范围如下:
(1)“还原浸出”发生的最主要反应的离子方程式为___________
(2)“净化除杂I”需先加入双氧水,再加入氨水调高pH除掉铁、铝杂质,应调节溶液pH范围为___________ 。
(3)“沉铜”操作中,通过加入MnCO3调控溶液酸碱性实现Cu2+与其他金属离子的有效分离,该过程产生气体,写出“沉铜”的离子方程式___________
(4)“净化除杂Ⅱ”除了能深度除钙,还能起到的作用是___________ (用离子方程式表示)。
(5)“沉钴”操作中,加入的(NH4)2S溶液浓度不宜过大,理由是___________ 。
(6)“沉锰”后的母液中存在的主要溶质为___________ (写化学式)。
(7)某种MnOx晶体的晶胞如下图所示,该晶体中Mn元素的化合价为___________ 。已知该晶胞底面是边长为acm的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为(0,0,0)、(m,n, )、(
)、( ,
, ,
, ),则Mn与O形成化学键的键长为
),则Mn与O形成化学键的键长为___________ cm(用含a、m、n的代数式表示)


已知:相关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Cu2+ | Co2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀时pH | 8.1 | 5.2 | 7.1 | 7.5 | 2.2 | 3.7 | 8.9 |
| 完全沉淀时pH | 10.1 | 7.2 | 9.1 | 9.0 | 3.2 | 4.7 | 10.9 |
(2)“净化除杂I”需先加入双氧水,再加入氨水调高pH除掉铁、铝杂质,应调节溶液pH范围为
(3)“沉铜”操作中,通过加入MnCO3调控溶液酸碱性实现Cu2+与其他金属离子的有效分离,该过程产生气体,写出“沉铜”的离子方程式
(4)“净化除杂Ⅱ”除了能深度除钙,还能起到的作用是
(5)“沉钴”操作中,加入的(NH4)2S溶液浓度不宜过大,理由是
(6)“沉锰”后的母液中存在的主要溶质为
(7)某种MnOx晶体的晶胞如下图所示,该晶体中Mn元素的化合价为
 )、(
)、( ,
, ,
, ),则Mn与O形成化学键的键长为
),则Mn与O形成化学键的键长为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】利用氯碱工业的盐泥[含Mg(OH)2及少量的CaCO3、MnCO3、FeCO3、Al(OH)3、SiO2等]生产MgSO4·7H2O的工艺流程如下:

(1)酸浸时,FeCO3与硫酸反应的离子反应方程式为___________________ ;滤渣1的主要成分为CaSO4和____ (填化学式);为了提高浸取率可采取的措施有____ (填字母)。
a. 多次用废硫酸浸取 b. 减小盐泥粒度并充分搅拌
c. 延长浸取时间 d.适当的提高酸浸的温度
(2)氧化时,次氯酸钠溶液将MnSO4氧化为MnO2的离子方程式为__________________ ;滤渣2为MnO2和____ 、____ (填化学式)。
(3) 镁的碳化物常见的有MgC2和Mg2C3两种,分别可发生水解反应生成乙炔和丙二烯,MgC2的电子式为________ 。
(4)一种碱式碳酸镁[4MgCO3·Mg(OH)2·5H2O]可用作防火保温材料,用化学方程式说明可作防火材料的原理:____________________________________ 。

(1)酸浸时,FeCO3与硫酸反应的离子反应方程式为
a. 多次用废硫酸浸取 b. 减小盐泥粒度并充分搅拌
c. 延长浸取时间 d.适当的提高酸浸的温度
(2)氧化时,次氯酸钠溶液将MnSO4氧化为MnO2的离子方程式为
(3) 镁的碳化物常见的有MgC2和Mg2C3两种,分别可发生水解反应生成乙炔和丙二烯,MgC2的电子式为
(4)一种碱式碳酸镁[4MgCO3·Mg(OH)2·5H2O]可用作防火保温材料,用化学方程式说明可作防火材料的原理:
您最近一年使用:0次
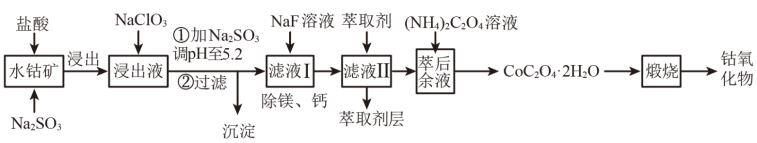
【推荐2】工业上利用钴渣[主要成分为Co2O3、Co(OH)3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制备钴氧化物的工艺流程如下。
已知:部分阳离子以氢氧化物形式沉淀时溶液的 pH 见下表。
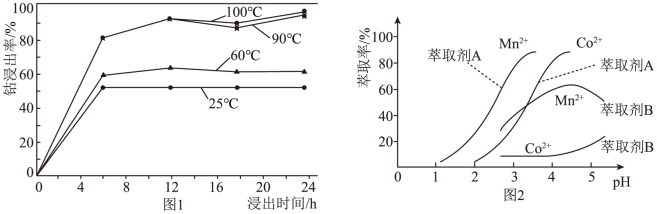
(1)钴的浸出率随酸浸时间、温度的变化关系如图1,应选择的最佳工艺条件为______ 。金属离子在萃取剂中的萃取率随pH变化关系如图2,据此分析pH的最佳范围是______ 。
A.5~5.5 B. 4~4.5 C. 3~3.5 D. 2~2.5
(2)Fe2+、Co2+、 SO 三种离子的还原性由强到弱的顺序是
三种离子的还原性由强到弱的顺序是______ 。氧化过程中加NaClO3被还原,产物中的氯元素处在最低价态,反应的离子方程式为______ 。
(3)25℃ Ksp(MgF2)=7.4×10-11,Ksp(CaF2)=1.5×10-10。除钙、镁工艺中加过量NaF溶液,滤液中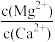 =
=______ (保留两位有效数字)。
(4)已知常温下Kb(NH3·H2O)=1.8×10-5,Kh(C2O )=1.8×10-10,(NH4)2C2O4溶液显
)=1.8×10-10,(NH4)2C2O4溶液显______ (填“酸性” 或“中性”或“碱性”)。在“萃后余液”中加入(NH4)2C2O4溶液后析出晶体,再过滤、洗涤,洗涤时应选用的试剂为______ (填字母代号)。
A.蒸馏水 B.自来水 C.饱和的(NH4)2C2O4溶液 D.稀盐酸
(5)取一定质量煅烧后产生的钴氧化物(Co为+2、+3价),用100 mL 8 mol·L-1的盐酸恰好完全溶解,得到CoCl2溶液和标准状况2.24 L黄绿色气体。则该钴氧化物中+2价的Co与+3价Co元素的物质的量之比为______ 。

已知:部分阳离子以氢氧化物形式沉淀时溶液的 pH 见下表。
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)钴的浸出率随酸浸时间、温度的变化关系如图1,应选择的最佳工艺条件为
A.5~5.5 B. 4~4.5 C. 3~3.5 D. 2~2.5

(2)Fe2+、Co2+、 SO
 三种离子的还原性由强到弱的顺序是
三种离子的还原性由强到弱的顺序是(3)25℃ Ksp(MgF2)=7.4×10-11,Ksp(CaF2)=1.5×10-10。除钙、镁工艺中加过量NaF溶液,滤液中
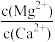 =
=(4)已知常温下Kb(NH3·H2O)=1.8×10-5,Kh(C2O
 )=1.8×10-10,(NH4)2C2O4溶液显
)=1.8×10-10,(NH4)2C2O4溶液显A.蒸馏水 B.自来水 C.饱和的(NH4)2C2O4溶液 D.稀盐酸
(5)取一定质量煅烧后产生的钴氧化物(Co为+2、+3价),用100 mL 8 mol·L-1的盐酸恰好完全溶解,得到CoCl2溶液和标准状况2.24 L黄绿色气体。则该钴氧化物中+2价的Co与+3价Co元素的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】 气体是一种优良的消毒剂,常用于自来水的消毒。工业上常将
气体是一种优良的消毒剂,常用于自来水的消毒。工业上常将 制备成
制备成 固体以便运输和贮存,具体流程如下:
固体以便运输和贮存,具体流程如下:

(1)反应器中, 的作用是
的作用是___________ 。(填“氧化剂”或“还原剂”)。
(2)吸收器中发生的反应有 产生,该反应的化学方程式是
产生,该反应的化学方程式是___________ 。
(3)已知: 饱和溶液在低于38℃时析出
饱和溶液在低于38℃时析出 ,高于38℃时析出
,高于38℃时析出 。请补充从
。请补充从 溶液中制得
溶液中制得 晶体的实验操作步骤:①
晶体的实验操作步骤:①___________ ;②___________ ;③用无水乙醇洗涤;④干燥得到 固体。
固体。
(4)为了测定获得产品中 的纯度,进行如下实验:
的纯度,进行如下实验:
步骤1:准确称取2.000g上述产品,溶于水配成250mL的溶液。
步骤2:取25.00mL待测液,加入过量的KI溶液和 溶液发生如下反应:
溶液发生如下反应:
 ,杂质不与KI反应。
,杂质不与KI反应。
步骤3:以淀粉溶液作指示剂,再加入 溶液,恰好完全反应时消耗
溶液,恰好完全反应时消耗 溶液的体积为40.00mL。(已知:
溶液的体积为40.00mL。(已知: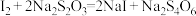 )。
)。
①步骤1配制溶液过程中,“转移”时忘记洗涤烧杯,最终所测样品纯度将___________ 。(填“偏高”“偏低”或“不变”)
②计算该样品中 的纯度
的纯度___________ 。(写出计算过程)。
 气体是一种优良的消毒剂,常用于自来水的消毒。工业上常将
气体是一种优良的消毒剂,常用于自来水的消毒。工业上常将 制备成
制备成 固体以便运输和贮存,具体流程如下:
固体以便运输和贮存,具体流程如下:
(1)反应器中,
 的作用是
的作用是(2)吸收器中发生的反应有
 产生,该反应的化学方程式是
产生,该反应的化学方程式是(3)已知:
 饱和溶液在低于38℃时析出
饱和溶液在低于38℃时析出 ,高于38℃时析出
,高于38℃时析出 。请补充从
。请补充从 溶液中制得
溶液中制得 晶体的实验操作步骤:①
晶体的实验操作步骤:① 固体。
固体。(4)为了测定获得产品中
 的纯度,进行如下实验:
的纯度,进行如下实验:步骤1:准确称取2.000g上述产品,溶于水配成250mL的溶液。
步骤2:取25.00mL待测液,加入过量的KI溶液和
 溶液发生如下反应:
溶液发生如下反应:
 ,杂质不与KI反应。
,杂质不与KI反应。步骤3:以淀粉溶液作指示剂,再加入
 溶液,恰好完全反应时消耗
溶液,恰好完全反应时消耗 溶液的体积为40.00mL。(已知:
溶液的体积为40.00mL。(已知: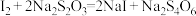 )。
)。①步骤1配制溶液过程中,“转移”时忘记洗涤烧杯,最终所测样品纯度将
②计算该样品中
 的纯度
的纯度
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钒酸钇(YVO4)广泛应用于光纤通信领域,一种用废钒催化剂(含 V2O5、K2O、SiO2少量Fe2O3制取YVO4的工艺流程如下:
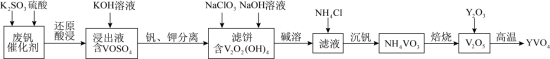
已知:V2O2(OH)4既能与强酸反应,又能与强碱反应。 回答下列问题:
(1)“还原酸浸”时,钒以VO2+浸出,“浸出液”中还含有的金属离子是___________ 。V2O5被还原的离子方程式为___________ 。
(2)结合“碱溶”和“沉钒”可知,ClO 、VO
、VO 氧化性更强的是
氧化性更强的是___________ ,“沉钒”时发生反应的化学方程式为___________ 。
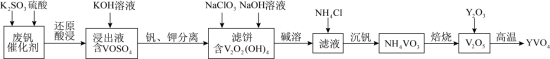
已知:V2O2(OH)4既能与强酸反应,又能与强碱反应。 回答下列问题:
(1)“还原酸浸”时,钒以VO2+浸出,“浸出液”中还含有的金属离子是
(2)结合“碱溶”和“沉钒”可知,ClO
 、VO
、VO 氧化性更强的是
氧化性更强的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】从处理后的矿石硝酸浸取液(含Ni2+、Co2+、Al3+、Mg2+)中,利用氨浸工艺可提取Ni、Co,并获得高附加值化工产品.工艺流程如下:
(1)Co位于元素周期表中的位置______________ (周期、族);
(2)“氨浸”时,由Co(OH)3转化为[Co(NH3)6]2+的离子方程式为______________________ ;
(3)(NH4)2CO3会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物.滤渣的X射线衍射图谱中,出现了NH4Al(OH)2CO3的明锐衍射峰;
①NH4Al(OH)2CO3属于______________ (填“晶体”或“非晶体”);
②(NH4)2CO3提高了Ni、Co的浸取速率,其原因是______________________ ;
(4)“析晶”过程中通入的酸性气体A为______________ .
(5)①“结晶纯化”过程中,没有引入新物质,晶体A含6个结晶水,则所得HNO3溶液中n(HNO3)与n(H2O)的比值,理论上最高为______________ ;
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用HNO3和___________ (填化学式)。
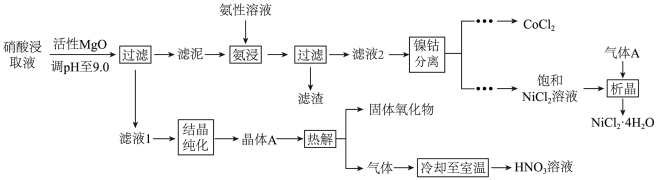
(1)Co位于元素周期表中的位置
(2)“氨浸”时,由Co(OH)3转化为[Co(NH3)6]2+的离子方程式为
(3)(NH4)2CO3会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物.滤渣的X射线衍射图谱中,出现了NH4Al(OH)2CO3的明锐衍射峰;
①NH4Al(OH)2CO3属于
②(NH4)2CO3提高了Ni、Co的浸取速率,其原因是
(4)“析晶”过程中通入的酸性气体A为
(5)①“结晶纯化”过程中,没有引入新物质,晶体A含6个结晶水,则所得HNO3溶液中n(HNO3)与n(H2O)的比值,理论上最高为
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用HNO3和
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】化学小组实验探究SO2与AgNO3溶液的反应。
(1)实验一:用如下装置(夹持、加热仪器略)制备SO2,将足量SO2通入AgNO3溶液中,迅速反应,得到无色溶液A和白色沉淀B。
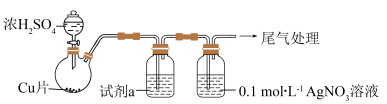
尾气吸收所用试剂是_______ 。
(2)对体系中有关物质性质分析得出:沉淀B可能为Ag2SO3、Ag2SO4或二者混合物。(资料:Ag2SO4微溶于水;Ag2SO3难溶于水)
实验二:验证B的成分

①写出Ag2SO3溶于氨水的离子方程式:_______ 。
②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F。推断D中主要是BaSO3,进而推断B中含有Ag2SO3。向滤液E中加入一种试剂,可进一步证实B中含有Ag2SO3。所用试剂及现象是_______ 。
(3)根据沉淀F的存在,推测 的产生有两个途径:
的产生有两个途径:
途径1:实验一中,SO2在AgNO3溶液中被氧化生成Ag2SO4,随沉淀B进入D。
途径2:实验二中, 被氧化为
被氧化为 进入D。
进入D。
实验三:探究 的产生途径
的产生途径
①向溶液A中滴入过量盐酸,产生白色沉淀,取上层清液继续滴加BaCl2溶液,未出现白色沉淀,可判断B中不含Ag2SO4.做出判断的理由:_______ 。
②实验三的结论:_______ 。
(4)实验一中,SO2与AgNO3溶液反应的离子方程式是_______ 。
(1)实验一:用如下装置(夹持、加热仪器略)制备SO2,将足量SO2通入AgNO3溶液中,迅速反应,得到无色溶液A和白色沉淀B。

尾气吸收所用试剂是
(2)对体系中有关物质性质分析得出:沉淀B可能为Ag2SO3、Ag2SO4或二者混合物。(资料:Ag2SO4微溶于水;Ag2SO3难溶于水)
实验二:验证B的成分

①写出Ag2SO3溶于氨水的离子方程式:
②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F。推断D中主要是BaSO3,进而推断B中含有Ag2SO3。向滤液E中加入一种试剂,可进一步证实B中含有Ag2SO3。所用试剂及现象是
(3)根据沉淀F的存在,推测
 的产生有两个途径:
的产生有两个途径:途径1:实验一中,SO2在AgNO3溶液中被氧化生成Ag2SO4,随沉淀B进入D。
途径2:实验二中,
 被氧化为
被氧化为 进入D。
进入D。实验三:探究
 的产生途径
的产生途径①向溶液A中滴入过量盐酸,产生白色沉淀,取上层清液继续滴加BaCl2溶液,未出现白色沉淀,可判断B中不含Ag2SO4.做出判断的理由:
②实验三的结论:
(4)实验一中,SO2与AgNO3溶液反应的离子方程式是
您最近一年使用:0次



