“宏观辨识与微观探析”是学科核心素养之一,下列离子方程式正确且符合题意的是
A.“84消毒液”具有漂白作用: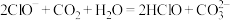 |
B.用铜片作电极,电解饱和食盐水: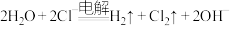 |
C.赤血盐溶液滴入FeSO4溶液中: |
D.向过量的NaHSO3溶液中滴加少量溴水: |
更新时间:2024-05-10 17:42:13
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列反应的离子方程式书写正确的是
| A.硫酸铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| B.氢氧化铁溶于氢碘酸溶液:Fe(OH)3+3H+=Fe3++3H2O |
| C.向氯化铁溶液中加入过量的硫化钠:2Fe3++S2-=2Fe2++S↓ |
| D.向石灰乳中加入氯化铁溶液:3Ca(OH)2+2Fe3+=2Fe(OH)3+3Ca2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式书写正确的是
| A.铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑ |
| B.三氯化铁刻蚀印刷电路板: Cu + Fe3+ ══ Fe2+ + Cu2+ |
| C.用小苏打治疗胃酸过多: H+ +HCO3-══ H2O + CO2↑ |
| D.氢氧化亚铁在空气中最后变为红褐色:4 Fe(OH)2+O2+2H2O══ 4Fe3++12OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列离子方程式书写正确的是
A.铁与稀硫酸反应: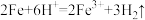 |
B.氯化铁溶液与氨水反应: |
C.足量 溶液与少量石灰水反应: 溶液与少量石灰水反应: |
D.氢氧化亚铁与稀硝酸反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验现象与对应结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下将Cu片放入浓H2SO4中 | 生成刺激性气味气体 | Cu与浓H2SO4反应生成SO2 |
| B | Al2(SO4)3溶液中滴加过量氨水 | 生成白色胶状物质 | Al(OH)3不溶于氨水 |
| C | 氯气通入湿润的红色布条 | 红色布条褪色 | 氯气具有漂白性 |
| D | 向某溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 该溶液中存在I﹣ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图所示,A处通入 ,关闭B阀时,C处干燥的红布看不到明显现象,当打开B阀后,C处干燥的红布条逐渐褪色,则下列说法错误的是
,关闭B阀时,C处干燥的红布看不到明显现象,当打开B阀后,C处干燥的红布条逐渐褪色,则下列说法错误的是

 ,关闭B阀时,C处干燥的红布看不到明显现象,当打开B阀后,C处干燥的红布条逐渐褪色,则下列说法错误的是
,关闭B阀时,C处干燥的红布看不到明显现象,当打开B阀后,C处干燥的红布条逐渐褪色,则下列说法错误的是
| A.通入的氯气是湿润的 |
| B.D瓶中的液体可以是饱和NaCl溶液 |
C.D瓶中的液体可以是浓硫酸、也可以是 溶液、NaOH溶液 溶液、NaOH溶液 |
| D.红布条褪色是因为有次氯酸生成,其源白原理与过氧化钠相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列设计的实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 证明“84”消毒液的氧化能力随溶液pH的减小而增强 | 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快褪为无色 |
| B | 证明反应速率会随反应物浓度的增大而加快 | 用3 mL稀硫酸与足量纯锌反应,产生气泡速率较慢,然后加入1mL 1mol•L-1CuSO4溶液,迅速产生较多气泡 |
| C | 证明碳和浓硫酸共热生成的气体中含有二氧化碳 | 将生成的气体直接通入澄清石灰水,有白色沉淀生成 |
| D | 证明氯化银的溶解度大于硫化银的溶解度 | 向2 mL 0.1 mol•L-1硝酸银溶液中加入1mL 0.1mol•L-1 NaCl溶液,出现白色沉淀,再加入几滴0.1 mol•L-1的Na2S溶液,有黑色沉淀生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
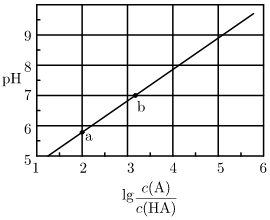
【推荐1】常温下,用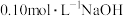 溶液滴定
溶液滴定 溶液,混合溶液的pH与离子浓度变化的关系如图所示,下列叙述错误的是
溶液,混合溶液的pH与离子浓度变化的关系如图所示,下列叙述错误的是
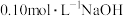 溶液滴定
溶液滴定 溶液,混合溶液的pH与离子浓度变化的关系如图所示,下列叙述错误的是
溶液,混合溶液的pH与离子浓度变化的关系如图所示,下列叙述错误的是
A. 的数量级为 的数量级为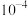 |
| B.b点时消耗NaOH溶液的体积小于20mL |
C.b点溶液中离子浓度: |
D.混合溶液的导电能力: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,将pH=a的NaOH溶液与pH=b的醋酸溶液等体积混合后,两者恰好完全反应,则该温度下醋酸的电离平衡常数约为
| A.1014-a-2b | B.10 a+b-14 | C.10a-2b | D.10a-2b+14 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】电-Fenton法是用于水体中有机污染物降解的高级氧化技术,反应原理如图所示。电解产生的H2O2与Fe2+发生反应生成的羟基自由基(·OH)能氧化降解有机污染物。下列说法错误的是


| A.电源的A极为负极 |
| B.与电源B极相连电极的电极反应式为H2O-e- =H++·OH |
| C.Fenton反应为:H2O2+Fe2+=Fe(OH)2++·OH |
| D.每消耗2.24LO2(标准状况),整个电解池中理论上可产生的·OH为0.2mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在电解液不参与反应的情况下,采用电化学法还原CO2可制备ZnC2O4,原理如图所示。下列说法正确的是


| A.电解结束后电解液Ⅱ中c(Zn2+)增大 |
| B.电解液Ⅰ应为ZnSO4溶液 |
C.Pt极反应式为2CO2+2e−= |
| D.当通入44 g CO2时,溶液中转移1 mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】液体锌电池是一种电压较高的二次电池,具有成本低、安全性强、可循环使用等特点,其示意图如图。下列说法不正确 的是

已知:①Zn(OH)2+2OH-=Zn(OH) 。
。
②KOH凝胶中允许离子存在、生成或迁移。

已知:①Zn(OH)2+2OH-=Zn(OH)
 。
。②KOH凝胶中允许离子存在、生成或迁移。
| A.放电过程中,H+由负极向正极迁移 |
| B.放电过程中,负极的电极反应:MnO2+4H++2e-=Mn2++2H2O |
C.充电过程中,阴极的电极反应:Zn(OH) +2e-=Zn+4OH- +2e-=Zn+4OH- |
| D.充电过程中,凝胶中的KOH可再生 |
您最近一年使用:0次



