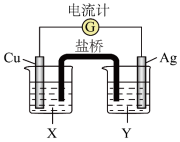
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:___________ 。若初始时两电极质量相等,当电路中有2mole﹣通过时,两极的质量差为___________ g。
(2)当电极a为Al,电极b为Mg,电解质溶液为NaOH溶液时,该电池的负极反应式为___________ ,当反应中收集到标准状况下336mL气体时,消耗负极的物质的量为___________ mol。
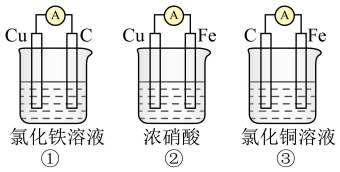
(3)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是___________ ,写出正极的电极反应式___________ 。___________ (填“正”或“负”)极。
②该电池负极的电极反应式为___________ 。
③工作一段时间后,当3.2g甲醇完全反应生成CO2时,外电路中通过的电子数目为___________ 。(用含NA的式子表示)
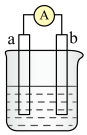
(2)当电极a为Al,电极b为Mg,电解质溶液为NaOH溶液时,该电池的负极反应式为
(3)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是
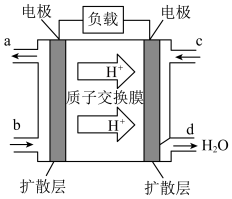
②该电池负极的电极反应式为
③工作一段时间后,当3.2g甲醇完全反应生成CO2时,外电路中通过的电子数目为
更新时间:2024-05-10 18:58:55
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】电化学装置可实现化学能与电能的直接转化,是助力实现“30、60”双碳目标的一种重要路径。
(1)图1所示的盐桥电池工作时,Zn为___________ 极(填“正”或“负”),Cu电极的电极反应式为___________ ,盐桥中的 移向
移向___________ 池(填“左”或“右”)。___________ 。
②乙池工作时,电子由___________ (填“c”或“d”)极流出,电解总化学方程式为___________ ,d电极附近观察到的现象是___________ ,阳离子交换膜的作用是___________ 。
(1)图1所示的盐桥电池工作时,Zn为
 移向
移向
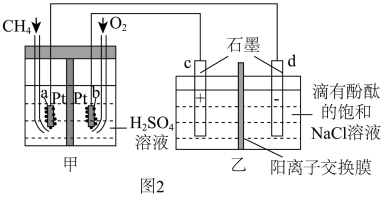
②乙池工作时,电子由
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有A、B、C、D四种金属片:
①把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生;
②把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应;
③把A、C用导线连接后同时浸入稀H2SO4溶液中,电子流动方向为A→导线→C。
根据上述情况,回答下列问题:
(1)在①中,金属片___________ 发生氧化反应,金属片___________ 作正极;
(2)在②中,金属片___________ 作负极;___________ 金属更活泼。
(3)如果把B、D用导线连接后同时浸入稀H2SO4溶液,则金属片___________ 上有气泡产生;
(4)上述四种金属的活动性由强到弱的顺序是___________ 。
①把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生;
②把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应;
③把A、C用导线连接后同时浸入稀H2SO4溶液中,电子流动方向为A→导线→C。
根据上述情况,回答下列问题:
(1)在①中,金属片
(2)在②中,金属片
(3)如果把B、D用导线连接后同时浸入稀H2SO4溶液,则金属片
(4)上述四种金属的活动性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)甲醇是一种可再生能源,由 制备甲醇可能涉及的反应如下:
制备甲醇可能涉及的反应如下:
反应Ⅰ: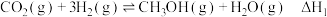
反应Ⅱ: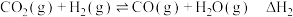
反应Ⅲ: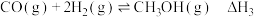
反应Ⅰ、Ⅱ、Ⅲ平衡常数分别为 ,则
,则
___________ (用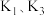 表示)。
表示)。
(2)某探究小组用 与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用 浓度为
浓度为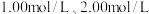 ,大理石有细颗粒和粗颗粒两种规格,实验温度为
,大理石有细颗粒和粗颗粒两种规格,实验温度为 、
、 ,每次实验
,每次实验 的用量为
的用量为 ,大理石用量为
,大理石用量为 。
。
请完成实验设计表,其中a为___________ ,e为___________ 。
(3)①氯气是制备系列含氯化合物的主要原料,可采用如图A所示的装置来制取氯气。装置中的离子膜只允许___________ (填“ ”或“
”或“ ”)通过,氯气的逸出口是
”)通过,氯气的逸出口是___________ (填标号“ ”或“b”)。
”或“b”)。

② 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为___________ 。

(1)甲醇是一种可再生能源,由
 制备甲醇可能涉及的反应如下:
制备甲醇可能涉及的反应如下:反应Ⅰ:
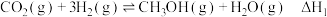
反应Ⅱ:
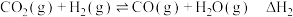
反应Ⅲ:
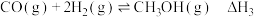
反应Ⅰ、Ⅱ、Ⅲ平衡常数分别为
 ,则
,则
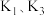 表示)。
表示)。(2)某探究小组用
 与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用 浓度为
浓度为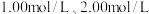 ,大理石有细颗粒和粗颗粒两种规格,实验温度为
,大理石有细颗粒和粗颗粒两种规格,实验温度为 、
、 ,每次实验
,每次实验 的用量为
的用量为 ,大理石用量为
,大理石用量为 。
。| 实验编号 | 温度( ) ) | 大理石规格 |  (浓度) (浓度)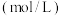 | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究浓度对反应速率的影响; (Ⅱ)实验①和③探究温度对反应速率的影响; (Ⅲ)实验①和④探究e___________对反应速率的影响 |
| ② | 25 | 粗颗粒 | a___________ | |
| ③ | b___________ | 粗颗粒 | 2.00 | |
| ④ | c___________ | 细颗粒 | d___________ |
(3)①氯气是制备系列含氯化合物的主要原料,可采用如图A所示的装置来制取氯气。装置中的离子膜只允许
 ”或“
”或“ ”)通过,氯气的逸出口是
”)通过,氯气的逸出口是 ”或“b”)。
”或“b”)。
②
 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。请根据题中提供的信息,回答下列问题:
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_____。
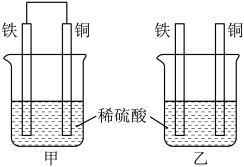
(2)将纯铁片和纯铜片按图甲、乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:_____ 。
A.甲中铜片质量减少、乙中铁片质量减少 B.甲、乙均为化学能转变为电能的装置
C.乙中铜片上没有明显变化 D.甲、乙两烧杯中 均减小
均减小
②在相同时间内,两烧杯中产生气泡的速度:甲_____ 乙(填“>”、“<”或“=”)。
③请写出甲、乙中构成原电池的正极电极反应式:_____ 。电池工作时,溶液中 向
向_____ 极(填“正”或“负”)移动。当甲中溶液质量增重27g时,电极上转移电子数目为_____ 。
④若将甲中的稀硫酸换为浓硝酸,则电池总反应的离子方程式为_____ 。
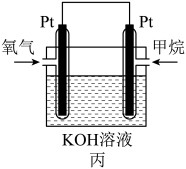
(3)图丙为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH.通甲烷一极是电池的____ 极,电极反应为______ 。
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_____。
A. 与 与 反应 反应 | B. 与 与 燃烧反应 燃烧反应 |
C.灼热的炭与 反应 反应 | D.氢氧化钠与稀盐酸反应 |
(2)将纯铁片和纯铜片按图甲、乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
A.甲中铜片质量减少、乙中铁片质量减少 B.甲、乙均为化学能转变为电能的装置
C.乙中铜片上没有明显变化 D.甲、乙两烧杯中
 均减小
均减小②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出甲、乙中构成原电池的正极电极反应式:
 向
向④若将甲中的稀硫酸换为浓硝酸,则电池总反应的离子方程式为
(3)图丙为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH.通甲烷一极是电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】酸雨的危害很大,能直接破坏农作物、腐蚀建筑物,还会危害人体健康。 、
、 是形成酸雨的主要物质。研究
是形成酸雨的主要物质。研究 、
、 等对减少酸雨,改善空气质量具有重要意义。请回答下列问题:
等对减少酸雨,改善空气质量具有重要意义。请回答下列问题:
(1)酸雨是指 小于
小于_______ 的雨水。
(2)你认为减少酸雨的产生可采取的措施有_______ (填序号)。
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰
(3)开发新能源可有效减少酸雨。下列能源不属于新能源的有_______ (填序号)。
①太阳能 ②风能 ③地热能 ④海洋能 ⑤氢能 ⑥石油 ⑦无烟煤
(4) 主要来源于汽车尾气。通过
主要来源于汽车尾气。通过 传感器可监测汽车尾气中
传感器可监测汽车尾气中 含量,其工作原理如图。据此回答:
含量,其工作原理如图。据此回答:
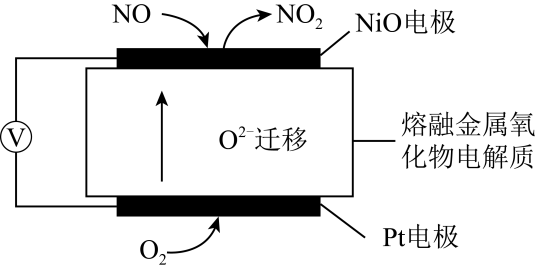
 电极为
电极为_______ (填“正极”或“负极”);其电极反应式为_______ 。
(5)可用氨水将 转化为
转化为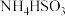 ,再用
,再用 氧化成NH4HSO4来脱除烟气中的
氧化成NH4HSO4来脱除烟气中的 ,原理是
,原理是_______ 、_______ (用离子方程式表示)。
 、
、 是形成酸雨的主要物质。研究
是形成酸雨的主要物质。研究 、
、 等对减少酸雨,改善空气质量具有重要意义。请回答下列问题:
等对减少酸雨,改善空气质量具有重要意义。请回答下列问题:(1)酸雨是指
 小于
小于(2)你认为减少酸雨的产生可采取的措施有
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰
(3)开发新能源可有效减少酸雨。下列能源不属于新能源的有
①太阳能 ②风能 ③地热能 ④海洋能 ⑤氢能 ⑥石油 ⑦无烟煤
(4)
 主要来源于汽车尾气。通过
主要来源于汽车尾气。通过 传感器可监测汽车尾气中
传感器可监测汽车尾气中 含量,其工作原理如图。据此回答:
含量,其工作原理如图。据此回答:
 电极为
电极为(5)可用氨水将
 转化为
转化为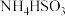 ,再用
,再用 氧化成NH4HSO4来脱除烟气中的
氧化成NH4HSO4来脱除烟气中的 ,原理是
,原理是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应与能量,是学习和研究化学原理的重要内容。
(1)铁、铜、铝是生活中使用广泛的金属,氯化铁溶液常用于腐蚀印刷电路铜板,若将此反应设计成原电池,则负极所用电极材料为___________ ,正极反应式为___________ 。
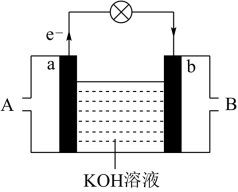
(2)将氢气与氧气的反应设计成燃料电池,其能量利用率更高,装置如图所示(a、b为多孔炭棒),其中___________ (填A或B)处电极入口通氢气,其电极反应式为___________ 。工作一段时间后正极区溶液的pH值___________ (填变大、减小或不变)。当消耗标况下氢气33.6L时,假设能量转化率为90%,则导线中转移电子的物质的量为___________ mol。
(1)铁、铜、铝是生活中使用广泛的金属,氯化铁溶液常用于腐蚀印刷电路铜板,若将此反应设计成原电池,则负极所用电极材料为
(2)将氢气与氧气的反应设计成燃料电池,其能量利用率更高,装置如图所示(a、b为多孔炭棒),其中

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为__________ 、_______ 。
(2)用甲烷制取氢气的两步反应的能量变化如下图所示:
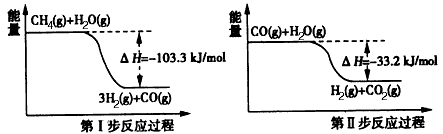
甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是________________ 。
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159.5KJ/mol
②NH2CO2NH4(s)= CO(NH2)2(s) +H2O(g) △H=+116.5KJ/mol
③H2O(l)=H2O(g) △H=+44KJ/mol
写出CO2与NH3合成尿素和液态水的热化学方程式__________________ 。
(4)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为_________________ 。
(2)用甲烷制取氢气的两步反应的能量变化如下图所示:

甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159.5KJ/mol
②NH2CO2NH4(s)= CO(NH2)2(s) +H2O(g) △H=+116.5KJ/mol
③H2O(l)=H2O(g) △H=+44KJ/mol
写出CO2与NH3合成尿素和液态水的热化学方程式
(4)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷(或氢气、一氧化碳等可燃性气体)和氧气构成燃料电池,则通入甲烷气体的一极是原电池的____ 极,该极的电极反应式是____ ,电池工作时的总反应的离子方程式是_____ 。
(2)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极气体,空气与CO2的混合气体为正极气体,制得650 ℃下工作的燃料电池,完成下列反应式:
正极:_______ ,
负极:2CO+2CO32--4e-=4CO2。
总反应:______ 。
(3)铅蓄电池放电时,总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O,由此可以判断:
①原电池的电极材料:负极:__ 。
②电极反应式:正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,负极反应式为_______ 。
③工作后,铅蓄电池里电解质溶液的pH____ (填“变大”“变小”或“不变”),理由是_____ 。
(2)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极气体,空气与CO2的混合气体为正极气体,制得650 ℃下工作的燃料电池,完成下列反应式:
正极:
负极:2CO+2CO32--4e-=4CO2。
总反应:
(3)铅蓄电池放电时,总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O,由此可以判断:
①原电池的电极材料:负极:
②电极反应式:正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,负极反应式为
③工作后,铅蓄电池里电解质溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
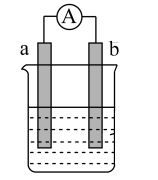
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为___ ,H+移向___ 极(填“a”或“b”)。
(2)现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液,则甲烷应通入__ 极(填“a”或“b”)。
(3)利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池,该电池的电解质溶液是___ 。
(4)若这是氢氧燃料电池,当有20molH2反应时,则导线中通过电子的物质的量为___ mol。
(5)如果电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液,当反应中收集到标准状况下224mL气体时,消耗的电极质量为__ g。

(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为
(2)现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液,则甲烷应通入
(3)利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池,该电池的电解质溶液是
(4)若这是氢氧燃料电池,当有20molH2反应时,则导线中通过电子的物质的量为
(5)如果电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液,当反应中收集到标准状况下224mL气体时,消耗的电极质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)地下钢管连接镁块是金属防腐措施中的_______ 法。
(2)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨Ⅰ为电池的_______ 极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为_______ 。
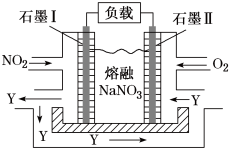
(3)铅及其化合物可用于蓄电池,耐酸设备及X射线防护材料等。回答下列问题:
①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为_______ 。
②铅蓄电池放电时的正极反应式为_______ ,当电路中有2mol电子转移时,理论上两电极质量变化的差值为_______ g。
(1)地下钢管连接镁块是金属防腐措施中的
(2)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨Ⅰ为电池的

(3)铅及其化合物可用于蓄电池,耐酸设备及X射线防护材料等。回答下列问题:
①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为
②铅蓄电池放电时的正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.能源的开发、利用与人类社会的可持续发展息息相关,充分利用好能源是摆在人类面前的重大课题。
(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是_______ (填字母)
A.C(s)+CO2(g)=2CO(g) ΔH>0
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH<0
C.2H2O(l)=2H2(g)+O2(g) ΔH>0
D.C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH<0
若以稀硫酸为电解质溶液,则该原电池的负极反应式为_______
Ⅱ.如图所示的装置,X、Y都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在Fe极附近显红色。试回答下列问题:
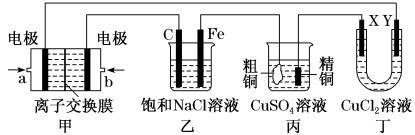
(2)甲装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是_______ (填“CH4”或“O2”),电极上发生的电极反应是_______
(3)在乙装置中,总反应的离子方程式是_______
(4)如果丙装置中精铜电极的质量增加了6.4 g,则甲装置中消耗的CH4的质量为_______
(5)丁装置中在通电一段时间后,Y电极上发生的电极反应是_______
(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是
A.C(s)+CO2(g)=2CO(g) ΔH>0
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH<0
C.2H2O(l)=2H2(g)+O2(g) ΔH>0
D.C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH<0
若以稀硫酸为电解质溶液,则该原电池的负极反应式为
Ⅱ.如图所示的装置,X、Y都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在Fe极附近显红色。试回答下列问题:

(2)甲装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是
(3)在乙装置中,总反应的离子方程式是
(4)如果丙装置中精铜电极的质量增加了6.4 g,则甲装置中消耗的CH4的质量为
(5)丁装置中在通电一段时间后,Y电极上发生的电极反应是
您最近一年使用:0次

 设计了如图所示的原电池。回答下列问题:
设计了如图所示的原电池。回答下列问题: