硫酸铈铵[ ,相对分子质量为596]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。以氟碳铈矿(含
,相对分子质量为596]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。以氟碳铈矿(含 等)为原料制备硫酸铈铵的工艺流程如图所示。
等)为原料制备硫酸铈铵的工艺流程如图所示。
 在空气中易被氧化为
在空气中易被氧化为 ;
; ;
;
回答下列问题:
(1)“滤渣A”的成分除 外,还有
外,还有_____________ (填化学式);
(2)“焙烧”时,下列采取的措施正确的是_____________(填标号);
(3)在另一种工艺中,在氟碳铈矿粉中加入碳酸氢钠固体同时通入氧气焙烧,得到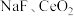 两种固体以及两种高温下的气态物质,该反应的化学方程式为
两种固体以及两种高温下的气态物质,该反应的化学方程式为____________________________ ;
(4)“酸浸”中,铈浸出率与温度的关系如图1所示,铈浸出率与硫酸浓度的关系如图2所示。工业生产应选择的适宜条件是_____________(填标号)。
(5) 分子中
分子中 键角
键角_________ (填“大于”“小于”或“等于”)硫脲分子中 键角;
键角;
(6)“溶解”时加入稀盐酸后,还需加入另一种化学试剂X,根据题中信息推测,加入X的作用是__________ ;
(7)含 溶液与足量
溶液与足量 溶液反应生成
溶液反应生成 沉淀的离子方程式为
沉淀的离子方程式为________________ ;
(8)利用硫化锌锂电池电解含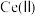 的溶液,可将
的溶液,可将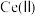 转化为
转化为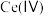 .该硫化锌锂电池放电时,负极材料的立方晶胞组成变化如图所示;
.该硫化锌锂电池放电时,负极材料的立方晶胞组成变化如图所示; 中,
中,
________ ;
②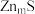 晶胞中,
晶胞中, 填充在
填充在 构成的部分正四面体空隙中,
构成的部分正四面体空隙中, 和
和 之间最近的核间距为
之间最近的核间距为 ,则
,则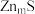 晶体的密度为
晶体的密度为__________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 ,相对分子质量为596]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。以氟碳铈矿(含
,相对分子质量为596]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。以氟碳铈矿(含 等)为原料制备硫酸铈铵的工艺流程如图所示。
等)为原料制备硫酸铈铵的工艺流程如图所示。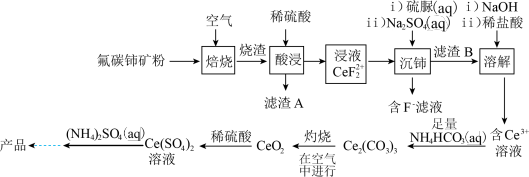
 在空气中易被氧化为
在空气中易被氧化为 ;
;②硫脲的结构简式为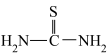 ,具有还原性;
,具有还原性;
 ;
;回答下列问题:
(1)“滤渣A”的成分除
 外,还有
外,还有(2)“焙烧”时,下列采取的措施正确的是_____________(填标号);
| A.采用高压空气,使矿粉呈“沸腾”状 |
| B.空气从焙烧炉上部通入,矿粉从焙烧炉下部加入 |
| C.空气从焙烧炉下部通入,矿粉从焙烧炉上部加入 |
| D.空气、矿粉均从焙烧炉上部通入或加入 |
(3)在另一种工艺中,在氟碳铈矿粉中加入碳酸氢钠固体同时通入氧气焙烧,得到
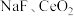 两种固体以及两种高温下的气态物质,该反应的化学方程式为
两种固体以及两种高温下的气态物质,该反应的化学方程式为(4)“酸浸”中,铈浸出率与温度的关系如图1所示,铈浸出率与硫酸浓度的关系如图2所示。工业生产应选择的适宜条件是_____________(填标号)。

A.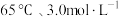 | B.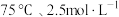 | C. | D. |
(5)
 分子中
分子中 键角
键角 键角;
键角;(6)“溶解”时加入稀盐酸后,还需加入另一种化学试剂X,根据题中信息推测,加入X的作用是
(7)含
 溶液与足量
溶液与足量 溶液反应生成
溶液反应生成 沉淀的离子方程式为
沉淀的离子方程式为(8)利用硫化锌锂电池电解含
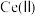 的溶液,可将
的溶液,可将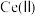 转化为
转化为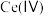 .该硫化锌锂电池放电时,负极材料的立方晶胞组成变化如图所示;
.该硫化锌锂电池放电时,负极材料的立方晶胞组成变化如图所示;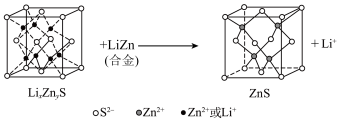
 中,
中,
②
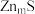 晶胞中,
晶胞中, 填充在
填充在 构成的部分正四面体空隙中,
构成的部分正四面体空隙中, 和
和 之间最近的核间距为
之间最近的核间距为 ,则
,则 晶体的密度为
晶体的密度为 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
更新时间:2024-05-14 14:51:24
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】钠、铝和铁是三种重要的金属。请回答:
(1)这三种金属中金属活动性最强的是______ (填元素符号)
(2)画出铝的原子结构示意图________ 。
(3)写出氯化铝的电离方程式________ 。
(4)把一小块金属钠投入水中,观察到以下各种现象:钠浮在水面上,熔成闪亮的小球,四处游动,逐渐减少,直至消失。写出该反应的化学方程式______ ;其中钠熔成闪亮小球的原因是_______ 。钠完全反应后,收集到标准状况下的氢气2.24L,则参加反应的钠的物质的量为______ mol。
(5)将(4)所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式:___________ 。
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的反应的离子方程式__________ ;继续将沉淀过滤、洗涤、干燥、灼烧,此时得到的固体为_____ (填化学式)。
(1)这三种金属中金属活动性最强的是
(2)画出铝的原子结构示意图
(3)写出氯化铝的电离方程式
(4)把一小块金属钠投入水中,观察到以下各种现象:钠浮在水面上,熔成闪亮的小球,四处游动,逐渐减少,直至消失。写出该反应的化学方程式
(5)将(4)所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式:
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】将两种盐混合后溶于水得到一种无色透明溶液,溶液中有下列离子中的某些离子: 、
、 、
、 、
、 、
、 、
、 、
、 和
和 。取该溶液进行如下实验:
。取该溶液进行如下实验:
Ⅰ.取少量溶液滴入紫色石蕊溶液,溶液呈红色。
Ⅱ.取少许溶液滴入过量的 溶液,有白色沉淀产生。过滤,向沉淀中加入足量稀盐酸,沉淀不溶解。
溶液,有白色沉淀产生。过滤,向沉淀中加入足量稀盐酸,沉淀不溶解。
Ⅲ.取步骤Ⅱ中滤液少许,先滴加硝酸酸化,再滴加 溶液,产生白色沉。
溶液,产生白色沉。
(1)根据以上现象判断,两种盐的混合溶液中肯定不存在的离子是______ ;两种盐分别是______ 和______ 。
(2)写出反应的离子方程式:实验Ⅱ中滴入过量的 溶液:
溶液:______ ;实验Ⅲ中:______ 。
(3)某同学取原混合液少许,滴加 溶液,产生白色沉淀,证明溶液中含有
溶液,产生白色沉淀,证明溶液中含有 。该同学的操作是否合理
。该同学的操作是否合理______ (填“合理”或“不合理”),如果认为不合理,说明你的理由:______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 和
和 。取该溶液进行如下实验:
。取该溶液进行如下实验:Ⅰ.取少量溶液滴入紫色石蕊溶液,溶液呈红色。
Ⅱ.取少许溶液滴入过量的
 溶液,有白色沉淀产生。过滤,向沉淀中加入足量稀盐酸,沉淀不溶解。
溶液,有白色沉淀产生。过滤,向沉淀中加入足量稀盐酸,沉淀不溶解。Ⅲ.取步骤Ⅱ中滤液少许,先滴加硝酸酸化,再滴加
 溶液,产生白色沉。
溶液,产生白色沉。(1)根据以上现象判断,两种盐的混合溶液中肯定不存在的离子是
(2)写出反应的离子方程式:实验Ⅱ中滴入过量的
 溶液:
溶液:(3)某同学取原混合液少许,滴加
 溶液,产生白色沉淀,证明溶液中含有
溶液,产生白色沉淀,证明溶液中含有 。该同学的操作是否合理
。该同学的操作是否合理
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某校化学实验兴趣小组欲采用如图所示的实验装置制备Cl2,同时进行与氯气有关的某些实验,按要求回答问题。
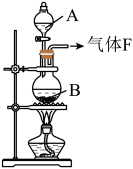
(1)A是浓盐酸,B是二氧化锰,将A滴入B中时发生反应的离子方程式为__________________________ 。
(2)甲同学用含有146 g HCl的浓盐酸与足量的MnO2反应制Cl2,结果制得的Cl2小于71 g,这是由于反应过程中盐酸浓度变小造成的。请列举导致盐酸浓度变小的原因:_________________ 。
(3)在实验室中,乙同学欲用下图中的装置净化氯气,则瓶①②中应盛放的试剂分别是:
①_________________ ,②__________ (填试剂名称)。
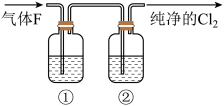
(4)丙同学将纯净的Cl2通入一定量石灰乳中来制取漂白粉,若通入x个Cl2完全反应,则反应过程中转移电子____________ 个。

(1)A是浓盐酸,B是二氧化锰,将A滴入B中时发生反应的离子方程式为
(2)甲同学用含有146 g HCl的浓盐酸与足量的MnO2反应制Cl2,结果制得的Cl2小于71 g,这是由于反应过程中盐酸浓度变小造成的。请列举导致盐酸浓度变小的原因:
(3)在实验室中,乙同学欲用下图中的装置净化氯气,则瓶①②中应盛放的试剂分别是:
①

(4)丙同学将纯净的Cl2通入一定量石灰乳中来制取漂白粉,若通入x个Cl2完全反应,则反应过程中转移电子
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
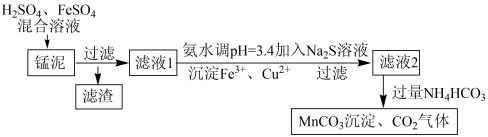
【推荐1】用软锰矿(主要成分为MnO2)生产高锰酸钾产生的锰泥中,还含有18%的MnO2、3%的KOH(均为质量分数),及少量Cu、Pb的化合物等,用锰泥可回收制取MnCO3,过程如图:
(1)高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强。通常用来酸化高锰酸钾的酸是______
A.H2SO4 B.HCl C.HNO3
(2)除去滤液1中Cu2+的离子方程式是___________________________
(3)经实验证明:MnO2稍过量时,起始H2SO4、FeSO4混合溶液中 <0.7时,滤液1中能够检验出有Fe2+;
<0.7时,滤液1中能够检验出有Fe2+; ≥0.7时,滤液1中不能检验出有Fe2+。根据上述信息回答①②:
≥0.7时,滤液1中不能检验出有Fe2+。根据上述信息回答①②:
①检验Fe2+是否氧化完全的实验试剂是__________ A.KSCN B.K3Fe(CN)6
②若 >1,调节
>1,调节 到0.7~1的最理想试剂是
到0.7~1的最理想试剂是_______ (填序号)
a.NaOH溶液 b.铁粉 c.MnO。
(4)写出滤液2中加入过量NH4HCO3反应的离子方程式__________ 。
(5)上述过程锰回收率可达95%,若处理1740 kg的锰泥,可生产MnCO3__________ kg。
(1)高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强。通常用来酸化高锰酸钾的酸是
A.H2SO4 B.HCl C.HNO3
(2)除去滤液1中Cu2+的离子方程式是
(3)经实验证明:MnO2稍过量时,起始H2SO4、FeSO4混合溶液中
 <0.7时,滤液1中能够检验出有Fe2+;
<0.7时,滤液1中能够检验出有Fe2+; ≥0.7时,滤液1中不能检验出有Fe2+。根据上述信息回答①②:
≥0.7时,滤液1中不能检验出有Fe2+。根据上述信息回答①②:①检验Fe2+是否氧化完全的实验试剂是
②若
 >1,调节
>1,调节 到0.7~1的最理想试剂是
到0.7~1的最理想试剂是a.NaOH溶液 b.铁粉 c.MnO。
(4)写出滤液2中加入过量NH4HCO3反应的离子方程式
(5)上述过程锰回收率可达95%,若处理1740 kg的锰泥,可生产MnCO3
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】钒酸铋( )是一种亮黄色无毒无害的光催化剂,主要应用于高选择性制备氢气。工业上以辉铋矿粉(主要成分是
)是一种亮黄色无毒无害的光催化剂,主要应用于高选择性制备氢气。工业上以辉铋矿粉(主要成分是 ,并含
,并含 、Bi、
、Bi、 和
和 等杂质)为原料制备钒酸铋(
等杂质)为原料制备钒酸铋( )的流程如图所示:
)的流程如图所示:
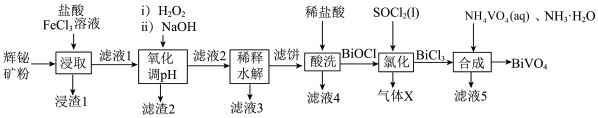
已知部分信息如下:
①氧化性: 。
。
②滤液1中的阴离子主要是 。
。
③常温下,几种离子生成氢氧化物沉淀的pH如下表所示:
当溶液中某离子浓度小于 时,视为沉淀完全。
时,视为沉淀完全。
回答下列问题:
(1)浸渣1的主要成分为_______ 。
(2)浸取时 转化的离子方程式为
转化的离子方程式为_______ 。
(3)从工艺流程分析,氧化调节pH环节,除了可用NaOH溶液,还可用_______ 调节,且需调至溶液的pH为_______ (填范围)。
(4)稀释水解时通常通入水蒸气,其目的是_______ ;水解的化学方程式为_______ 。
(5)设计实验检验气体X的成分:_______ 。
(6)常温下, 的
的 为
为_______ 。
 )是一种亮黄色无毒无害的光催化剂,主要应用于高选择性制备氢气。工业上以辉铋矿粉(主要成分是
)是一种亮黄色无毒无害的光催化剂,主要应用于高选择性制备氢气。工业上以辉铋矿粉(主要成分是 ,并含
,并含 、Bi、
、Bi、 和
和 等杂质)为原料制备钒酸铋(
等杂质)为原料制备钒酸铋( )的流程如图所示:
)的流程如图所示:
已知部分信息如下:
①氧化性:
 。
。②滤液1中的阴离子主要是
 。
。③常温下,几种离子生成氢氧化物沉淀的pH如下表所示:
| 氢氧化物 |  |  |  |
| 开始沉淀时的pH | 7.6 | 1.6 | 4.0 |
| 完全沉淀时的pH | 9.6 | 3.1 | 5.5 |
 时,视为沉淀完全。
时,视为沉淀完全。回答下列问题:
(1)浸渣1的主要成分为
(2)浸取时
 转化的离子方程式为
转化的离子方程式为(3)从工艺流程分析,氧化调节pH环节,除了可用NaOH溶液,还可用
(4)稀释水解时通常通入水蒸气,其目的是
(5)设计实验检验气体X的成分:
(6)常温下,
 的
的 为
为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5•H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3,白色片状晶体,溶于水和酒精等,对人体的受伤组织有防腐消毒作用)的工艺流程如图所示:
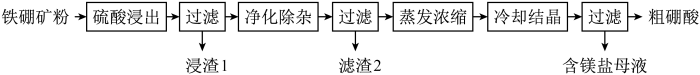
(1)硼在元素周期表中的位置为____ ;硼元素有两种天然同位素10B和11B,硼元素的近似相对原子质量为10.8,则两种同位素原子的原子个数之比为____ 。
(2)写出Mg2B2O5•H2O与硫酸反应的化学方程式:____ 。
(3)利用Fe3O4的磁性,可将其从“浸渣1”中分离,“浸渣1”中还剩余的物质是____ (化学式)。
(4)“净化除杂”需先加H2O2溶液,作用是:____ ;然后再调节溶液的pH约为5,目的是____ 。
(5)以硼酸为原料可制得硼氢化钠(NaBH4),其电子式为____ 。
(6)H3BO3溶液中存在H3BO3(aq)+H2O(l) [B(OH)4]-(aq)+H+(aq)平衡。下列关于硼酸的说法正确的是
[B(OH)4]-(aq)+H+(aq)平衡。下列关于硼酸的说法正确的是____ 。
a.H3BO3是一元酸
b.其水溶液中,水的电离平衡受到抑制
c.硼酸和过量NaOH溶液反应的方程式为H3BO3+NaOH=Na[B(OH)4]

(1)硼在元素周期表中的位置为
(2)写出Mg2B2O5•H2O与硫酸反应的化学方程式:
(3)利用Fe3O4的磁性,可将其从“浸渣1”中分离,“浸渣1”中还剩余的物质是
(4)“净化除杂”需先加H2O2溶液,作用是:
(5)以硼酸为原料可制得硼氢化钠(NaBH4),其电子式为
(6)H3BO3溶液中存在H3BO3(aq)+H2O(l)
 [B(OH)4]-(aq)+H+(aq)平衡。下列关于硼酸的说法正确的是
[B(OH)4]-(aq)+H+(aq)平衡。下列关于硼酸的说法正确的是a.H3BO3是一元酸
b.其水溶液中,水的电离平衡受到抑制
c.硼酸和过量NaOH溶液反应的方程式为H3BO3+NaOH=Na[B(OH)4]
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门。
信息二:氯化铬酰(CrO2Cl2)是铬的一种化合物,常温下该化合物是暗红色液体,熔点为-96.5℃,沸点为117℃,能和丙酮(CH3COCH3)、四氯化碳、CS2等有机溶剂互溶。
(1)铬(24号元素) 基态原子的电子排布式为___________ 。
(2)CH3COCH3分子中含有________ 个π键,含有____________ 个σ键。
(3)固态氯化铬酰属于______________ 晶体,丙酮中碳原子的杂化方式为______________ ,二硫化碳属于______________ (填“极性”或“非极性”)分子,分子中含有____________ (填“极性”或“非极性”)键。
(4)K[Cr(C2O4)2(H2O)2]也是铬的一种化合物,该化合物属于离子化合物,其中除含离子键、共价键外,还含有____________ 键。
(5)金属铬的晶胞如图所示,一个晶胞中含有_______ 个铬原子。

信息二:氯化铬酰(CrO2Cl2)是铬的一种化合物,常温下该化合物是暗红色液体,熔点为-96.5℃,沸点为117℃,能和丙酮(CH3COCH3)、四氯化碳、CS2等有机溶剂互溶。
(1)铬(24号元素) 基态原子的电子排布式为
(2)CH3COCH3分子中含有
(3)固态氯化铬酰属于
(4)K[Cr(C2O4)2(H2O)2]也是铬的一种化合物,该化合物属于离子化合物,其中除含离子键、共价键外,还含有
(5)金属铬的晶胞如图所示,一个晶胞中含有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】我国硒含量居世界首位,含硒化合物与材料被广泛应用于合成化学、催化化学医学研究、环境保护、农业化学品等方面。
(1)硒原子核外电子排布式为_______
(2)人体代谢甲硒醇(CH3SeH)后可增加抗癌活性,甲硒醇分子中碳原子和硒原子的杂化类型分别是_______ 、_______ 。下表中有机物沸点不同的原因是_______ 。
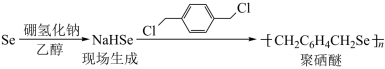
(3)NaHSe可用于合成聚硒醚,NaHSe晶体类型为_______ ,得到NaHSe过程中生成的化学键类型为_______ 。聚硒醚能清除水中的铅污染,其原因是_______ 。
(4)硒酸是一种强酸,根据价层电子对互斥理论的推测,其阴离子空间构型是_______
(5)Na2Se的晶体结构如下图所示,其晶胞参数为anm,阿伏加德罗常数值为NA.则Na2Se的晶胞密度为_______ g·cm-3(列出计算式)。

(1)硒原子核外电子排布式为
(2)人体代谢甲硒醇(CH3SeH)后可增加抗癌活性,甲硒醇分子中碳原子和硒原子的杂化类型分别是
| 有机物 | 甲醇 | 甲硫醇 | 甲硒醇 |
| 沸点/℃ | 64.7 | 5.95 | 25.05 |

(4)硒酸是一种强酸,根据价层电子对互斥理论的推测,其阴离子空间构型是
(5)Na2Se的晶体结构如下图所示,其晶胞参数为anm,阿伏加德罗常数值为NA.则Na2Se的晶胞密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】锰单质及其化合物应用十分广泛。回答下列问题:
(1)基态锰原子的核外电子排布式为___ ,Mn成为阳离子时首先失去___ 轨道电子。
(2)MnO和MnS的熔点分别为1650℃和1610℃,前者熔点较高的原因是__ 。
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

①THF中与Mn2+形成配位键的原子为__ (填元素符号)。
②BH4-的空间构型为__ ,写出两种与BH4-互为等电子体的分子或离子__ 。
(4)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为__ ;其中原子坐标参数A为(0,0,0),B为(0, ,
, ),则晶胞中氮原子的坐标参数为
),则晶胞中氮原子的坐标参数为__ 。

(5)金属锰有多种晶型,其中δ-Mn的结构为体心立方堆积,晶胞参数为apm,δ-Mn中锰的原子半径为__ pm。已知阿伏加 德罗常数的值为NA,δ-Mn的理论密度ρ=__ g•cm-3(列出计算式)。
(1)基态锰原子的核外电子排布式为
(2)MnO和MnS的熔点分别为1650℃和1610℃,前者熔点较高的原因是
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

①THF中与Mn2+形成配位键的原子为
②BH4-的空间构型为
(4)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为
 ,
, ),则晶胞中氮原子的坐标参数为
),则晶胞中氮原子的坐标参数为
(5)金属锰有多种晶型,其中δ-Mn的结构为体心立方堆积,晶胞参数为apm,δ-Mn中锰的原子半径为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】为了除去KCl固体中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按如图所示步骤操作:
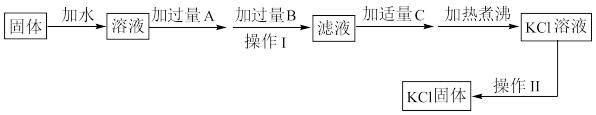
(1)①加入过量A的目的是_______ ,有关离子反应方程式为_______ 、_______ ;
②加入过量B的目的是_______ ;
③加热煮沸目的是_______ 。
(2)操作Ⅰ名称是_______ ,所需主要玻璃仪器有(写3种)_______ 、_______ 、_______ 。

(1)①加入过量A的目的是
②加入过量B的目的是
③加热煮沸目的是
(2)操作Ⅰ名称是
您最近一年使用:0次
【推荐2】工厂的含砷废水必须经过一定的处理。 某厂用某含砷废水(含HAsO2、H2SO4、及少量Fe3+、Cu2+、Bi2+ )提取三氧化二砷(俗称砒霜,分子式:As2O3)的流程如图:
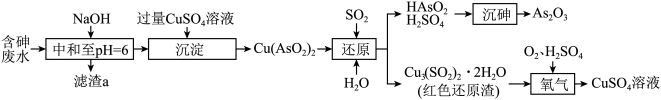
已知:Ksp[Fe(OH)3]=2.8 ×10-39,Ksp[Cu(OH)2]=2.2 ×10-22,Ksp [Bi(OH)3]=4.4 ×10-31。
回答下列问题:
(1)滤渣a的成分是_______ (写化学式)。
(2)“沉淀”时,CuSO4溶液必须过量的原因是_______ 。
(3)写出“还原”时Cu(AsO2)2与H2O、SO2发生反应的化学方程式:_______ 。
(4)红色还原渣(不溶于水)“氧化”时反应的离子方程式为_______ 。
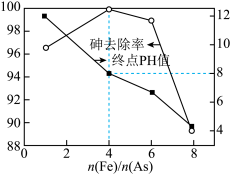
(5)“沉砷”后废水中残留的砷可用PFS(聚铁)进一步去除,用石灰乳调节废水的pH值,通入空气,PFS用量[以 表示]、终点pH值与砷去除率的关系如图所示。PFS除砷的最佳条件是
表示]、终点pH值与砷去除率的关系如图所示。PFS除砷的最佳条件是_______ 。
(6)当废水中砷质量浓度为5.0g·L-1时,若实验取75 L含砷废水,制得475.2 gAs2O3,则As元素的回收率为_______ 。
(7)已知I2 + AsO +2OH- ⇌2I-+AsO
+2OH- ⇌2I-+AsO +H2O。为验证该反应具有可逆性,将等物质的量浓度的碘水与Na3AsO3溶液按体积比为V1:V2的比例混合(另加入适量的碱)。当V1
+H2O。为验证该反应具有可逆性,将等物质的量浓度的碘水与Na3AsO3溶液按体积比为V1:V2的比例混合(另加入适量的碱)。当V1_______ V2 (填“>”或“<”) 时,只需加入_______ (填试剂名称)就可以确定该反应具有可逆性。上述反应显示:AsO 能在碱性溶液中被I2氧化成AsO
能在碱性溶液中被I2氧化成AsO ,而H3AsO4又能在酸性溶液中被I-还原成H3AsO3,这表明
,而H3AsO4又能在酸性溶液中被I-还原成H3AsO3,这表明_______ 。

已知:Ksp[Fe(OH)3]=2.8 ×10-39,Ksp[Cu(OH)2]=2.2 ×10-22,Ksp [Bi(OH)3]=4.4 ×10-31。
回答下列问题:
(1)滤渣a的成分是
(2)“沉淀”时,CuSO4溶液必须过量的原因是
(3)写出“还原”时Cu(AsO2)2与H2O、SO2发生反应的化学方程式:
(4)红色还原渣(不溶于水)“氧化”时反应的离子方程式为
(5)“沉砷”后废水中残留的砷可用PFS(聚铁)进一步去除,用石灰乳调节废水的pH值,通入空气,PFS用量[以
 表示]、终点pH值与砷去除率的关系如图所示。PFS除砷的最佳条件是
表示]、终点pH值与砷去除率的关系如图所示。PFS除砷的最佳条件是
(6)当废水中砷质量浓度为5.0g·L-1时,若实验取75 L含砷废水,制得475.2 gAs2O3,则As元素的回收率为
(7)已知I2 + AsO
 +2OH- ⇌2I-+AsO
+2OH- ⇌2I-+AsO +H2O。为验证该反应具有可逆性,将等物质的量浓度的碘水与Na3AsO3溶液按体积比为V1:V2的比例混合(另加入适量的碱)。当V1
+H2O。为验证该反应具有可逆性,将等物质的量浓度的碘水与Na3AsO3溶液按体积比为V1:V2的比例混合(另加入适量的碱)。当V1 能在碱性溶液中被I2氧化成AsO
能在碱性溶液中被I2氧化成AsO ,而H3AsO4又能在酸性溶液中被I-还原成H3AsO3,这表明
,而H3AsO4又能在酸性溶液中被I-还原成H3AsO3,这表明
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】硼是第IIIA族中唯一的非金属元素,可以形成众多的化合物。回答下列问题
(1)硼烷泛指一切硼和氢组成的化合物。乙硼烷(B2H6)是最简单的硼烷。可以在乙醚介质中使用LiAlH4(离子化合物)还原BCl3获得,LiAlH4的电子式是___________ ,制备乙硼烷的化学方程式为___________ 。
(2)工业利用硼矿石(2MgO•B2O3)制备单质B并联产轻质MgO的流程如下:

硼酸(H3BO3)的溶解度
回答下列问题:
①为了加快硼矿石与Na2CO3溶液和CO2的反应速率,可以采取的措施有___________ (填一种)。
②操作1是___________ ,整过流程中可循环利用的物质是___________ 。
③制备B发生反应的化学方程式是___________ ,过程中易生成金属硼化物杂质。该杂质的化学式是___________ 。
(3)硼酸(H3BO3)是一元弱酸,在溶液中能电离生成[B(OH)4]-,硼酸的电离方程式为___________ ;室温时测得0.1000 mol•L-1硼酸溶液的pH=5.18,硼酸的电离常数Ka=___________
(1)硼烷泛指一切硼和氢组成的化合物。乙硼烷(B2H6)是最简单的硼烷。可以在乙醚介质中使用LiAlH4(离子化合物)还原BCl3获得,LiAlH4的电子式是
(2)工业利用硼矿石(2MgO•B2O3)制备单质B并联产轻质MgO的流程如下:

硼酸(H3BO3)的溶解度
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 80 |
| 溶解度/g | 2.77 | 3.65 | 4.87 | 6.77 | 8.90 | 23.54 |
①为了加快硼矿石与Na2CO3溶液和CO2的反应速率,可以采取的措施有
②操作1是
③制备B发生反应的化学方程式是
(3)硼酸(H3BO3)是一元弱酸,在溶液中能电离生成[B(OH)4]-,硼酸的电离方程式为
您最近一年使用:0次



