氯化亚铜(CuCl)广泛应用于有机合成,难溶于水和乙醇,在潮湿空气中易氧化和水解。某学习小组探究CuCl的制备并测定纯度。回答下列问题:
已知:①
②某些含铜化合物和离子在水中的颜色和状态如下表:
Ⅰ.组装仪器,检查装置气密性,添加药品;
Ⅱ.水浴加热三颈烧瓶,打开K1、K2;
Ⅲ.待三颈烧瓶中溶液由黄绿色变为无色,关闭K1、K2;
Ⅳ.通过注射器向三颈烧瓶中加入水,生成白色沉淀,一段时间后部分沉淀变为棕红色。
(1)仪器a的名称为___________ ;B的作用为___________ (答出一点即可)。
(2)步骤Ⅲ反应的离子方程式为___________ 。
(3)步骤Ⅳ中,沉淀由白色转化为棕红色的原因___________ 。
(4)为防止生成棕红色固体,还需在原步骤Ⅰ中通过注射器往三颈烧瓶中加入一定量___________ (药品名称),再按上述步骤进行实验即可。
(5)产品先快速水洗后再醇洗,醇洗的目的为___________ 。
(6)测定CuCl产品纯度:将10.00 g产品溶于硝酸,配成250 mL溶液,取25.00 mL,加20.00 mL 0.5000 mol/L AgNO3溶液,充分反应后,加少量硝基苯覆盖沉淀。NH4Fe(SO4)2溶液作指示剂,用0.1000mol/L NH4SCN标准溶液滴定过量的AgNO3溶液,平行实验三次,平均消耗NH4SCN溶液10.00 mL。产品的纯度为___________ ,若未加入硝基苯会导致测定结果___________ (填“偏高”或“偏低”或“无影响”)。
[已知: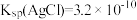 ,
,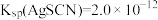 ]。
]。
已知:①

②某些含铜化合物和离子在水中的颜色和状态如下表:
| 化合物或离子 | CuCl | [CuCl4]2- | [CuCl3]2- | CuOH | Cu2O |
| 颜色和状态 | 白色沉淀 | 黄绿色溶液 | 无色溶液 | 黄色沉淀 | 棕红色沉淀 |
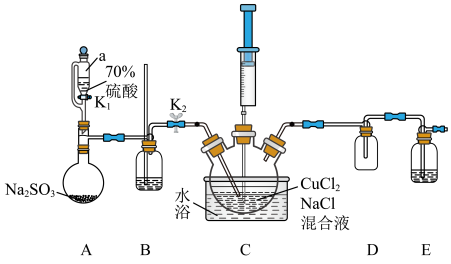
Ⅰ.组装仪器,检查装置气密性,添加药品;
Ⅱ.水浴加热三颈烧瓶,打开K1、K2;
Ⅲ.待三颈烧瓶中溶液由黄绿色变为无色,关闭K1、K2;
Ⅳ.通过注射器向三颈烧瓶中加入水,生成白色沉淀,一段时间后部分沉淀变为棕红色。
(1)仪器a的名称为
(2)步骤Ⅲ反应的离子方程式为
(3)步骤Ⅳ中,沉淀由白色转化为棕红色的原因
(4)为防止生成棕红色固体,还需在原步骤Ⅰ中通过注射器往三颈烧瓶中加入一定量
(5)产品先快速水洗后再醇洗,醇洗的目的为
(6)测定CuCl产品纯度:将10.00 g产品溶于硝酸,配成250 mL溶液,取25.00 mL,加20.00 mL 0.5000 mol/L AgNO3溶液,充分反应后,加少量硝基苯覆盖沉淀。NH4Fe(SO4)2溶液作指示剂,用0.1000mol/L NH4SCN标准溶液滴定过量的AgNO3溶液,平行实验三次,平均消耗NH4SCN溶液10.00 mL。产品的纯度为
[已知:
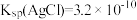 ,
,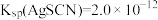 ]。
]。
更新时间:2024-05-14 20:19:32
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】已知常温下: ;
; ;
; ;
; ,
, 。
。
(1) 溶液中:
溶液中: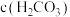
_____  。(填“<”或“>”或“=”)
。(填“<”或“>”或“=”)
(2)常温下,同浓度的①NaClO ② ③
③ ,pH由大到小的顺序为
,pH由大到小的顺序为________ (填序号)
(3)少量 气体分别通入到NaClO溶液、
气体分别通入到NaClO溶液、 溶液中反应的离子方程式:
溶液中反应的离子方程式:________ 。
(4)少量 溶液逐滴滴入到过量
溶液逐滴滴入到过量 溶液中反应的离子方程式:
溶液中反应的离子方程式:___________ ;该反应的化学平衡常数=______ 。
(5)珊瑚虫从周围海水中获取 和
和 形成珊瑚的反应离子方程式:
形成珊瑚的反应离子方程式:_________ 。
 ;
; ;
; ;
; ,
, 。
。(1)
 溶液中:
溶液中: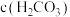
 。(填“<”或“>”或“=”)
。(填“<”或“>”或“=”)(2)常温下,同浓度的①NaClO ②
 ③
③ ,pH由大到小的顺序为
,pH由大到小的顺序为(3)少量
 气体分别通入到NaClO溶液、
气体分别通入到NaClO溶液、 溶液中反应的离子方程式:
溶液中反应的离子方程式:(4)少量
 溶液逐滴滴入到过量
溶液逐滴滴入到过量 溶液中反应的离子方程式:
溶液中反应的离子方程式:(5)珊瑚虫从周围海水中获取
 和
和 形成珊瑚的反应离子方程式:
形成珊瑚的反应离子方程式:
您最近一年使用:0次
【推荐2】离子反应是中学化学中重要的反应类型。请回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在的是_______(填字母)。
(2)有一瓶澄清的溶液,其中可能含有H+ 、Mg2+、Ba2+、 、
、 、
、 取该溶液进行以下实验:
取该溶液进行以下实验:
①用 pH 试纸检验,表明溶液呈强酸性,可以排除_______ 的存在。
②取出部分溶液逐滴加入 NaOH 溶液,使溶液从酸性逐渐变为碱性,继续滴加 NaOH 溶液,有白色沉淀产生,则产生白色沉淀的离子方程式为_______ 。
③取部分上述碱性溶液加Na2CO3 溶液,有白色沉淀生成,产生白色沉淀的离子方程式为_______ 。
④根据上述实验事实能确定溶液中肯定存在的离子是_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在的是_______(填字母)。
| A.单质 | B.氧化物 | C.盐 | D.化合物 |
 、
、 、
、 取该溶液进行以下实验:
取该溶液进行以下实验:①用 pH 试纸检验,表明溶液呈强酸性,可以排除
②取出部分溶液逐滴加入 NaOH 溶液,使溶液从酸性逐渐变为碱性,继续滴加 NaOH 溶液,有白色沉淀产生,则产生白色沉淀的离子方程式为
③取部分上述碱性溶液加Na2CO3 溶液,有白色沉淀生成,产生白色沉淀的离子方程式为
④根据上述实验事实能确定溶液中肯定存在的离子是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】甘氨酸亚铁[ ],是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法如下:
],是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法如下:

已知:①甘氨酸、甘氨酸亚铁易溶于水,微溶于乙醇、丙酮等有机溶剂
②异抗坏血酸易溶于水和乙醇、丙酮,有弱酸性和强还原性
③不同铁盐在有机溶剂中的溶解度如下表所示:
注:- -为不溶解;-为溶解不明显;+ -为溶解明显,+ +为全部溶解
请回答:
(1)如图所示合成装置中仪器b的名称是___________ 。

(2)流程中的亚铁盐和有机溶剂A应选择___________。
(3)合成过程中,本实验为了防止 被氧化,采取的措施除通入N2,还有
被氧化,采取的措施除通入N2,还有___________ 。
(4)步骤Ⅱ生成甘氨酸亚铁络合物的离子方程式___________ 。
(5)下列说法正确的是___________。
(6)合成过程需控制pH=5.5,试说明理由___________ 。
(7)产品分析:
①用酸性高锰酸钾溶液滴定法测定产品甘氨酸亚铁的 含量,进而计算产品甘氨酸亚铁的纯度,测定结果产品纯度总是大于100%,试分析主要原因可能是
含量,进而计算产品甘氨酸亚铁的纯度,测定结果产品纯度总是大于100%,试分析主要原因可能是___________ (滴定过程各项操作均正确)
②经查阅文献后,改用硫酸铈溶液滴定。称取5.000 g产品加酸溶解,用容量瓶配成250 mL溶液,移取25.00 mL于锥形瓶中,用0.1000 mol/L硫酸铈溶液滴定至终点。平行测定三次,平均消耗硫酸铈标准滴定溶液20.00 mL,计算产品中 的纯度为
的纯度为___________ 。(每1 mL 0.1000 mol/L硫酸铈溶液相当于20.40 mg甘氨酸亚铁)
 ],是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法如下:
],是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法如下:
已知:①甘氨酸、甘氨酸亚铁易溶于水,微溶于乙醇、丙酮等有机溶剂
②异抗坏血酸易溶于水和乙醇、丙酮,有弱酸性和强还原性
③不同铁盐在有机溶剂中的溶解度如下表所示:
| 铁盐 | 乙醇的体积分数/% | 丙酮的体积分数/% | ||||||||||||
| 100 | 90 | 80 | 70 | 60 | 50 | 40 | 100 | 90 | 80 | 70 | 60 | 50 | 40 | |
 | - - | - | - | - | - | - | + - | - - | - | - | - | - | - | + - |
 | + + | + + | + + | + + | + + | + + | + + | - - | - | - | - | - | - | + - |
请回答:
(1)如图所示合成装置中仪器b的名称是

(2)流程中的亚铁盐和有机溶剂A应选择___________。
A. 乙醇 乙醇 | B. 丙酮 丙酮 |
C. 乙醇 乙醇 | D. 丙酮 丙酮 |
 被氧化,采取的措施除通入N2,还有
被氧化,采取的措施除通入N2,还有(4)步骤Ⅱ生成甘氨酸亚铁络合物的离子方程式
(5)下列说法正确的是___________。
| A.滴入液体前,应先打开滴液漏斗a的上口玻璃塞 |
| B.步骤Ⅱ应采用水浴加热 |
| C.步骤Ⅲ中的分离方法是过滤 |
| D.步骤Ⅲ加入有机溶剂A的目的是降低甘氨酸亚铁在水中的溶解度,促使其结晶析出,同时除去杂质 |
(7)产品分析:
①用酸性高锰酸钾溶液滴定法测定产品甘氨酸亚铁的
 含量,进而计算产品甘氨酸亚铁的纯度,测定结果产品纯度总是大于100%,试分析主要原因可能是
含量,进而计算产品甘氨酸亚铁的纯度,测定结果产品纯度总是大于100%,试分析主要原因可能是②经查阅文献后,改用硫酸铈溶液滴定。称取5.000 g产品加酸溶解,用容量瓶配成250 mL溶液,移取25.00 mL于锥形瓶中,用0.1000 mol/L硫酸铈溶液滴定至终点。平行测定三次,平均消耗硫酸铈标准滴定溶液20.00 mL,计算产品中
 的纯度为
的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某烧碱样品含少量不与酸作用的杂质,为了测定其纯度,进行以下滴定操作
A.在250mL的容量瓶中定容配成250mL烧碱溶液
B.用移液管移取25mL烧碱溶液于锥形瓶中并滴几滴指示剂甲基橙
C.在天平上准确称取烧碱样品Wg,在烧杯中用蒸馏水溶解
D.将物质的量浓度为c的标准硫酸溶液装入酸式滴定管,调节液面,记下开始读数为V1
E.在锥形瓶下垫一张白纸,滴定至终点,记下读数V2
回答下列各问题:
(1)正确操作步骤的顺序是(用字母填写) → → →D→ 。______ 。
(2)滴定管的读数应注意_____ 。
(3)E中在锥形瓶下垫一张白纸的作用是_____ 。
(4)D步骤中液面应调节到____ ,尖嘴部分应_____ 。
(5)滴定终点时锥形瓶中颜色变化是_____ 。
(6)若酸式滴定管不用标准硫酸润洗,在其它操作均正确的前提下,会对测定结果_____ (指烧碱的纯度)有何影响?(指偏高、低或不变)
(7)该烧碱样品纯度的计算式为______ 。
A.在250mL的容量瓶中定容配成250mL烧碱溶液
B.用移液管移取25mL烧碱溶液于锥形瓶中并滴几滴指示剂甲基橙
C.在天平上准确称取烧碱样品Wg,在烧杯中用蒸馏水溶解
D.将物质的量浓度为c的标准硫酸溶液装入酸式滴定管,调节液面,记下开始读数为V1
E.在锥形瓶下垫一张白纸,滴定至终点,记下读数V2
回答下列各问题:
(1)正确操作步骤的顺序是(用字母填写) → → →D→ 。
(2)滴定管的读数应注意
(3)E中在锥形瓶下垫一张白纸的作用是
(4)D步骤中液面应调节到
(5)滴定终点时锥形瓶中颜色变化是
(6)若酸式滴定管不用标准硫酸润洗,在其它操作均正确的前提下,会对测定结果
(7)该烧碱样品纯度的计算式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】由白色和黑色固体组成的混合物A,可以发生如下框图所示的一系列变化:
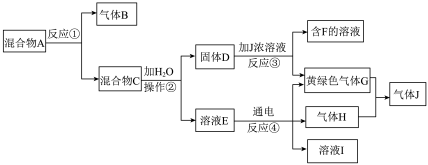
(1)写出反应③的化学方程式:_____________________________________________ 。写出反应④的离子方程式:_____________________________________________ 。
(2)在操作②中所使用的玻璃仪器的名称是:____________________________ 。
(3)下列实验装置中可用于实验室制取气体G的发生装置是______ ;(用字母表示)为了得到纯净干燥的气体G,可将气体通过c和d装置,c装置中存放的试剂_____ ,d装置中存放的试剂______ 。
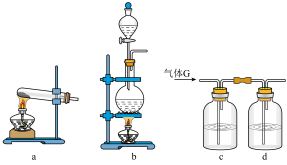
(4)气体G有毒,为了防止污染环境,必须将尾气进行处理,请写出实验室利用烧碱溶液吸收气体G的离子方程式:____________________________ 。
(5)J是一种极易溶于水的气体,为了防止倒吸,下列e~i装置中,可用于吸收J的是____________ 。
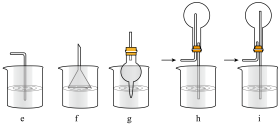
(6)某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数的测定。
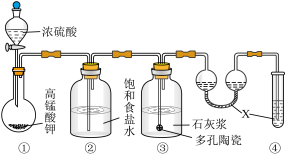
①装置③中发生反应的化学方程式为________________________________________
②测定漂白粉有效成分的质量分数:称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.100 0 mol·L-1KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。
反应原理为3ClO-+I-===3Cl-+IO3- IO3-+5I-+3H2O===6OH-+3I2
实验测得数据如下表所示。该漂白粉中有效成分的质量分数为________________ 。

(1)写出反应③的化学方程式:
(2)在操作②中所使用的玻璃仪器的名称是:
(3)下列实验装置中可用于实验室制取气体G的发生装置是

(4)气体G有毒,为了防止污染环境,必须将尾气进行处理,请写出实验室利用烧碱溶液吸收气体G的离子方程式:
(5)J是一种极易溶于水的气体,为了防止倒吸,下列e~i装置中,可用于吸收J的是

(6)某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数的测定。

①装置③中发生反应的化学方程式为
②测定漂白粉有效成分的质量分数:称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.100 0 mol·L-1KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。
反应原理为3ClO-+I-===3Cl-+IO3- IO3-+5I-+3H2O===6OH-+3I2
实验测得数据如下表所示。该漂白粉中有效成分的质量分数为
滴定次数 | 1 | 2 | 3 |
KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下采样和检测方法。回答下列问题:
NOx含量的测定:将v L气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3−,加水稀释至100.00 mL。量取20.00 mL该溶液,加入v1 mL c1 mol·L−1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。
(1)滴定操作使用的玻璃仪器主要有___________ 。
(2)滴定过程中发生下列反应:
①3Fe2++NO3−+4H+ NO↑+3Fe3++2H2O
NO↑+3Fe3++2H2O
②Cr2O72− + 6Fe2+ +14H+ 2Cr3+ +6Fe3++7H2O
2Cr3+ +6Fe3++7H2O
则气样中NOx折合成NO2的含量为_________ mg·m−3。
(3)若FeSO4标准溶液部分变质,会使测定结果___________ 。
NOx含量的测定:将v L气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3−,加水稀释至100.00 mL。量取20.00 mL该溶液,加入v1 mL c1 mol·L−1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。
(1)滴定操作使用的玻璃仪器主要有
(2)滴定过程中发生下列反应:
①3Fe2++NO3−+4H+
 NO↑+3Fe3++2H2O
NO↑+3Fe3++2H2O②Cr2O72− + 6Fe2+ +14H+
 2Cr3+ +6Fe3++7H2O
2Cr3+ +6Fe3++7H2O则气样中NOx折合成NO2的含量为
(3)若FeSO4标准溶液部分变质,会使测定结果
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某科研小组设计出利用工业废酸(含10%的H2SO4)和废弃铜锌矿制取活性ZnO的方案如图。

已知:298K时各离子开始沉淀及完全沉淀时的pH如表所示。
回答下列问题:
(1)在H2SO4作用下矿石中含有的ZnS溶解而CuS不溶解,这是由于相同温度下:Ksp(CuS)___ Ksp(ZnS)(填“>”、“<”或“=”)。
(2)除铁过程中试剂甲最好选用___ (填字母编号)。
A.KMnO4 B.H2O2 C.HNO3 D.Cl2
(3)除铁过程中加入氨水的目的是调节pH在范围之间___ 。
(4)沉淀Zn2+时发生反应的离子方程式为___ 。
(5)相同物质的量浓度的①NH4HSO4、②NH4HCO3、③NH4Cl三种溶液,pH值从大到小的顺序为____ (用数字标号填空,下同);相同温度下,NH 浓度相等的上述三种溶液,物质的量浓度从大到小的顺序为
浓度相等的上述三种溶液,物质的量浓度从大到小的顺序为____ 。
(6)含有Cr2O 的废水毒性较大。某工厂酸性废水中含5.0×10-3mol•L-1的Cr2O
的废水毒性较大。某工厂酸性废水中含5.0×10-3mol•L-1的Cr2O ,可先向废水中加入绿矾(FeSO4·7H2O),搅拌后撒入生石灰处理。
,可先向废水中加入绿矾(FeSO4·7H2O),搅拌后撒入生石灰处理。
①写出加入绿矾的离子方程式___ 。
②若处理后的废水中残留的c(Fe3+)=4.0×10-13mol•L-1,则残留的Cr3+的浓度为___ mol•L-1(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-33)。

已知:298K时各离子开始沉淀及完全沉淀时的pH如表所示。
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
(1)在H2SO4作用下矿石中含有的ZnS溶解而CuS不溶解,这是由于相同温度下:Ksp(CuS)
(2)除铁过程中试剂甲最好选用
A.KMnO4 B.H2O2 C.HNO3 D.Cl2
(3)除铁过程中加入氨水的目的是调节pH在范围之间
(4)沉淀Zn2+时发生反应的离子方程式为
(5)相同物质的量浓度的①NH4HSO4、②NH4HCO3、③NH4Cl三种溶液,pH值从大到小的顺序为
 浓度相等的上述三种溶液,物质的量浓度从大到小的顺序为
浓度相等的上述三种溶液,物质的量浓度从大到小的顺序为(6)含有Cr2O
 的废水毒性较大。某工厂酸性废水中含5.0×10-3mol•L-1的Cr2O
的废水毒性较大。某工厂酸性废水中含5.0×10-3mol•L-1的Cr2O ,可先向废水中加入绿矾(FeSO4·7H2O),搅拌后撒入生石灰处理。
,可先向废水中加入绿矾(FeSO4·7H2O),搅拌后撒入生石灰处理。①写出加入绿矾的离子方程式
②若处理后的废水中残留的c(Fe3+)=4.0×10-13mol•L-1,则残留的Cr3+的浓度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】2020年12月,嫦娥五号“探月”任务正在进行当中,本次任务将实现中国首次月球无人采样返回,助力深化月球成因和演化历史等科学探究,时隔n年,人类再一次成功取得月球样本,中国成为人类第三个获取月球样本的国家。电源是航天器在广袤太空中持续运行的重要支撑,嫦娥五号采用的是钴酸锂电源,以钴酸锂为正极材料所制备的锂离子电池,具有重量轻,比能量高,工作电压高,放电平衡、寿命长等特点。从废旧钴酸锂离子电池的正极材料(在铝箔上涂覆活性物质LiCoO2)中,回收钴、锂的操作流程如图所示:

回答下列问题。
(1)“过滤”所得滤液用盐酸处理可得到氢氧化铝,该反应的离子方程式为_______ ;
(2)LiCoO2中Co的化合价为_______ ,“酸浸”时主要反应的离子方程式为_______ ;若将硫酸、Na2S2O3溶液用一定浓度的盐酸替代,也可以达到“酸浸”的目的,但会产生_______ (填化学式)污染环境。
(3)“沉钴”后溶液中c(CO2+)=_______ 。(已知:Ksp[Co(OH)2]=1.09×10-15)
(4)根据下图判断:“沉锂”中获得Li2CO3固体的操作主要包括_______ 、_______ 、洗涤、干燥等步骤。证明Li2CO3固体已洗涤干净的实验方法_______ 。


回答下列问题。
(1)“过滤”所得滤液用盐酸处理可得到氢氧化铝,该反应的离子方程式为
(2)LiCoO2中Co的化合价为
(3)“沉钴”后溶液中c(CO2+)=
(4)根据下图判断:“沉锂”中获得Li2CO3固体的操作主要包括

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】近期发现, 是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是___________ (填标号)
a.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
b.常温下,氢硫酸的导电能力低于相同浓度的亚硫酸
c.常温下, 的氢硫酸和亚硫酸的
的氢硫酸和亚硫酸的 分别为4.5和2.1
分别为4.5和2.1
d.氢硫酸的还原性强于亚硫酸
(2)向 的水溶液中缓慢通入
的水溶液中缓慢通入 至饱和,再继续通一段时间,整个过程中
至饱和,再继续通一段时间,整个过程中 的变化情况为
的变化情况为___________
(3)常温下,向 溶液中通入
溶液中通入 气体或加入
气体或加入 固体,测得
固体,测得 与溶液
与溶液 的关系如图(忽略溶液体积的变化及
的关系如图(忽略溶液体积的变化及 的挥发)。请计算:
的挥发)。请计算:
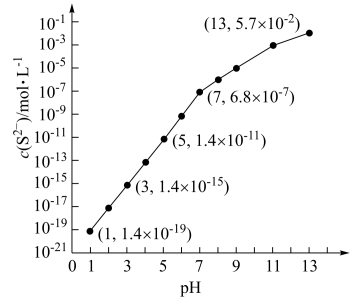
①当溶液中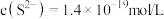 ,溶液中,水电离产生的
,溶液中,水电离产生的
___________ 
②当 时,溶液中
时,溶液中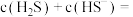
___________ 
(4)向 溶液中滴加饱和
溶液中滴加饱和 溶液,没有沉淀生成,继续滴加一定量的氨水后,生成
溶液,没有沉淀生成,继续滴加一定量的氨水后,生成 沉淀。用电离平衡原理解释上述现象
沉淀。用电离平衡原理解释上述现象___________
 是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是
a.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
b.常温下,氢硫酸的导电能力低于相同浓度的亚硫酸
c.常温下,
 的氢硫酸和亚硫酸的
的氢硫酸和亚硫酸的 分别为4.5和2.1
分别为4.5和2.1d.氢硫酸的还原性强于亚硫酸
(2)向
 的水溶液中缓慢通入
的水溶液中缓慢通入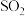 至饱和,再继续通一段时间,整个过程中
至饱和,再继续通一段时间,整个过程中 的变化情况为
的变化情况为(3)常温下,向
 溶液中通入
溶液中通入 气体或加入
气体或加入 固体,测得
固体,测得 与溶液
与溶液 的关系如图(忽略溶液体积的变化及
的关系如图(忽略溶液体积的变化及 的挥发)。请计算:
的挥发)。请计算:
①当溶液中
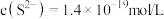 ,溶液中,水电离产生的
,溶液中,水电离产生的

②当
 时,溶液中
时,溶液中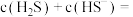

(4)向
 溶液中滴加饱和
溶液中滴加饱和 溶液,没有沉淀生成,继续滴加一定量的氨水后,生成
溶液,没有沉淀生成,继续滴加一定量的氨水后,生成 沉淀。用电离平衡原理解释上述现象
沉淀。用电离平衡原理解释上述现象
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】肉桂酸(白色或淡黄色固体),用于香精香料、合成药物等。实验室采用苯甲醛与醋酸酐[(CH3CO)2O]在催化剂的作用下合成肉桂酸,化学反应方程式如下:

相关数据如下表:

实验步骤:
步骤1.在干燥的仪器A中依次加入5 mL苯甲醛(0. 05 mol),14 mL醋酸酐(0. 146 mol),以及研细的7 g无水碳酸钾,振荡混合均匀,搅拌下升温至170°C,充分反应1 h。实验装置如图所示。
步骤2.冷却后,加入20mL.水,缓慢加入适量固体碳酸钠,将pH调至8。通入水蒸气进行蒸馏(实验装置图略),直到无油状物蒸出为止。
步骤3.向水蒸气蒸馏后的残留液中加入少量活性炭,煮沸数分钟至黄色混合液变为无色,趁热过滤,滤液冷却至室温,加入盐酸调节pH为4,析出大量晶体,过滤,洗涤,干燥得肉桂酸粗产品。
回答下列问题:
(1)仪器A的名称为______ ;球形冷凝管的进水口为_______ (填“a"或"b")。

(2)仪器A需干燥及冷凝管上方连接干燥装置,原因是_________ ;反应可逆,加入的醋酸酐过量,目的是_______ ;本实验为便于控制反应温度,下列加热方式中应选用的是______ .(填标号)。
a水浴 b.油浴 c.沙浴(传热较差,200°C或300°C以上适用)
(3)步骤2中水蒸气蒸馏时,分离出的杂质主要是_________ 。
(4)步骤3中有两次过滤,第一次趁热过滤的目的是______ ;滤液冷却后加入盐酸析出晶体的原因是________ (用离子方程式表示);第二次过能时,洗涤肉桂酸晶体应使用_____ (填标号)。
a.冷水 b.热水 c.无水乙醇 d.75%乙醇
(5)为提纯含杂质的晶体,常用的实验方法的名称为_______ ;若提纯后得到肉桂酸4. 420g,则产率为_______ 。

相关数据如下表:

实验步骤:
步骤1.在干燥的仪器A中依次加入5 mL苯甲醛(0. 05 mol),14 mL醋酸酐(0. 146 mol),以及研细的7 g无水碳酸钾,振荡混合均匀,搅拌下升温至170°C,充分反应1 h。实验装置如图所示。
步骤2.冷却后,加入20mL.水,缓慢加入适量固体碳酸钠,将pH调至8。通入水蒸气进行蒸馏(实验装置图略),直到无油状物蒸出为止。
步骤3.向水蒸气蒸馏后的残留液中加入少量活性炭,煮沸数分钟至黄色混合液变为无色,趁热过滤,滤液冷却至室温,加入盐酸调节pH为4,析出大量晶体,过滤,洗涤,干燥得肉桂酸粗产品。
回答下列问题:
(1)仪器A的名称为

(2)仪器A需干燥及冷凝管上方连接干燥装置,原因是
a水浴 b.油浴 c.沙浴(传热较差,200°C或300°C以上适用)
(3)步骤2中水蒸气蒸馏时,分离出的杂质主要是
(4)步骤3中有两次过滤,第一次趁热过滤的目的是
a.冷水 b.热水 c.无水乙醇 d.75%乙醇
(5)为提纯含杂质的晶体,常用的实验方法的名称为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】Co3O4在磁性材料、电化学领域应用广泛,实验室中可以用CoCO3或CoC2O4煅烧后制得。利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的流程如图所示

已知:Ksp[Co(OH)2]=1.6x10–15,Ksp(BaC2O4)=1.6×10–7 ,Ksp(CoC2O4)=6.3x10–8,CoCO3煅烧300℃~600℃生成Co3O4,1100℃以上生成Co2O3。
(1)“溶解还原”过程中Co(OH)3发生反应的离子方程式为___________ 。
(2)“沉钴”时,不能用Na2C2O4溶液代替(NH4)C2O4溶液,原因是______ 。
(3)检验CoC2O4固体是否洗净的实验操作是_____ 。
(4)为测定草酸钻样品中草酸钴晶体(CoC2O4·2H2O)的质量分数进行如下实验:
①取草酸钴(CoC2O4·2H2O 摩尔质量为183g·mol-1)样品3.050g,加入100.00mL 0.1000mol/L酸性KMnO4溶液,加热(该条件下Co2+不被氧化)。
②充分反应后将溶液冷却至室温,加入250mL容量瓶中,定容。
③取25.00mL溶液,用0.1000mol/LFeSO4溶液滴定,消耗FeSO4溶液18.00mL。
计算样品中草酸钴晶体(CoC2O4·2H2O)的质量分数:______ (写出计算过程)。
(5)以尿素为原料可获得CoCO3并制备Co3O4。已知:尿素水溶液在70℃以上能缓慢水解产生CO ,在pH为1~3时水解速率对生成CoCO3沉淀较为适宜。设计以CoCl2溶液、尿素粉末、盐酸为原料,制备Co3O4的实验方案:取一定体积CoCl2溶液
,在pH为1~3时水解速率对生成CoCO3沉淀较为适宜。设计以CoCl2溶液、尿素粉末、盐酸为原料,制备Co3O4的实验方案:取一定体积CoCl2溶液______ ,

已知:Ksp[Co(OH)2]=1.6x10–15,Ksp(BaC2O4)=1.6×10–7 ,Ksp(CoC2O4)=6.3x10–8,CoCO3煅烧300℃~600℃生成Co3O4,1100℃以上生成Co2O3。
(1)“溶解还原”过程中Co(OH)3发生反应的离子方程式为
(2)“沉钴”时,不能用Na2C2O4溶液代替(NH4)C2O4溶液,原因是
(3)检验CoC2O4固体是否洗净的实验操作是
(4)为测定草酸钻样品中草酸钴晶体(CoC2O4·2H2O)的质量分数进行如下实验:
①取草酸钴(CoC2O4·2H2O 摩尔质量为183g·mol-1)样品3.050g,加入100.00mL 0.1000mol/L酸性KMnO4溶液,加热(该条件下Co2+不被氧化)。
②充分反应后将溶液冷却至室温,加入250mL容量瓶中,定容。
③取25.00mL溶液,用0.1000mol/LFeSO4溶液滴定,消耗FeSO4溶液18.00mL。
计算样品中草酸钴晶体(CoC2O4·2H2O)的质量分数:
(5)以尿素为原料可获得CoCO3并制备Co3O4。已知:尿素水溶液在70℃以上能缓慢水解产生CO
 ,在pH为1~3时水解速率对生成CoCO3沉淀较为适宜。设计以CoCl2溶液、尿素粉末、盐酸为原料,制备Co3O4的实验方案:取一定体积CoCl2溶液
,在pH为1~3时水解速率对生成CoCO3沉淀较为适宜。设计以CoCl2溶液、尿素粉末、盐酸为原料,制备Co3O4的实验方案:取一定体积CoCl2溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】碱式碳酸镁有多种不同的组成,如:Mg2(OH)2CO3、Mg4(OH)2(CO3)3、Mg5(OH)2(CO3)4等。某研究性学习小组的同学们为了确定某碱式碳酸镁的组成,设下图所示的实验装置。

(1)实验步骤:
①按上图(夹持仪器未画出)组装好置后,首先进行的操作是___________ 。E处干燥管盛放的药品是___________ 。
②称取碱式碳酸镁样品m1g,并将其放入硬质玻璃管中;
称量:装浓硫酸的洗气瓶C的质量为m2g;装碱石灰的U形管D的质量为m3g
③打开活塞___________ ,关闭___________ 缓缓鼓入空气数分钟。
④关闭活塞___________ ,打开___________ ,点燃酒精灯加热,待不再产生气体为止。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为m4g;U形管D的质量为m5g.实验测得数据如下:m1=31g ,m2=87.6g ,m3= 74.7g,m4= 89.4g,m5= 87.9g,计算推导:该碱式碳酸镁的化学式为___________ 。
(2)关于该实验方案,以下说法你认为正确的是___________ (填字母)
A.硬质玻璃管中有水凝结对测定结果有较大影响
B.不称量碱式碳酸镁样品的质量无法确定碱式碳酸镁的组成
C.该实验装置也可用于确定天然碱[aNa2CO3·bNaHCO3·cH2O(a、b、c为正整数)]的化学组成

(1)实验步骤:
①按上图(夹持仪器未画出)组装好置后,首先进行的操作是
②称取碱式碳酸镁样品m1g,并将其放入硬质玻璃管中;
称量:装浓硫酸的洗气瓶C的质量为m2g;装碱石灰的U形管D的质量为m3g
③打开活塞
④关闭活塞
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为m4g;U形管D的质量为m5g.实验测得数据如下:m1=31g ,m2=87.6g ,m3= 74.7g,m4= 89.4g,m5= 87.9g,计算推导:该碱式碳酸镁的化学式为
(2)关于该实验方案,以下说法你认为正确的是
A.硬质玻璃管中有水凝结对测定结果有较大影响
B.不称量碱式碳酸镁样品的质量无法确定碱式碳酸镁的组成
C.该实验装置也可用于确定天然碱[aNa2CO3·bNaHCO3·cH2O(a、b、c为正整数)]的化学组成
您最近一年使用:0次



