含钴废渣中主要含有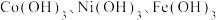 以及少量的钙、镁等杂质。一种提取钴氧化物的工艺流程如下:
以及少量的钙、镁等杂质。一种提取钴氧化物的工艺流程如下:
(1)“酸浸”过程中, 发生反应的离子方程式为
发生反应的离子方程式为_____________ 。
(2)“除铁”过程中加入 的作用是
的作用是_____________ 。
(3)“除杂”的目的是_____________ 。
(4)“沉钴”后需将沉淀洗净,检验沉淀已洗净的方法是_____________ 。“沉钴”所得固体经过滤、洗涤、干燥,得到纯度80%的 晶体。称取
晶体。称取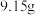 该晶体,在空气中加热一段时间后(杂质变为气态),得到
该晶体,在空气中加热一段时间后(杂质变为气态),得到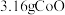 和
和 的混合物。该混合物中
的混合物。该混合物中 和
和 的质量之比
的质量之比_____________ 。
(5)“萃取”“反萃取”的目的是_____________ ;有机萃取剂与溶液的体积比 对溶液中
对溶液中 萃取率影响如图,则
萃取率影响如图,则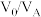 的最佳取值为
的最佳取值为_____________ 。
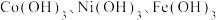 以及少量的钙、镁等杂质。一种提取钴氧化物的工艺流程如下:
以及少量的钙、镁等杂质。一种提取钴氧化物的工艺流程如下: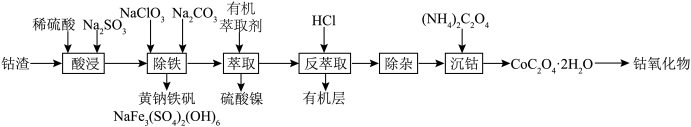
(1)“酸浸”过程中,
 发生反应的离子方程式为
发生反应的离子方程式为(2)“除铁”过程中加入
 的作用是
的作用是(3)“除杂”的目的是
(4)“沉钴”后需将沉淀洗净,检验沉淀已洗净的方法是
 晶体。称取
晶体。称取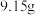 该晶体,在空气中加热一段时间后(杂质变为气态),得到
该晶体,在空气中加热一段时间后(杂质变为气态),得到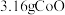 和
和 的混合物。该混合物中
的混合物。该混合物中 和
和 的质量之比
的质量之比(5)“萃取”“反萃取”的目的是
 对溶液中
对溶液中 萃取率影响如图,则
萃取率影响如图,则 的最佳取值为
的最佳取值为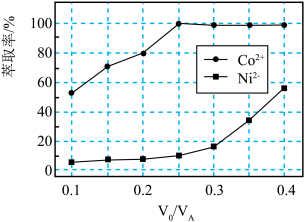
更新时间:2024-05-21 15:55:09
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某铜合金中Cu的质量分数为80%~90%,还含有Fe等。通常用间接碘量法测定其中Cu的含量,步骤如下:
Ⅰ.称取a g样品,加入稀H2SO4和H2O2溶液使其溶解,煮沸除去过量的H2O2,冷却后过滤,滤液定容于250 mL容量瓶中;
Ⅱ.取50.00 mL滤液于锥形瓶中,加入NH4F溶液,控制溶液pH为3~4,充分反应后,加入过量KI溶液,生成白色沉淀,溶液呈棕黄色;
Ⅲ.向Ⅱ的锥形瓶中加入c mol·L−1 Na2S2O3溶液滴定,至锥形瓶中溶液为浅黄色时,加入少量淀粉溶液,继续滴至浅蓝色,再加入KSCN溶液,剧烈振荡后滴至终点;
Ⅳ.平行测定三次,消耗Na2S2O3溶液的体积平均为v mL,计算铜的质量分数。
已知:ⅰ.F−与Fe3+生成稳定的FeF63−(无色)。
ⅱ.I2在水中溶解度小,易挥发。
ⅲ.I2+I− ⇌ I3−(棕黄色)。
ⅳ.I2+2Na2S2O3== 2NaI+Na2S4O6(无色)。
(1)Ⅰ中Cu溶解的离子方程式是__________________________ 。
(2)Ⅱ中Cu2+和I−反应生成CuI白色沉淀和I2。
①加入NH4F溶液的目的是__________________________ 。
②Cu2+和I−反应的离子方程式是_________________________ 。
③加入过量KI溶液的作用是________________________________ 。
(3)室温时,CuSCN的溶解度比CuI小。CuI沉淀表面易吸附I2和I3−,使测定结果不准确。Ⅲ中,在滴定至终点前加入KSCN溶液的原因是_ 。
(4)样品中Cu的质量分数为______ (列出表达式)。
Ⅰ.称取a g样品,加入稀H2SO4和H2O2溶液使其溶解,煮沸除去过量的H2O2,冷却后过滤,滤液定容于250 mL容量瓶中;
Ⅱ.取50.00 mL滤液于锥形瓶中,加入NH4F溶液,控制溶液pH为3~4,充分反应后,加入过量KI溶液,生成白色沉淀,溶液呈棕黄色;
Ⅲ.向Ⅱ的锥形瓶中加入c mol·L−1 Na2S2O3溶液滴定,至锥形瓶中溶液为浅黄色时,加入少量淀粉溶液,继续滴至浅蓝色,再加入KSCN溶液,剧烈振荡后滴至终点;
Ⅳ.平行测定三次,消耗Na2S2O3溶液的体积平均为v mL,计算铜的质量分数。
已知:ⅰ.F−与Fe3+生成稳定的FeF63−(无色)。
ⅱ.I2在水中溶解度小,易挥发。
ⅲ.I2+I− ⇌ I3−(棕黄色)。
ⅳ.I2+2Na2S2O3== 2NaI+Na2S4O6(无色)。
(1)Ⅰ中Cu溶解的离子方程式是
(2)Ⅱ中Cu2+和I−反应生成CuI白色沉淀和I2。
①加入NH4F溶液的目的是
②Cu2+和I−反应的离子方程式是
③加入过量KI溶液的作用是
(3)室温时,CuSCN的溶解度比CuI小。CuI沉淀表面易吸附I2和I3−,使测定结果不准确。Ⅲ中,在滴定至终点前加入KSCN溶液的原因是
(4)样品中Cu的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】孔雀石主要成分是 ,还含少量
,还含少量 及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:

有关物质沉淀的pH数据如下:
(1)步骤Ⅰ加稀硫酸充分反应,提高步骤Ⅰ反应速率的措施是_______ (写一条即可)。
(2)步骤Ⅱ中试剂①应选用试剂_______ (填代号)。
a. b.稀
b.稀 c.双氧水 d.氯水
c.双氧水 d.氯水
相关反应的离子方程式为:_______ 。
(3)步骤Ⅲ加入CuO调节溶液的pH至_______ (填写范围),目的是_______ 。
(4)从滤液3中获得干燥的硫酸铜晶体的操作是_______ 。
(5)常温下 的
的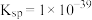 ,若要将溶液中的
,若要将溶液中的 转化为
转化为 沉淀,使溶液中
沉淀,使溶液中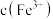 降低至
降低至 ,必须将溶液调节至
,必须将溶液调节至
_______ 。
(6)用 和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的
和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的 可以产生
可以产生 金属铜,则该反应的化学方程式为
金属铜,则该反应的化学方程式为_______ 。
 ,还含少量
,还含少量 及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
有关物质沉淀的pH数据如下:
| 物质 |  开始沉淀 开始沉淀 |  完全沉淀 完全沉淀 |
 | 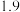 |  |
 | 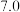 |  |
 |  | 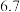 |
(1)步骤Ⅰ加稀硫酸充分反应,提高步骤Ⅰ反应速率的措施是
(2)步骤Ⅱ中试剂①应选用试剂
a.
 b.稀
b.稀 c.双氧水 d.氯水
c.双氧水 d.氯水相关反应的离子方程式为:
(3)步骤Ⅲ加入CuO调节溶液的pH至
(4)从滤液3中获得干燥的硫酸铜晶体的操作是
(5)常温下
 的
的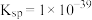 ,若要将溶液中的
,若要将溶液中的 转化为
转化为 沉淀,使溶液中
沉淀,使溶液中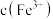 降低至
降低至 ,必须将溶液调节至
,必须将溶液调节至
(6)用
 和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的
和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的 可以产生
可以产生 金属铜,则该反应的化学方程式为
金属铜,则该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】苯胺是重要的化工原料,某化学兴趣小组在实验室里制备苯胺并提纯苯胺。
有关物质的部分物理性质如表:
I.制备苯胺
将如下图所示装置(夹持装置略,下同)置于热水浴中回流 ,使硝基苯充分还原;冷却后,往三颈烧瓶中加入
,使硝基苯充分还原;冷却后,往三颈烧瓶中加入 溶液。
溶液。 的作用是
的作用是______ ,三颈烧瓶合适的容积是______ 。
a. b.
b. c.
c.
(2)使用水浴加热的优点是______ ,三颈烧瓶中反应生成 和易溶于水的盐酸苯胺(
和易溶于水的盐酸苯胺(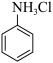 ),该反应的离子方程式为
),该反应的离子方程式为______ 。
(3)加入 的目的是
的目的是______ 。
II.提取苯胺
(4)实验步骤:
①向反应后混合物中通入热的水蒸气进行蒸馏,蒸馏时收集到苯胺与水的混合物;将此混合物分离得到粗苯胺和水溶液。
②向水溶液中加入适量乙醚萃取,然后分液得到乙醚萃取液。分液必须使用到的一种玻璃仪器名称是______ 。
③合并粗苯胺和乙醚萃取液,再加入______ 固体后再次蒸馏,得到纯苯胺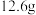 。
。
(5)该实验中苯胺的产率为______ (保留3位小数)。
有关物质的部分物理性质如表:
物质 | 熔点 | 沸点 | 溶解性 | 密度 | 相对分子质量 |
苯胺 |
| 184 | 微溶于水,易溶于乙醚 | 1.02 | 93 |
硝基苯 | 5.7 | 210.9 | 难溶于水,易溶于乙醚 | 1.23 | 123 |
乙醚 |
| 34.6 | 微溶于水 | 0.7134 |
将如下图所示装置(夹持装置略,下同)置于热水浴中回流
 ,使硝基苯充分还原;冷却后,往三颈烧瓶中加入
,使硝基苯充分还原;冷却后,往三颈烧瓶中加入 溶液。
溶液。
 的作用是
的作用是a.
 b.
b. c.
c.
(2)使用水浴加热的优点是
 和易溶于水的盐酸苯胺(
和易溶于水的盐酸苯胺( ),该反应的离子方程式为
),该反应的离子方程式为(3)加入
 的目的是
的目的是II.提取苯胺
(4)实验步骤:
①向反应后混合物中通入热的水蒸气进行蒸馏,蒸馏时收集到苯胺与水的混合物;将此混合物分离得到粗苯胺和水溶液。
②向水溶液中加入适量乙醚萃取,然后分液得到乙醚萃取液。分液必须使用到的一种玻璃仪器名称是
③合并粗苯胺和乙醚萃取液,再加入
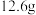 。
。(5)该实验中苯胺的产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某油脂厂废弃的油脂加氢所用催化剂主要含金属Ni、Al、Fe及他们的氧化物,还有少量其他不溶性物质。采用如图工艺流程回收其中的镍来制备硫酸镍晶体(NiSO4·7H2O):

溶液中金属离子开始沉淀和完全沉淀的pH如表所示,回答下列问题:
(1)废弃催化剂上的油脂在_______ 过程中被处理
(2)滤液①中含有的无机阴离子除OH-离子外还有_______ 。
(3)“转化”过程的离子方程式_______ ;“转化”过程宜控制较低温度的原因是_______ 。
(4)加NaOH溶液“调pH”应控制的pH范围是_______ 。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式_______ 。
(6)操作I为_______ 、_______ 、过滤、洗涤、干燥,得到产品。

溶液中金属离子开始沉淀和完全沉淀的pH如表所示,回答下列问题:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时的pH | 6.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(2)滤液①中含有的无机阴离子除OH-离子外还有
(3)“转化”过程的离子方程式
(4)加NaOH溶液“调pH”应控制的pH范围是
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
(6)操作I为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:

已知:①硫酸浸取中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH值如下:
③Cr2O +H2O=CrO
+H2O=CrO +2H+
+2H+
(1)实验室用12.5mol/L的硫酸配制480ml 2mol/L的硫酸,需量取12.5mol/L的硫酸_______ ml。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O ,写出此反应的离子方程式
,写出此反应的离子方程式_____ 。
(3)加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时又可以将Cr2O 转化为
转化为____________ (填微粒的化学式)。
(4)钠离子交换树脂的反应原理为:Mn++nNaR MR+nNa+则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有
MR+nNa+则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有 ___________ 。
(5)写出上述流程中用SO2进行还原时发生反应的离子方程式_______ 。
(6)沉淀滴定法是测定粒子浓度的方法之一。为了测定某废水中SCN-浓度,可用标准AgNO3溶液滴定待测液,已知:
滴定时下列试剂可选为滴定指示剂的是 ________ (填字母代号),滴定终点的现象是_____ 。
A NaCl B K2CrO4 C KI D NaCN

已知:①硫酸浸取中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH值如下:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 沉淀完全时的pH值 | 3.7 | 11.1 | 5.4(>8溶解) | 9(>溶解) |
 +H2O=CrO
+H2O=CrO +2H+
+2H+(1)实验室用12.5mol/L的硫酸配制480ml 2mol/L的硫酸,需量取12.5mol/L的硫酸
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O
 ,写出此反应的离子方程式
,写出此反应的离子方程式(3)加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时又可以将Cr2O
 转化为
转化为(4)钠离子交换树脂的反应原理为:Mn++nNaR
 MR+nNa+则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有
MR+nNa+则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有 (5)写出上述流程中用SO2进行还原时发生反应的离子方程式
(6)沉淀滴定法是测定粒子浓度的方法之一。为了测定某废水中SCN-浓度,可用标准AgNO3溶液滴定待测液,已知:
| 银盐性质 | AgCl | AgI | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 黄 | 白 | 砖红 | 白 |
| KW | 1.8×10﹣10 | 8.3×10﹣17 | 1.2×10﹣16 | 3.5×10﹣11 | 1.0×10﹣12 |
A NaCl B K2CrO4 C KI D NaCN
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】回收稀土元素对促进稀土资源循环利用有十分重要的意义。利用钕铁硼合金废料制备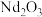 和
和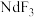 的工艺流程如下:
的工艺流程如下:
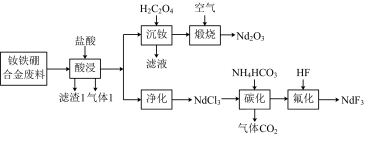
已知:①硼不与盐酸反应;钕离子可与足量 生成可溶性配合物。
生成可溶性配合物。
②25℃,相关物质的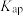 见下表。
见下表。
回答下列问题:
(1)探究不同条件下,“酸浸”操作中钕、铁元素的浸出率,如下表所示。
①酒石酸的作用是___________ 。
②温度升高钕浸出率降低,可能原因是___________ 。
(2)“沉钕”过程中,当草酸实际用量与理论计算量比值大于1.5时,沉钕率下降的原因是________ ;“沉钕”后的晶体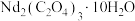 在空气中充分煅烧的化学方程式为
在空气中充分煅烧的化学方程式为________ 。
(3)“净化”时需先加入试剂将 氧化成
氧化成 ,再用氨水调溶液的
,再用氨水调溶液的 ,则
,则 的理论最小值为
的理论最小值为___________ (当溶液中某离子浓度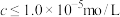 时,可认为该离子沉淀完全);“碳化”过程的离子方程式为
时,可认为该离子沉淀完全);“碳化”过程的离子方程式为___________ 。
(4)利用膜电解技术(装置如图所示),以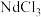 溶液为原料制备
溶液为原料制备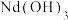 ,阳极电极反应式为
,阳极电极反应式为___________ ,电解时通过膜的离子主要为___________ 。

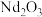 和
和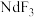 的工艺流程如下:
的工艺流程如下:
已知:①硼不与盐酸反应;钕离子可与足量
 生成可溶性配合物。
生成可溶性配合物。②25℃,相关物质的
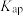 见下表。
见下表。| 物质 | 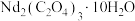 |  |  |  |
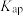 | 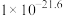 |  | 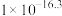 | 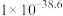 |
(1)探究不同条件下,“酸浸”操作中钕、铁元素的浸出率,如下表所示。
| 序号 | 温度(℃) | 盐酸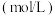 | 酒石酸浓度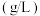 | Fe的浸出率(%) |  的浸出率(%) 的浸出率(%) |
| I | 40 | 4 | 0 | 69.15 | 87.22 |
| Ⅱ | 50 | 4 | 0 | 65.35 | 83.45 |
| Ⅲ | 40 | 6 | 0 | 74.64 | 91.05 |
| Ⅳ | 40 | 6 | 50 | 71.54 | 93.62 |
②温度升高钕浸出率降低,可能原因是
(2)“沉钕”过程中,当草酸实际用量与理论计算量比值大于1.5时,沉钕率下降的原因是
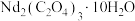 在空气中充分煅烧的化学方程式为
在空气中充分煅烧的化学方程式为(3)“净化”时需先加入试剂将
 氧化成
氧化成 ,再用氨水调溶液的
,再用氨水调溶液的 ,则
,则 的理论最小值为
的理论最小值为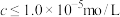 时,可认为该离子沉淀完全);“碳化”过程的离子方程式为
时,可认为该离子沉淀完全);“碳化”过程的离子方程式为(4)利用膜电解技术(装置如图所示),以
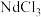 溶液为原料制备
溶液为原料制备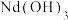 ,阳极电极反应式为
,阳极电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】四钼酸铵是钼深加工的重要中间产品具有广泛的用途。一种以钼精矿(主要含MoS2,还有Cu、Fe的化合物及SiO2等)为原料制备四钼酸铵的工艺流程如下图所示。

回答下列问题:
(1)“焙烧”产生的气体用
(2)“浸出”时,MoO3转化为MoO
 ,已知Na2MoO4溶解度超过80℃明显降低。
,已知Na2MoO4溶解度超过80℃明显降低。①“浸取”在如图所示装置中进行,保持温度、反应物和溶剂的量不变,提高单位时间内钼浸出率的措施有
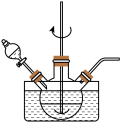
②温度对90min内钼浸出率的影响如图所示。当浸出温度超过80℃后,钼的浸出率反而降低,主要原因是温度升高使水大量蒸发,导致

(3)“净化”时,浸出液中残留的Cu2+、Fe2+转化为沉淀除去。为了使溶液中的Fe2+杂质离子浓度小于1.0×10-6mol·L-1,应控制溶液的S2-浓度不小于
(4)“净化”后,溶液中若有低价钼(以MoO
 表示),可加入适量H2O2将其氧化为MoO
表示),可加入适量H2O2将其氧化为MoO ,反应的离子方程式为
,反应的离子方程式为(5)“沉淀”时,加入NH4NO3的目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】金属铜在人类文明中有悠久的历史,火法炼铜是铜的主要冶炼方式。以硫化铜精矿(含有铁、砷等杂质)火法炼铜的工艺流程如下:

已知:①造锍(liǚ)熔炼和铜锍吹炼的温度均在1200 左右,铜锍(
左右,铜锍( 、FeS)的熔点为1000
、FeS)的熔点为1000 左右。②熔炼渣中
左右。②熔炼渣中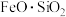 ,可以附着在熔剂表面。
,可以附着在熔剂表面。
请回答下列问题:
(1)造锍熔炼和铜锍吹炼均产生熔炼渣,熔炼渣中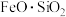 ,易与液态铜锍形成浆状物从而难以分离。为顺利从铜锍中分离出熔炼渣,采取的措施是
,易与液态铜锍形成浆状物从而难以分离。为顺利从铜锍中分离出熔炼渣,采取的措施是___________ 。
(2)在冶炼过程中通过造锍后制粗铜,并非直接由矿石制粗铜的原因___________ 。
(3)写出铜锍吹炼时 发生反应的化学方程式
发生反应的化学方程式___________ 。
(4)绿水青山就是金山银山,环境保护是每位化学研究者的义务。火法炼铜产生的废气烟尘通常含有三价砷元素( ),三价砷元素的毒性是五价砷元素的60倍。通常采用氧化浸出液(含NaOH和NaClO)来处理烟尘用以降低毒性,该过程称为“烟尘除砷”。“烟尘除砷”反应的化学方程式为
),三价砷元素的毒性是五价砷元素的60倍。通常采用氧化浸出液(含NaOH和NaClO)来处理烟尘用以降低毒性,该过程称为“烟尘除砷”。“烟尘除砷”反应的化学方程式为___________ 。“烟尘除砷”所用的氧化浸出液通常使用余氯吸收废液来替代,原因为___________ 。
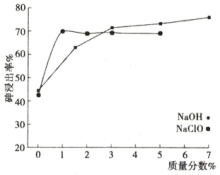
(5)合理的反应条件是工业生产的重要问题,烟尘中三价砷的去除率与氧化浸出液中各反应成分的质量分数的关系如图所示,则氧化浸出液中各反应成分的最佳质量分数是___________ 。

已知:①造锍(liǚ)熔炼和铜锍吹炼的温度均在1200
 左右,铜锍(
左右,铜锍( 、FeS)的熔点为1000
、FeS)的熔点为1000 左右。②熔炼渣中
左右。②熔炼渣中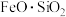 ,可以附着在熔剂表面。
,可以附着在熔剂表面。请回答下列问题:
(1)造锍熔炼和铜锍吹炼均产生熔炼渣,熔炼渣中
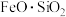 ,易与液态铜锍形成浆状物从而难以分离。为顺利从铜锍中分离出熔炼渣,采取的措施是
,易与液态铜锍形成浆状物从而难以分离。为顺利从铜锍中分离出熔炼渣,采取的措施是(2)在冶炼过程中通过造锍后制粗铜,并非直接由矿石制粗铜的原因
(3)写出铜锍吹炼时
 发生反应的化学方程式
发生反应的化学方程式(4)绿水青山就是金山银山,环境保护是每位化学研究者的义务。火法炼铜产生的废气烟尘通常含有三价砷元素(
 ),三价砷元素的毒性是五价砷元素的60倍。通常采用氧化浸出液(含NaOH和NaClO)来处理烟尘用以降低毒性,该过程称为“烟尘除砷”。“烟尘除砷”反应的化学方程式为
),三价砷元素的毒性是五价砷元素的60倍。通常采用氧化浸出液(含NaOH和NaClO)来处理烟尘用以降低毒性,该过程称为“烟尘除砷”。“烟尘除砷”反应的化学方程式为(5)合理的反应条件是工业生产的重要问题,烟尘中三价砷的去除率与氧化浸出液中各反应成分的质量分数的关系如图所示,则氧化浸出液中各反应成分的最佳质量分数是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】现有一定量含有 杂质的
杂质的 试样,用如图所示的实验装置测定
试样,用如图所示的实验装置测定 试样的纯度。(可供选用的试剂只有
试样的纯度。(可供选用的试剂只有 固体、6
固体、6 盐酸、6
盐酸、6 硫酸和蒸馏水)
硫酸和蒸馏水)

请回答下列问题:
(1)装置A中的液体试剂选用_______ 。
(2)装置B的作用是_______ ,装置E中碱石灰的作用是_______ 。
(3)装置D中发生反应的化学方程式是:_______ 、_______ 。
 杂质的
杂质的 试样,用如图所示的实验装置测定
试样,用如图所示的实验装置测定 试样的纯度。(可供选用的试剂只有
试样的纯度。(可供选用的试剂只有 固体、6
固体、6 盐酸、6
盐酸、6 硫酸和蒸馏水)
硫酸和蒸馏水)
请回答下列问题:
(1)装置A中的液体试剂选用
(2)装置B的作用是
(3)装置D中发生反应的化学方程式是:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室用废铁屑制备硫酸铁铵[NH4Fe(SO4)2·xH2O],具体流程如下:
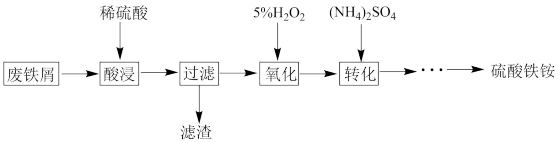
(1)废铁屑需用热的纯碱溶液洗涤,其目的是___________ 。
(2)“酸浸”是温度需保持为80~95℃,采用的合适加热方式是___________ 。实验室过滤操作必须用到的玻璃仪器有烧杯、 ___________ 。
(3)5%H2O2的作用是氧化Fe2+(“酸浸”过程稀硫酸过量),写出该反应的离子方程式是___________ 。
(4)“转化”后制取硫酸铁铵晶体的操作主要包括___________ 、过滤、洗涤、干燥。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150℃时失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为___________ 。

(1)废铁屑需用热的纯碱溶液洗涤,其目的是
(2)“酸浸”是温度需保持为80~95℃,采用的合适加热方式是
(3)5%H2O2的作用是氧化Fe2+(“酸浸”过程稀硫酸过量),写出该反应的离子方程式是
(4)“转化”后制取硫酸铁铵晶体的操作主要包括
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150℃时失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】为测定碱式碳酸钴[Cox(OH)y(CO3)z]的化学组成,研究性学习小组的同学设计了如图所示的装置进行实验探究。已知:碱式碳酸钴受热时可分解生成三种氧化物。

(1)按如图所示装置组装好仪器,并______ (填操作名称);称取3.65g样品置于硬质玻璃管内,加热,当乙装置中______ (填实验现象),停止加热;打开活塞a,缓缓通入空气数分钟,通入空气的目的是______ 。
(2)丁的作用是______ ,某同学认为上述实验中存在一个缺陷,该缺陷是______ 。
(3)通过正确实验测得乙、丙装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为______ 。
(4)CoCl2·6H2O常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种工艺如图:

已知:25℃时
①净化除杂时,加入H2O2发生反应的离子方程式为______ ;
②加入CoCO3调pH为5.2~7.6,则操作I获得的滤渣成分为______ ;
③加盐酸调整pH为2~3的目的为______ ;
④操作II过程为蒸发浓缩、冷却结晶、过滤。

(1)按如图所示装置组装好仪器,并
(2)丁的作用是
(3)通过正确实验测得乙、丙装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为
(4)CoCl2·6H2O常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种工艺如图:

已知:25℃时
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
①净化除杂时,加入H2O2发生反应的离子方程式为
②加入CoCO3调pH为5.2~7.6,则操作I获得的滤渣成分为
③加盐酸调整pH为2~3的目的为
④操作II过程为蒸发浓缩、冷却结晶、过滤。
您最近一年使用:0次



 是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 等)为原料制备
等)为原料制备


 的溶解度曲线。从“含
的溶解度曲线。从“含


