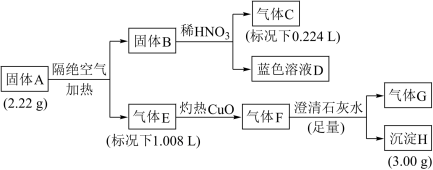
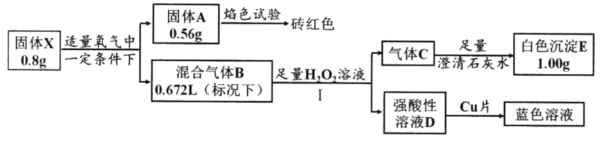
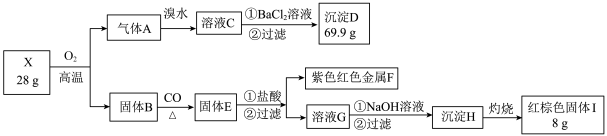
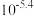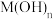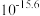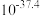为探究某矿物X(含三种常见元素)的组成和性质,某兴趣小组设计了如下实验:已知实验中所用试剂均足量,固体B是一种单质和化合物的混合物,请回答如下问题:______ 。
(2)气体A与溴水反应的离子方程式:______ 。
(3)X在高温下与氧气充分反应的化学方程式:______ 。
(4)红棕色固体Ⅰ溶于HI溶液的离子方程式______ 。
(5)检验溶液G中的金属阳离子的实验方案:______ 。
(2)气体A与溴水反应的离子方程式:
(3)X在高温下与氧气充分反应的化学方程式:
(4)红棕色固体Ⅰ溶于HI溶液的离子方程式
(5)检验溶液G中的金属阳离子的实验方案:
更新时间:2024-05-25 09:10:39
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】利用高压氨浸法从黄铜矿中提取铜具有提取率高、污染小等优点,被广泛使用。一种由黄铜矿(主要成分为 ,含少量
,含少量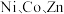 等元素)提取铜的工艺如下:
等元素)提取铜的工艺如下:
I.“固液分离”后溶液中主要离子为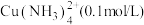 ,杂质离子为
,杂质离子为 、
、 、
、 等阳离子(浓度均为
等阳离子(浓度均为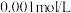 );“电积”时溶液中主要溶质为
);“电积”时溶液中主要溶质为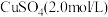 。
。
Ⅱ.不稳定常数对 ,不稳定常数
,不稳定常数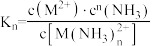
Ⅲ.溶度积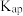
(1)基态 原子的价电子排布式为
原子的价电子排布式为________________ , 中氮原子的杂化方式为
中氮原子的杂化方式为_______________ 。
(2)①浸出前“粉碎磨矿”的目的是_______________ ,②“固液分离”用到的操作是_______________ 。
(3)①“搅拌浸出”主要成分反应的化学方程式为______________ 。(已知:硫元素变成最高价,铁元素变成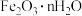 );
);
②铁元素没有以配合物离子存在的原因是__________________ 。
(4)常温下,“沉钴”步骤中,溶液中氨气分子浓度为 ,若要“沉钻”完全[
,若要“沉钻”完全[ 浓度为
浓度为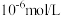 ],需调节
],需调节 至
至___________ ,“萃取”和“反萃取”的作用为________________ 。
 ,含少量
,含少量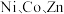 等元素)提取铜的工艺如下:
等元素)提取铜的工艺如下: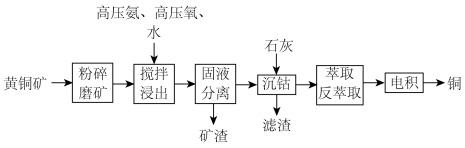
I.“固液分离”后溶液中主要离子为
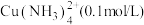 ,杂质离子为
,杂质离子为 、
、 、
、 等阳离子(浓度均为
等阳离子(浓度均为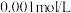 );“电积”时溶液中主要溶质为
);“电积”时溶液中主要溶质为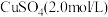 。
。Ⅱ.不稳定常数对
 ,不稳定常数
,不稳定常数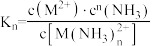
|
|
|
不稳定常数 |
| 0.2 |
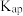
|
|
|
溶度积 |
|
|
(1)基态
 原子的价电子排布式为
原子的价电子排布式为 中氮原子的杂化方式为
中氮原子的杂化方式为(2)①浸出前“粉碎磨矿”的目的是
(3)①“搅拌浸出”主要成分反应的化学方程式为
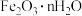 );
);②铁元素没有以配合物离子存在的原因是
(4)常温下,“沉钴”步骤中,溶液中氨气分子浓度为
 ,若要“沉钻”完全[
,若要“沉钻”完全[ 浓度为
浓度为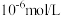 ],需调节
],需调节 至
至
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,该厂用上述废金属屑制取新型高效水处理剂Na2FeO4(高铁酸钠)等产品,过程如下:
I.向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
II.向I所得固体中加入过量稀H2SO4,充分反应后过滤;
III.向II所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
IV.……
(1)步骤I中Al与NaOH溶液的反应化学方程式为___________ ;另一种与NaOH溶液反应的氧化物是___________ ;该氧化物属于___________ (填“碱性”,“酸性”或“两性氧化物”)。
(2)步骤II所得的滤液中加入KSCN溶液无明显现象,表明滤液中不存在___________ (填离子符号);用离子方程式解释其可能的原因___________ ;取该硫酸亚铁滤液滴加NaOH溶液的现象是___________ 。
(3)步骤II所得硫酸亚铁滤液经进一步处理可制得Na2FeO4,流程如下:

该流程有关反应中属于氧化剂的有___________ 。
(4)步骤III获得CuSO4溶液的离子方程式为___________ 。
I.向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
II.向I所得固体中加入过量稀H2SO4,充分反应后过滤;
III.向II所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
IV.……
(1)步骤I中Al与NaOH溶液的反应化学方程式为
(2)步骤II所得的滤液中加入KSCN溶液无明显现象,表明滤液中不存在
(3)步骤II所得硫酸亚铁滤液经进一步处理可制得Na2FeO4,流程如下:

该流程有关反应中属于氧化剂的有
(4)步骤III获得CuSO4溶液的离子方程式为
您最近一年使用:0次
【推荐3】炼锌工艺产生大量废泥,主要含有金属锌、铜、镉(Cd),还有少量铁和微量砷。废泥资源化工艺如下:
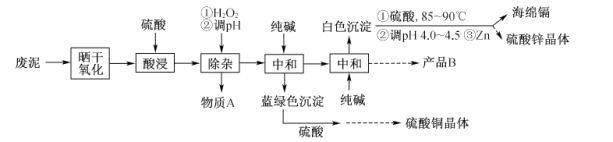
(1)废泥“晒干氧化”主要是把金属转化为盐,有关该盐下列说法正确的是___________(填编号)
(2)“除杂”过程中,发生的离子方程式是___________ ,H2O2需要分批加入,主要目的是___________ 。
(3)两次“中和”后,经过浓缩降温结晶等一系列物理过程,产品B为___________ 。
(4)加入Zn,得到的还原产物是___________ 。
(5)废泥资源化工艺得到4种产品,这样设计的目的是___________(填编号)。

(1)废泥“晒干氧化”主要是把金属转化为盐,有关该盐下列说法正确的是___________(填编号)
| A.硫酸盐 | B.碱式碳酸盐 | C.盐酸盐 | D.亚硫酸盐 |
(3)两次“中和”后,经过浓缩降温结晶等一系列物理过程,产品B为
(4)加入Zn,得到的还原产物是
(5)废泥资源化工艺得到4种产品,这样设计的目的是___________(填编号)。
| A.降低成本,提高效益 |
| B.充分利用废泥,使废泥资源化 |
| C.整个工艺原子利用率达到100% |
| D.增加反应速率,提高反应程度 |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】已知:A、B、C均为常见的单质或化合物,它们在一定条件下有如下关系:
A + H2O → B + C
(1)若A可作为呼吸面具和潜水艇中氧气的来源,则A与水反应的化学方程式为___________ 。
(2)若A为氧化物,B为强酸,则该反应的化学方程式为____________ ,3mol的A参加反应时转移的电子数为_____________ 。
(3)若A为单质,B、C均为酸,写出A与水反应的离子方程式:_________________ ;写出一种关于A的用途:___________________________ 。
(4)若C为氢气,则单质A可能是__________________ 。
A + H2O → B + C
(1)若A可作为呼吸面具和潜水艇中氧气的来源,则A与水反应的化学方程式为
(2)若A为氧化物,B为强酸,则该反应的化学方程式为
(3)若A为单质,B、C均为酸,写出A与水反应的离子方程式:
(4)若C为氢气,则单质A可能是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】有A、B、C、D、E、F、G、H、I九种物质,转化关系如下图所示(相关反应的某些产物在图中已略去).其中A为黑色粉末状固体物质,常用作氯酸钾分解制氧气的催化剂;D在C中燃烧,火焰呈苍白色;E与B接触有大量白烟产生;G为焰色反应呈黄色的强碱.

(1)写出下列物质的化学式:A___________ E__________ G___________ I__________
(2)写出A+B→C的化学方程式:______________ ;
(3)写出C+G→H+I+H2O的离子方程式:_______________ .

(1)写出下列物质的化学式:A
(2)写出A+B→C的化学方程式:
(3)写出C+G→H+I+H2O的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】甲同学向做过银镜反应的试管滴加0.1mol/L的Fe(NO3)3溶液(pH=2),发现银镜部分溶解,和大家一起分析原因:
甲同学认为:Fe3+具有氧化性,能够溶解单质Ag。
乙同学认为:Fe(NO3)3溶液显酸性,该条件下NO3-也能氧化单质Ag。
丙同学认为:Fe3+和NO3-均能把Ag氧化而溶解。
(1)生成银镜反应过程中银氨溶液发生_____________ (氧化、还原)反应。
(2)为得出正确结论,只需设计两个实验验证即可。
实验I:向溶解了银镜的Fe(NO3)3的溶液中加入____________ (填序号,①KSCN溶液、②K3[Fe(CN)6]溶液、③稀HCl),现象为___________ ,证明甲的结论正确。
实验Ⅱ:向附有银镜的试管中加入______________ 溶液,观察银镜是否溶解。
两个实验结果证明了丙同学的结论。
(3)丙同学又把5mLFeSO4溶液分成两份:第一份滴加2滴KSCN溶液无变化;第二份加入1mL0.1mol/LAgNO3溶液,出现白色沉淀,随后有黑色固体产生(经验证黑色固体为Ag颗粒),再取上层溶液滴加KSCN溶液变红。根据上述的实验情况,用离子方程式表示Fe3+、Fe2+、Ag+、Ag之间的反应关系_______________ 。
(4)丁同学改用如图实验装置做进一步探究:

①K刚闭合时,指针向左偏转,此时石墨作_________ ,(填“正极”或“负极。此过程氧化性:Fe3+_______ Ag+(填>或<)。
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,指针向右偏转。此过程氧化性:Fe3+_______ Ag+(填>或<)。
③由上述①②实验,得出的结论是:_______________________ 。
甲同学认为:Fe3+具有氧化性,能够溶解单质Ag。
乙同学认为:Fe(NO3)3溶液显酸性,该条件下NO3-也能氧化单质Ag。
丙同学认为:Fe3+和NO3-均能把Ag氧化而溶解。
(1)生成银镜反应过程中银氨溶液发生
(2)为得出正确结论,只需设计两个实验验证即可。
实验I:向溶解了银镜的Fe(NO3)3的溶液中加入
实验Ⅱ:向附有银镜的试管中加入
两个实验结果证明了丙同学的结论。
(3)丙同学又把5mLFeSO4溶液分成两份:第一份滴加2滴KSCN溶液无变化;第二份加入1mL0.1mol/LAgNO3溶液,出现白色沉淀,随后有黑色固体产生(经验证黑色固体为Ag颗粒),再取上层溶液滴加KSCN溶液变红。根据上述的实验情况,用离子方程式表示Fe3+、Fe2+、Ag+、Ag之间的反应关系
(4)丁同学改用如图实验装置做进一步探究:

①K刚闭合时,指针向左偏转,此时石墨作
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,指针向右偏转。此过程氧化性:Fe3+
③由上述①②实验,得出的结论是:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
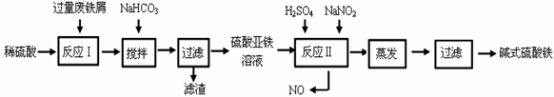
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH在 范围内,使溶液中的 离子沉淀。
(2)反应Ⅱ中加入NaNO2,反应的离子方程式为 。
(3)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2有5.6 L(标准状况),则相当于节约NaNO2的物质的量为 。
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,Fe(OH)2+可部分水解生成Fe2(OH)42+ 聚合离子,该水解反应的离子方程式为 。
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为 。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 3.4 | 完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH在 范围内,使溶液中的 离子沉淀。
(2)反应Ⅱ中加入NaNO2,反应的离子方程式为 。
(3)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2有5.6 L(标准状况),则相当于节约NaNO2的物质的量为 。
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,Fe(OH)2+可部分水解生成Fe2(OH)42+ 聚合离子,该水解反应的离子方程式为 。
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为 。
A.氯水 B.KSCN溶液 C.NaOH溶液 D.K3Fe(CN)6溶液
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐1】某兴趣小组对化合物X开展探究实验:
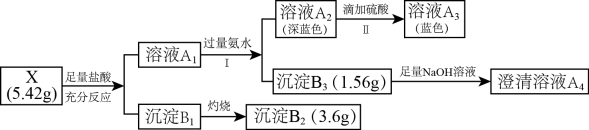
其中:化合物X有由4种元素组成;沉淀B2是工业生产玻璃的重要原料。
请回答:
(1)组成X的四种元素中除含O外,还有___________ (填元素符号)。
(2)在澄清溶液A4中通入过量CO2,产生沉淀的离子方程式为___________ 。
(3)步骤I中生成沉淀B3的离子方程式为___________ 。
(4)步骤II中溶液由深蓝色转变为蓝色的原因是___________ 。
(5)为进一步确定X的化学式,往溶液A1中通入足量的SO2,生成0.995g的白色沉淀(其中氯元素的质量分数为35.7%),在反应后的溶液中滴加BaCl2溶液,有白色沉淀生成。
①写出A1中通入SO2的离子反应方程式___________ 。
②确定X的化学式为___________ 。

其中:化合物X有由4种元素组成;沉淀B2是工业生产玻璃的重要原料。
请回答:
(1)组成X的四种元素中除含O外,还有
(2)在澄清溶液A4中通入过量CO2,产生沉淀的离子方程式为
(3)步骤I中生成沉淀B3的离子方程式为
(4)步骤II中溶液由深蓝色转变为蓝色的原因是
(5)为进一步确定X的化学式,往溶液A1中通入足量的SO2,生成0.995g的白色沉淀(其中氯元素的质量分数为35.7%),在反应后的溶液中滴加BaCl2溶液,有白色沉淀生成。
①写出A1中通入SO2的离子反应方程式
②确定X的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】亚铁氰化钾晶体化学式为:KxFey(CN)z•nH2O,俗称黄血盐,常用作食品抗结剂。一种用NaCN(N显-3价)废液制取黄血盐的主要工艺流程:

(1)实验室用绿矾固体配制FeSO4溶液时,应先________ ,再用蒸馏水稀释。
(2)“转化罐”中生成黄血盐晶体的反应类型为________ 。
(3)采用密封气流干燥取代在通风橱内干燥的原因是________ 。
(4)黄血盐的化学式可通过下列实验测定:
①准确称取4.220g样品加入水中充分溶解,将所得溶液转移至容量瓶配制成100.00mL溶液A。
②量取25.00mL溶液A,用2.000mol•L-1KMnO4溶液滴定,达到滴定终点时,共消耗KMnO4溶液15.25mL。反应如下(未配平):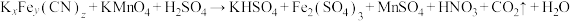 ③向②所得溶液加入Mn2+离子交换树脂,将Mn2+完全吸附后再滴加足量NaOH溶液,过滤、洗涤、灼烧,最终得固体0.2g。
③向②所得溶液加入Mn2+离子交换树脂,将Mn2+完全吸附后再滴加足量NaOH溶液,过滤、洗涤、灼烧,最终得固体0.2g。
通过计算确定样品的化学式(写出计算过程)。______________

(1)实验室用绿矾固体配制FeSO4溶液时,应先
(2)“转化罐”中生成黄血盐晶体的反应类型为
(3)采用密封气流干燥取代在通风橱内干燥的原因是
(4)黄血盐的化学式可通过下列实验测定:
①准确称取4.220g样品加入水中充分溶解,将所得溶液转移至容量瓶配制成100.00mL溶液A。
②量取25.00mL溶液A,用2.000mol•L-1KMnO4溶液滴定,达到滴定终点时,共消耗KMnO4溶液15.25mL。反应如下(未配平):
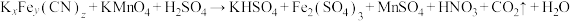 ③向②所得溶液加入Mn2+离子交换树脂,将Mn2+完全吸附后再滴加足量NaOH溶液,过滤、洗涤、灼烧,最终得固体0.2g。
③向②所得溶液加入Mn2+离子交换树脂,将Mn2+完全吸附后再滴加足量NaOH溶液,过滤、洗涤、灼烧,最终得固体0.2g。通过计算确定样品的化学式(写出计算过程)。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】根据题意,回答下列问题:
Ⅰ.某小组同学欲探究 催化氧化反应,按如图装置进行实验。
催化氧化反应,按如图装置进行实验。

A、B装置可选药品:浓氨水、 、蒸馏水、氧化钙、
、蒸馏水、氧化钙、 。
。
(1)B装置中烧瓶内固体名称为___________ 。
(2) 催化氧化的化学方程式是
催化氧化的化学方程式是___________ 。
(3)甲乙两同学分别按上述装置进行实验,一段时间后,装置G中溶液都变成蓝色。甲观察到装置F中有红棕色气体;乙观察到装置F中只有白烟生成,白烟的成分是(写化学式)___________ 。
Ⅱ.焦亚硫酸钠( )是一种食品抗氧化剂,易溶于水。
)是一种食品抗氧化剂,易溶于水。
(4)焦亚硫酸钠( )中硫元素的化合价为
)中硫元素的化合价为___________ 。
(5)向某些饮料中添加少量焦亚硫酸钠( ),可降低饮料中溶解氧的含量,发生反应的离子方程式为
),可降低饮料中溶解氧的含量,发生反应的离子方程式为___________ 。
(6)向饱和碳酸钠溶液中通入过量 可制得焦亚硫酸钠,发生反应的化学方程式为
可制得焦亚硫酸钠,发生反应的化学方程式为___________ 。
Ⅲ.硫代硫酸钠( )常用来测定溶液中的含碘量。
)常用来测定溶液中的含碘量。
(7)为测定某碘水中 的浓度(假设碘水中的碘元素均以碘单质形式存在),取该碘水200.0mL,滴加0.01
的浓度(假设碘水中的碘元素均以碘单质形式存在),取该碘水200.0mL,滴加0.01 硫代硫酸钠溶液,发生反应:
硫代硫酸钠溶液,发生反应: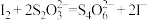 ,恰好完全反应时,硫代硫酸钠溶液用量为20.0mL,则该碘水中
,恰好完全反应时,硫代硫酸钠溶液用量为20.0mL,则该碘水中 的浓度为
的浓度为___________  。
。
Ⅰ.某小组同学欲探究
 催化氧化反应,按如图装置进行实验。
催化氧化反应,按如图装置进行实验。
A、B装置可选药品:浓氨水、
 、蒸馏水、氧化钙、
、蒸馏水、氧化钙、 。
。(1)B装置中烧瓶内固体名称为
(2)
 催化氧化的化学方程式是
催化氧化的化学方程式是(3)甲乙两同学分别按上述装置进行实验,一段时间后,装置G中溶液都变成蓝色。甲观察到装置F中有红棕色气体;乙观察到装置F中只有白烟生成,白烟的成分是(写化学式)
Ⅱ.焦亚硫酸钠(
 )是一种食品抗氧化剂,易溶于水。
)是一种食品抗氧化剂,易溶于水。(4)焦亚硫酸钠(
 )中硫元素的化合价为
)中硫元素的化合价为(5)向某些饮料中添加少量焦亚硫酸钠(
 ),可降低饮料中溶解氧的含量,发生反应的离子方程式为
),可降低饮料中溶解氧的含量,发生反应的离子方程式为(6)向饱和碳酸钠溶液中通入过量
 可制得焦亚硫酸钠,发生反应的化学方程式为
可制得焦亚硫酸钠,发生反应的化学方程式为Ⅲ.硫代硫酸钠(
 )常用来测定溶液中的含碘量。
)常用来测定溶液中的含碘量。(7)为测定某碘水中
 的浓度(假设碘水中的碘元素均以碘单质形式存在),取该碘水200.0mL,滴加0.01
的浓度(假设碘水中的碘元素均以碘单质形式存在),取该碘水200.0mL,滴加0.01 硫代硫酸钠溶液,发生反应:
硫代硫酸钠溶液,发生反应: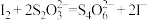 ,恰好完全反应时,硫代硫酸钠溶液用量为20.0mL,则该碘水中
,恰好完全反应时,硫代硫酸钠溶液用量为20.0mL,则该碘水中 的浓度为
的浓度为 。
。
您最近一年使用:0次



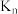 (常温)
(常温)