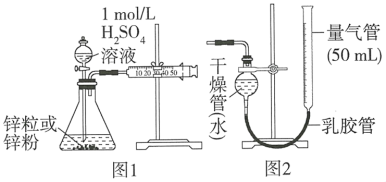
某研究性学习小组为了研究影响化学反应速率的因素,设计如下方案:
已知:反应的方程式(未配平):KMnO4 + H2C2O4 + H2SO4 —— K2SO4 + MnSO4 + CO2↑+ H2O
(1)实验记时方法是从溶液混合开始记时,至_______________ 时记时结束。
(2)实验I和II研究浓度对反应速率的影响,实验I和III研究温度对反应速率的影响。请在上表空格中填入合理的实验数据。
(3)从实验数据分析,实验I和IV研究________ 对反应的影响。
(4)请配平上面的化学方程式:
_ KMnO4 +__ H2C2O4 + __ H2SO4=_ K2SO4 + __ MnSO4 + __ CO2↑+ __ H2O
| 实验编号 | 0.01mol·L-1 酸性KMnO4溶液 | 0.1mol·L-1 H2C2O4溶液 | 水 | 1mol·L-1 MnSO4溶液 | 反应温度 /℃ | 反应时间 |
| I | 2mL | 2mL | 0 | 0 | 20 | 125 |
| II | 1mL | 0 | 20 | 320 | ||
| III | 0 | 50 | 30 | |||
| IV | 2mL | 2mL | 0 | 2滴 | 20 | 10 |
(1)实验记时方法是从溶液混合开始记时,至
(2)实验I和II研究浓度对反应速率的影响,实验I和III研究温度对反应速率的影响。请在上表空格中填入合理的实验数据。
(3)从实验数据分析,实验I和IV研究
(4)请配平上面的化学方程式:
14-15高二上·浙江杭州·期中 查看更多[3]
福建省泉州第十六中学2020-2021学年高二上学期期中考试化学(选考班)试题福建省惠安惠南中学2018-2019学年高二上学期期中考试化学试题(已下线)2014秋浙江省杭州地区六校高二上学期期中考试化学试卷
更新时间:2016-12-09 06:51:22
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】为探究影响化学反应速率的因素与化学反应限度的存在,某中学实验小组进行以下两组实验。
(Ⅰ)探究影响化学反应速率的因素,结合表中信息,回答问题:
(1)探究温度对反应速率的影响,应选择的实验组号是_______ ;实验组①②对比的实验目的是_______ 。
(2)实验过程中,需要观察和记录_______ ,比较化学反应速率的快慢。
(3)上述四组实验中,反应速率最慢的是_______ 。
(Ⅱ)验证铁离子与碘离子反应存在限度,结合相关实验,回答问题:
药品选择: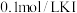 溶液、
溶液、 溶液、淀粉溶液、试剂N
溶液、淀粉溶液、试剂N
实验步骤:①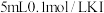 溶液中滴入5~6滴
溶液中滴入5~6滴 溶液,充分反应后,将所得溶液分成甲、乙两等份;
溶液,充分反应后,将所得溶液分成甲、乙两等份;
②向甲中滴加2滴淀粉,充分振荡;
③向乙中滴加试剂N。回答下列问题:
(4)步骤②甲试管中出现_______ 现象,证明反应有 的生成。
的生成。
(5)若实验①中的反应存在限度,可用试剂N的溶液检验 ,则试剂N是
,则试剂N是_______ ;乙试管中的现象是_______ 。
(6)写出实验步骤①的化学方程式_______ 。
(Ⅰ)探究影响化学反应速率的因素,结合表中信息,回答问题:
| 组号 | 反应温度/℃ | 参加反应的物质 | ||||
 |  |  | ||||
 | 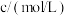 |  | 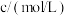 |  | ||
| ① | 10 | 2 | 0.1 | 2 | 0.1 | 2 |
| ② | 10 | 2 | 0.1 | 2 | 0.1 | 4 |
| ③ | 30 | 2 | 0.1 | 2 | 0.1 | 4 |
| ④ | 30 | 2 | 0.2 | 2 | 0.2 | 4 |
(2)实验过程中,需要观察和记录
(3)上述四组实验中,反应速率最慢的是
(Ⅱ)验证铁离子与碘离子反应存在限度,结合相关实验,回答问题:
药品选择:
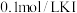 溶液、
溶液、 溶液、淀粉溶液、试剂N
溶液、淀粉溶液、试剂N实验步骤:①
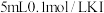 溶液中滴入5~6滴
溶液中滴入5~6滴 溶液,充分反应后,将所得溶液分成甲、乙两等份;
溶液,充分反应后,将所得溶液分成甲、乙两等份;②向甲中滴加2滴淀粉,充分振荡;
③向乙中滴加试剂N。回答下列问题:
(4)步骤②甲试管中出现
 的生成。
的生成。(5)若实验①中的反应存在限度,可用试剂N的溶液检验
 ,则试剂N是
,则试剂N是(6)写出实验步骤①的化学方程式
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某实验探究小组用酸性 溶液与
溶液与 溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性
溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性 溶液的浓度可选择0.010mol/L、0.001 mol/L,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验酸性
溶液的浓度可选择0.010mol/L、0.001 mol/L,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验酸性 溶液的用量均为4mL,
溶液的用量均为4mL, 溶液(0.100 mol/L)的用量均为2mL。已知
溶液(0.100 mol/L)的用量均为2mL。已知 。
。
(1)写出反应的离子方程式:___________ 。
(2)已知部分实验数据如下:
实验目的:
a.实验①和②探究___________ 对该反应速率的影响;
b.实验①和③探究___________ 对该反应速率的影响;
c.实验①和④探究催化剂对该反应速率的影响,则实验④选择温度___________ K,催化剂用量___________ g,酸性 溶液的浓度
溶液的浓度___________ mol/L。该反应的催化剂应选择___________ (填写“ “或“
“或“ ”),简述选择的理由:
”),简述选择的理由:___________ 。
 溶液与
溶液与 溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性
溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性 溶液的浓度可选择0.010mol/L、0.001 mol/L,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验酸性
溶液的浓度可选择0.010mol/L、0.001 mol/L,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验酸性 溶液的用量均为4mL,
溶液的用量均为4mL, 溶液(0.100 mol/L)的用量均为2mL。已知
溶液(0.100 mol/L)的用量均为2mL。已知 。
。(1)写出反应的离子方程式:
(2)已知部分实验数据如下:
| 实验编号 | T/K | 催化剂的用量/g | 酸性 溶液的浓度/( mol/L) 溶液的浓度/( mol/L) |
| ① | 298 | 0.5 | 0.010 |
| ② | 298 | 0.5 | 0.001 |
| ③ | 323 | 0.5 | 0.010 |
| ④ |
a.实验①和②探究
b.实验①和③探究
c.实验①和④探究催化剂对该反应速率的影响,则实验④选择温度
 溶液的浓度
溶液的浓度 “或“
“或“ ”),简述选择的理由:
”),简述选择的理由:
您最近半年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】如图是闪锌矿(主要成分是ZnS,含有少量FeS)制备ZnSO4·7H2O的一种工艺流程:闪锌矿粉→溶浸→除铁→结晶→ZnSO4∙7H2O。已知:相关金属离子浓度为0.1mol/L时形成氢氧化物沉淀的pH范围如表:
(1)闪锌矿在溶浸之前会将其粉碎,其目的是_____________ 。
(2)溶浸过程使用过量的Fe2(SO4)3溶液和H2SO4浸取矿粉,发生的主要反应是:ZnS+2Fe3+=Zn2++2Fe2++S。
①浸出液中含有的阳离子包括Zn2+、Fe2+、_____________ 。
②若改用CuSO4溶液浸取,发生复分解反应,也能达到浸出锌的目的,写出离子方程式_____________ 。
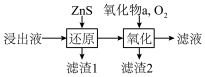
(3)工业除铁过程需要控制沉淀速率,因此分为还原和氧化两步先后进行,如图。还原过程将部分Fe3+转化为Fe2+,得到pH小于1.5的溶液。氧化过程向溶液中先加入氧化物a,再通入O2。下列说法正确的是_____________ (填序号)。
A. 氧化物a可以是ZnO
B. 滤渣2的主要成分是Fe(OH)2
C. 加入ZnS的量和通入O2的速率都可以控制溶液中的c(Fe3+)
| 金属离子 | Fe3+ | Fe2+ | Zn2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 |
(2)溶浸过程使用过量的Fe2(SO4)3溶液和H2SO4浸取矿粉,发生的主要反应是:ZnS+2Fe3+=Zn2++2Fe2++S。
①浸出液中含有的阳离子包括Zn2+、Fe2+、
②若改用CuSO4溶液浸取,发生复分解反应,也能达到浸出锌的目的,写出离子方程式
(3)工业除铁过程需要控制沉淀速率,因此分为还原和氧化两步先后进行,如图。还原过程将部分Fe3+转化为Fe2+,得到pH小于1.5的溶液。氧化过程向溶液中先加入氧化物a,再通入O2。下列说法正确的是

A. 氧化物a可以是ZnO
B. 滤渣2的主要成分是Fe(OH)2
C. 加入ZnS的量和通入O2的速率都可以控制溶液中的c(Fe3+)
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】广义的化学反应速率可以用参加化学反应的任一种物质“在单位时间内某一可测的物理量的变化量”来表示,即V(A) = ,ΔX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。
,ΔX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。

可选用试剂及规格:纯锌、粗锌(含铜杂质)、1mol/L 稀硫酸、2mol/L 稀硫酸,
反应温度:250C 、350C
(1)请写出锌和硫酸反应的离子方程式________________________________________
(2)为表达锌和硫酸反应快慢,该学习小组设计了如下表格,请填充表格丁、戊、己三处。
(3)该学习小组选用0.1 mol Zn和200 mL 1mol/L 稀硫酸(硫酸过量)在250C反应进行研究,用秒表计时,至锌块完全溶解且溶液中不再有气泡放出时,记录反应时间为5分钟,该反应速率V(H+) =____________
(4)该小组对“影响反应速率的因素”进行了分析,设计如下系列实验,庚辛壬癸四处空白。
 ,ΔX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。
,ΔX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。
可选用试剂及规格:纯锌、粗锌(含铜杂质)、1mol/L 稀硫酸、2mol/L 稀硫酸,
反应温度:250C 、350C
(1)请写出锌和硫酸反应的离子方程式
(2)为表达锌和硫酸反应快慢,该学习小组设计了如下表格,请填充表格丁、戊、己三处。
| 编号 | 反应速率表达式的定义 | 反应速率表达式 | 反应速率单位 |
| ① | 单位时间内H+浓度的变化量 | V(H+) = | mol / (L.min) |
| ② | 丁 | 戊 | 己 |
| ③ | 单位时间内生成H2标况下的体积 | V(H2) =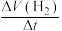 | L / min |
(4)该小组对“影响反应速率的因素”进行了分析,设计如下系列实验,庚辛壬癸四处空白。
| 编号 | 锌的形状 | 锌的规格 | 硫酸的浓度 | 反应温度 | 实验设计的目的 |
| ① | 块状 | 纯锌 | 1mol/L | 250C | 实验①和②研究的目的是庚 实验②和③研究硫酸浓度对反应速率影响; 实验③和④研究锌的规格对反应速率影响; 实验④和⑤研究的目的是癸 |
| ② | 颗粒状 | 纯锌 | 1mol/L | 250C | |
| ③ | 颗粒状 | 纯锌 | 辛 | 250C | |
| ④ | 颗粒状 | 壬 | 2mol/L | 250C | |
| ⑤ | 颗粒状 | 粗锌 | 2mol/L | 350C | |
| …… | |||||
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某研究小组为了验证反应物浓度对反应速率的影响,选用硫酸酸化的高锰酸钾溶液与草酸( )溶液在室温下进行反应。实验中所用的草酸溶液为稀溶液,该反应的化学方程式为
)溶液在室温下进行反应。实验中所用的草酸溶液为稀溶液,该反应的化学方程式为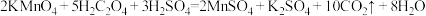 。
。
(1)该小组进行了实验Ⅰ,数据如下:
一般来说,其他条件相同时,增大反应物浓度,反应速率___________ (填“增大”或“减小”),但分析该实验数据,得到的结论是:在当前实验条件下,___________ 。
(2)该小组欲探究出现上述异常现象的原因,在实验Ⅰ的基础上,只改变草酸溶液浓度进行了实验Ⅱ,获得实验数据并绘制如下曲线图。

该小组为探究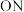 段曲线变化趋势的原因,进行了实验Ⅲ,所得数据如下。
段曲线变化趋势的原因,进行了实验Ⅲ,所得数据如下。
该小组进行实验Ⅲ的目的是___________ 。
(3)综合实验Ⅰ、Ⅱ、Ⅲ,推测造成曲线 变化趋势的原因有
变化趋势的原因有___________ (填序号)。
a.当草酸浓度较小时, 起主要作用,草酸浓度越大,反应速率越小
起主要作用,草酸浓度越大,反应速率越小
b.当草酸浓度较小时, 起主要作用,草酸浓度越大,反应速率越大
起主要作用,草酸浓度越大,反应速率越大
c.当草酸浓度较大时, 起主要作用,草酸浓度越大,反应速率越小
起主要作用,草酸浓度越大,反应速率越小
d.当草酸浓度较大时, 起主要作用,草酸浓度越大,反应速率越大
起主要作用,草酸浓度越大,反应速率越大
 )溶液在室温下进行反应。实验中所用的草酸溶液为稀溶液,该反应的化学方程式为
)溶液在室温下进行反应。实验中所用的草酸溶液为稀溶液,该反应的化学方程式为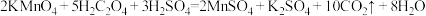 。
。(1)该小组进行了实验Ⅰ,数据如下:
 溶液 溶液 |  溶液 溶液 |  溶液 溶液 | 褪色时间(分:秒) |
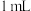 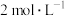 | 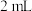  | 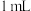  |  |
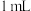 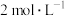 | 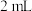  | 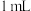 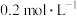 |  |
(2)该小组欲探究出现上述异常现象的原因,在实验Ⅰ的基础上,只改变草酸溶液浓度进行了实验Ⅱ,获得实验数据并绘制如下曲线图。

该小组为探究
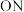 段曲线变化趋势的原因,进行了实验Ⅲ,所得数据如下。
段曲线变化趋势的原因,进行了实验Ⅲ,所得数据如下。 溶液 溶液 |  固体 固体 |  溶液 溶液 |  溶液 溶液 | 褪色时间(分:秒) |
 |  |  |  |  |
 |  |  |  | 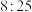 |
 |  |  |  | 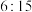 |
 | 0 |  |  |  |
(3)综合实验Ⅰ、Ⅱ、Ⅲ,推测造成曲线
 变化趋势的原因有
变化趋势的原因有a.当草酸浓度较小时,
 起主要作用,草酸浓度越大,反应速率越小
起主要作用,草酸浓度越大,反应速率越小b.当草酸浓度较小时,
 起主要作用,草酸浓度越大,反应速率越大
起主要作用,草酸浓度越大,反应速率越大c.当草酸浓度较大时,
 起主要作用,草酸浓度越大,反应速率越小
起主要作用,草酸浓度越大,反应速率越小d.当草酸浓度较大时,
 起主要作用,草酸浓度越大,反应速率越大
起主要作用,草酸浓度越大,反应速率越大
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某同学进行了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如下(见表格),请结合表中信息,回答有关问题:
(1)该反应的化学方程式_______________ 。
(2)根据你所掌握的知识判断,在上述实验中,反应速率最快的可能是______ (填实验序号)。
(3)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
i:能说明温度对该反应速率影响的组合是_____ (填实验序号);
ii:①和②、①和③的组合比较,所研究的问题是__________ 。
(4)教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:________________ 。
实验序号 | 反应温度/℃ | 参加反应的物质 | ||||
Na2S2O3 | H2SO4 | H2O | ||||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
① | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
② | 20 | 5 | 0.1 | 10 | 0.1 | 5 |
③ | 20 | 10 | 0.1 | 5 | 0.1 | 5 |
④ | 40 | 5 | 0.1 | 10 | 0.1 | 5 |
(2)根据你所掌握的知识判断,在上述实验中,反应速率最快的可能是
(3)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
i:能说明温度对该反应速率影响的组合是
ii:①和②、①和③的组合比较,所研究的问题是
(4)教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某探究性学习小组用相同质量的镁和锌与相同浓度足量的稀盐酸反应得到实验数据如表所示:
(1)实验Ⅰ和Ⅱ表明______________ ,化学反应速率越大。
(2)实验Ⅱ和IV表明_____________ ,化学反应速率越大。
(3)实验Ⅱ和Ⅲ为验证固体的表面积对反应速率的影响,则a=________ 。
(4)除本实验探究的因素外,影响化学反应速率的因素还有很多,试写出两个因素_____ 、_____ 。
| 实验编号 | 金属 | 形态 | 反应温度/℃ | 收集 100 mL 氢气所需时间/s |
| Ⅰ | 锌 | 薄片 | 15 | 200 |
| Ⅱ | 锌 | 薄片 | 25 | 90 |
| Ⅲ | 锌 | 粉末 | a | 10 |
| IV | 镁 | 薄片 | 25 | 42 |
(1)实验Ⅰ和Ⅱ表明
(2)实验Ⅱ和IV表明
(3)实验Ⅱ和Ⅲ为验证固体的表面积对反应速率的影响,则a=
(4)除本实验探究的因素外,影响化学反应速率的因素还有很多,试写出两个因素
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。实验药品:铜、铁、镁、0.5 mol • L-1H2SO4溶液、2 mol • L-1 H2SO4溶液。甲同学研究的实验报告如下表∶
(1) 甲同学表中实验步骤②为______________________ 。
(2) 甲同学的实验目的是__________________________ 。
要得出正确的实验结论,还需要控制的实验条件是_____________ 。
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行实验∶
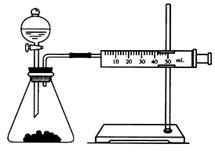
(3)乙同学在实验中应该测定的数据是_________________ 。
(4)乙同学完成该实验应选用的实验药品是________________ 。
| 实验步骤 | 现象 | 结论 |
| 分别取等体积的2 mol • L-1 的硫酸溶液于三支试管中 ②______________________ | 反应速率∶ 镁>铁,铜不反应 | 金属的性质越活泼,反应速率越快 |
(2) 甲同学的实验目的是
要得出正确的实验结论,还需要控制的实验条件是
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行实验∶

(3)乙同学在实验中应该测定的数据是
(4)乙同学完成该实验应选用的实验药品是
您最近半年使用:0次