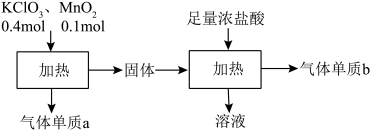
在实验室中,常用KMnO4代替MnO2与浓盐酸反应制取氯气,其反应的化学方程式为 2KMnO4+16HCl(浓)= 2MnCl2+5Cl2↑+2KCl+8H2O,下列叙述中正确的是( )
| A.反应中KMnO4被氧化 |
| B.氧化产物与还原产物的物质的量之比为5﹕2 |
| C.每生成0.5 mol Cl2时,反应中转移的电子为2 mol |
| D.氧化剂和还原剂的比例是1:8 |
更新时间:2016-12-09 07:02:58
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】加热硅与Ca(OH)2、NaOH的混合粉末可获得氢气Si+Ca(OH)2+2NaOH Na2SiO3+CaO+2H2↑,下列说法正确的是
Na2SiO3+CaO+2H2↑,下列说法正确的是
 Na2SiO3+CaO+2H2↑,下列说法正确的是
Na2SiO3+CaO+2H2↑,下列说法正确的是| A.Na2SiO3是还原产物 | B.可推知该反应为吸热反应 |
| C.氧化剂与还原剂的物质的量之比为2∶1 | D.该反应为置换反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中正确的有
| A.溶于水后能电离出氢离子的化合物一定是酸 |
| B.强氧化剂与强还原剂混合一定发生氧化还原反应 |
| C.两种盐反应一定生成两种新盐 |
| D.HCl既有氧化性又有还原性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列变化中,必须加入还原剂才能实现的是
A. | B. |
C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式书写不正确的是
A.AlCl3溶液与烧碱溶液反应,当 n(OH-)∶n(Al3+)=7∶2 时,2Al3++7OH-=Al(OH)3↓+ +2H2O +2H2O |
| B.CuCl2溶液与 NaHS溶液反应,当 n(CuCl2)∶n(NaHS)=1∶2时,Cu2++2HS-=CuS↓+H2S↑ |
| C.Cl2与FeBr2溶液反应,当 n(Cl2)∶n(FeBr2)=1∶1 时,2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
D.用NaOH溶液吸收工业废气中的NO2∶2NO2+2OH-= + + +H2O +H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】从《化学反应原理》中学习到碱性锌锰电池的工作原理:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,其中的电解质溶液是KOH溶液。我校课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnxZn(1-x)Fe2O4,其工艺流程如下图所示:

下列说法中不正确 的是

下列说法中
| A.已知MnxZn(1-x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为+3价 |
| B.“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,则该反应的离子方程式:MnO(OH)+Fe2++3H+=Mn2++Fe3++2H2O。 |
| C.在“氧化”工序中,加入双氧水的目的是把Fe2+氧化为Fe3+ |
D.用氨水“调pH”后,从滤液C中还可分离出一种氮肥(NH4)2SO4,该氮肥的溶液中离子浓度满足关系为:c( )+c(H+)=c( )+c(H+)=c( )+c(OH-) )+c(OH-) |
您最近一年使用:0次
【推荐1】已知:还原性 >I-,氧化性
>I-,氧化性 >I2。在含3molNaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是( )
>I2。在含3molNaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是( )

 >I-,氧化性
>I-,氧化性 >I2。在含3molNaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是( )
>I2。在含3molNaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是( )
A.0~a段发生反应:3 + + =3 =3 +I- +3H+ +I- +3H+ |
| B.b~c段反应:氧化产物的物质的量是0.5mol |
| C.当溶液中I-与I2的物质的量之比为5:1时,加入的KIO3为1.lmol |
| D.a-b段共消耗NaHSO3的物质的量为1.8mol |
您最近一年使用:0次
【推荐2】2020年新冠肺炎疫情在全球肆虐,84消毒液能有效杀死病毒,生活中常用其来消毒。84消毒液(主要成分是NaClO)与洁厕灵(主要成分是浓盐酸)不能混用,二者混合会反应产生一种黄绿色有毒气体,非常危险。下列说法正确的是
A.氧化性: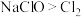 |
| B.NaClO发生了氧化反应 |
| C.反应中氧化剂和还原剂的化学计量数之比为1:2 |
| D.NaCl为还原产物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】以氧化铁渣(主要含Fe3O4和Fe2O3)制取氧化铁红的流程如下:

已知还原焙烧后氧化铁渣转化为FeO。下列说法不正确 的是

已知还原焙烧后氧化铁渣转化为FeO。下列说法
A.还原焙烧时Fe3O4发生反应的化学方程式为2Fe3O4+C 6FeO+CO2 6FeO+CO2 |
| B.酸浸时硫酸适当过量可以抑制金属离子的水解 |
C.滤液中主要存在的离子是:NH 、H+、HCO 、H+、HCO 、SO 、SO |
| D.煅烧时每生成1 mol Fe2O3,反应转移的电子数是2 mol |
您最近一年使用:0次
【推荐2】工业上常用浓氨水检查氯气管道,其反应为:8NH3+3Cl2= 6NH4Cl+N2,利用该反应中产生白烟这一现象来判断管道是否漏气,下列关于该反应的说法不正确的是
| A.氧化剂是Cl2 |
| B.氧化剂与还原剂的物质的量之比为3:8 |
| C.每生成1 mol N2,转移6 mol电子 |
| D.该条件下Cl2的氧化性强于N2 |
您最近一年使用:0次

 六种微粒,其中
六种微粒,其中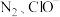 的数目随时间变化的曲线如图所示,下列说法不正确的是
的数目随时间变化的曲线如图所示,下列说法不正确的是
 为氧化剂
为氧化剂 被氧化成
被氧化成