一定温度下,A、B两瓶乙酸的浓度分别是1 mol/L和0.1 mol/L,则A、B两瓶乙酸溶液中[ H+ ]之比 10(填“<”、“>”或“=”),并简述理由 。
更新时间:2016-12-09 07:05:33
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐2】有一学生在实验室测某溶液的pH,实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作________ (填“正确”或“错误”),该操作是否一定有误差?并说明原因_______________________ 。
(2)若用此方法分别测定c(OH-)相等的氢氧化钠溶液和氨水的pH,误差较大的是_______ ,原因是__________________________ 。
(3)只从下列试剂中选择实验所需的试剂,你能否区分0.1mol∙L-1硫酸溶液和0.01mol∙L-1硫酸溶液?___________ ,简述操作过程:___________________________ 。
试剂:A.紫色石蕊试液 B.酚酞试液 C.甲基橙溶液 D.蒸馏水 E.氯化钡溶液 F.pH试纸
(1)该学生的操作
(2)若用此方法分别测定c(OH-)相等的氢氧化钠溶液和氨水的pH,误差较大的是
(3)只从下列试剂中选择实验所需的试剂,你能否区分0.1mol∙L-1硫酸溶液和0.01mol∙L-1硫酸溶液?
试剂:A.紫色石蕊试液 B.酚酞试液 C.甲基橙溶液 D.蒸馏水 E.氯化钡溶液 F.pH试纸
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】化学知识在生产和生活中处处都有体现,请用化学知识解释。
(1)冰箱能够在一定时间内保鲜食物,原因是_____ 。
(2)乳酸饮料(含乳酸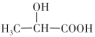 )显酸性的原因是
)显酸性的原因是_____ (用电离方程式表示)。
(3)工业上合成氨气时总是及时分离出反应器中的氨气,这样做的原因是_____ 。
(4)燃气灶具进风口通入的空气总是适当过量,这是为了_____ 。
(5)接近沸腾的纯净水pH<7,原因是_____ 。
(1)冰箱能够在一定时间内保鲜食物,原因是
(2)乳酸饮料(含乳酸
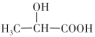 )显酸性的原因是
)显酸性的原因是(3)工业上合成氨气时总是及时分离出反应器中的氨气,这样做的原因是
(4)燃气灶具进风口通入的空气总是适当过量,这是为了
(5)接近沸腾的纯净水pH<7,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】Ⅰ.以下是生产、生活中常见的物质。按要求回答下列问题。
①冰醋酸;② ;③NaOH;④盐酸;⑤
;③NaOH;④盐酸;⑤ ;⑥熔融
;⑥熔融 ;⑦石墨;⑧酒精;⑨
;⑦石墨;⑧酒精;⑨ ;⑩
;⑩ 。
。
(1)属于强电解质的有_______ ,属于非电解质的有_______ 。(用序号填空)
(2)写出⑤溶液的电离方程式:_______ 。
(3)常温下, 的①溶液和
的①溶液和 的④溶液,加水稀释100倍,pH较大的是
的④溶液,加水稀释100倍,pH较大的是_______ 。(用序号填空)
(4)等体积的0.1 mol/L①溶液与0.1 mol/L④溶液分别与等浓度的氢氧化钠反应至中性,消耗的NaOH溶液的体积依次为 和
和 ,则
,则
_______  (填“>”、“<”或者“=”)。
(填“>”、“<”或者“=”)。
Ⅱ.已知,常温下几种酸的电离平衡常数如表:
(5)常温下,0.1 mol/L的HCN溶液中, 约为
约为_______ 。
(6)根据电离平衡常数判断,以下反应不能自发进行的是_______。
①冰醋酸;②
 ;③NaOH;④盐酸;⑤
;③NaOH;④盐酸;⑤ ;⑥熔融
;⑥熔融 ;⑦石墨;⑧酒精;⑨
;⑦石墨;⑧酒精;⑨ ;⑩
;⑩ 。
。(1)属于强电解质的有
(2)写出⑤溶液的电离方程式:
(3)常温下,
 的①溶液和
的①溶液和 的④溶液,加水稀释100倍,pH较大的是
的④溶液,加水稀释100倍,pH较大的是(4)等体积的0.1 mol/L①溶液与0.1 mol/L④溶液分别与等浓度的氢氧化钠反应至中性,消耗的NaOH溶液的体积依次为
 和
和 ,则
,则
 (填“>”、“<”或者“=”)。
(填“>”、“<”或者“=”)。Ⅱ.已知,常温下几种酸的电离平衡常数如表:
| 化学式 | HCOOH | HCN |  |
| 电离平衡常数 | 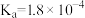 | 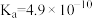 |   |
 约为
约为(6)根据电离平衡常数判断,以下反应不能自发进行的是_______。
A. |
B.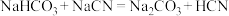 |
C.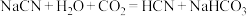 |
D. |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】25 ℃时,部分物质的电离常数如下表所示:
请回答下列问题:
(1)若把CH3COOH、H2C2O4、HC2O4-、H2S、HS- 都看作是酸,其中酸性最弱的是________ 。
(2)CH3COOH、H2C2O4、H2S的酸性由强到弱的顺序为_____________________ 。
(3)NaHS溶液与NaHC2O4溶液反应的离子方程式为_______________ 。
(4)0.1 mol·L-1H2S溶液中c(H+)=________ mol·L-1。
| 化学式 | CH3COOH | H2C2O4 | H2S |
| 电离常数 | 1.8×10-5 | Ka1=5.4×10-2 Ka2=5.4×10-5 | Ka1=1.0×10-7 Ka2=7.1×10-15 |
请回答下列问题:
(1)若把CH3COOH、H2C2O4、HC2O4-、H2S、HS- 都看作是酸,其中酸性最弱的是
(2)CH3COOH、H2C2O4、H2S的酸性由强到弱的顺序为
(3)NaHS溶液与NaHC2O4溶液反应的离子方程式为
(4)0.1 mol·L-1H2S溶液中c(H+)=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】水溶液是生命体赖以生存的环境,许多化学反应都是在水溶液中进行的。
I.25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)室温下,关于 的
的 溶液,下列分析正确的是
溶液,下列分析正确的是
(2)物质的量浓度均为0.1 的六种溶液①
的六种溶液①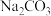 ②
② ③NaClO④
③NaClO④ ⑤
⑤ ⑥
⑥ ,pH由小到大的顺序
,pH由小到大的顺序___________ (填序号)。
(3)向次氯酸钠溶液通入少量 发生反应的离子方程式
发生反应的离子方程式___________ 。
(4)碳酸氢铵溶液显___________ (填“酸”、“中”或“碱”)性。
(5)向a 的
的 溶液加入等体积的未知浓度的稀盐酸,溶液恰好呈中性,则所加稀盐酸的物质的量浓度
溶液加入等体积的未知浓度的稀盐酸,溶液恰好呈中性,则所加稀盐酸的物质的量浓度___________  (用含a的式子表示)。
(用含a的式子表示)。
II. 是一种液态化合物,在盛有10mL水的锥形瓶中,小心地滴加8——10滴
是一种液态化合物,在盛有10mL水的锥形瓶中,小心地滴加8——10滴 ,发生剧烈反应,液面上有白色酸雾形成,产生有刺激性气味的气体,该气体可使湿润的品红试纸褪色。
,发生剧烈反应,液面上有白色酸雾形成,产生有刺激性气味的气体,该气体可使湿润的品红试纸褪色。
(6)则 和水反应的化学方程式为:
和水反应的化学方程式为:___________ 。
(7)若将 溶液直接蒸干得不到无水
溶液直接蒸干得不到无水 ,用
,用 与
与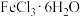 混合共热,则可得到无水
混合共热,则可得到无水 ,其原因是
,其原因是___________ 。(用简要的文字回答)
I.25℃时,部分物质的电离平衡常数如表所示:
| 化学式 |  |  |  |  |
| 电离平衡常数 |  |  |   | 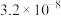 |
请回答下列问题:
(1)室温下,关于
 的
的 溶液,下列分析正确的是
溶液,下列分析正确的是 A.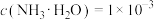  |
B.由水电离出的  |
C.加入少量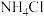 固体, 固体, 的电离平衡逆向移动, 的电离平衡逆向移动, 的值减小 的值减小 |
D.加入等体积 的盐酸,所得溶液: 的盐酸,所得溶液: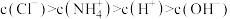 |
 的六种溶液①
的六种溶液①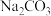 ②
② ③NaClO④
③NaClO④ ⑤
⑤ ⑥
⑥ ,pH由小到大的顺序
,pH由小到大的顺序(3)向次氯酸钠溶液通入少量
 发生反应的离子方程式
发生反应的离子方程式(4)碳酸氢铵溶液显
(5)向a
 的
的 溶液加入等体积的未知浓度的稀盐酸,溶液恰好呈中性,则所加稀盐酸的物质的量浓度
溶液加入等体积的未知浓度的稀盐酸,溶液恰好呈中性,则所加稀盐酸的物质的量浓度 (用含a的式子表示)。
(用含a的式子表示)。II.
 是一种液态化合物,在盛有10mL水的锥形瓶中,小心地滴加8——10滴
是一种液态化合物,在盛有10mL水的锥形瓶中,小心地滴加8——10滴 ,发生剧烈反应,液面上有白色酸雾形成,产生有刺激性气味的气体,该气体可使湿润的品红试纸褪色。
,发生剧烈反应,液面上有白色酸雾形成,产生有刺激性气味的气体,该气体可使湿润的品红试纸褪色。(6)则
 和水反应的化学方程式为:
和水反应的化学方程式为:(7)若将
 溶液直接蒸干得不到无水
溶液直接蒸干得不到无水 ,用
,用 与
与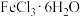 混合共热,则可得到无水
混合共热,则可得到无水 ,其原因是
,其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
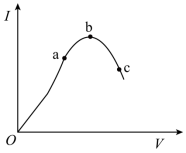
【推荐2】在一定温度下,对冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题:
(1)在一定温度下,向上述醋酸溶液中,加入加水稀释,按要求填空。
①电离平衡将________ (填“向电离方向”、“向生成醋酸分子方向”或“不”)移动;
②醋酸的平衡常数Ka将__________ (填“增大”、“减小”或“不变”)
(2)a、b、c三点对应的溶液中,c(H+)最小为___________ 。
(3)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是___________ 。
(4)若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是 (填字母,下同)。
(5)部分弱酸的电离平衡常数如下表:
①依据表格中三种酸的电离常数,判断三种酸酸性强弱的顺序为_____________________ 。
②向NaCN溶液中通入CO2气体,反应的化学方程式为__________________ 。

(1)在一定温度下,向上述醋酸溶液中,加入加水稀释,按要求填空。
①电离平衡将
②醋酸的平衡常数Ka将
(2)a、b、c三点对应的溶液中,c(H+)最小为
(3)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是
(4)若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是 (填字母,下同)。
| A.加热 | B.加入NaOH稀溶液 | C.加入K2CO3固体 | D.加水 |
| 弱酸 |  |  |  |
| 电离平衡常数 (25℃) | 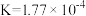 | 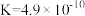 |  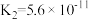 |
②向NaCN溶液中通入CO2气体,反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】I.已知:下表是25℃时某些弱酸的电离平衡常数。
(1)25℃时,体积相等的浓度均为0.1 mol∙L−1的NaClO溶液和CH3COONa溶液,两溶液中c(ClO-)________ c(CH3COO-)(填“>”“<”或“=”)。若要使两溶液的pH相等,应______ (填序号)
a.向NaClO溶液中加适量水
b.向NaClO溶液中加适量的NaOH固体
c.向CH3COONa溶液中加适量水
d.向CH3COONa溶液中加适量CH3COONa固体
(2)由表格中的数据判断下列离子方程式正确的是___________。
(3)在25℃时, 浓度相等的NH4Cl、CH3COONH4、NH4HSO4三种溶液,其对应溶液中溶质的物质的量浓度分别为a、b、c(单位为mol∙L−1),三者由大到小的顺序是
浓度相等的NH4Cl、CH3COONH4、NH4HSO4三种溶液,其对应溶液中溶质的物质的量浓度分别为a、b、c(单位为mol∙L−1),三者由大到小的顺序是___________ 。
(4)在25℃下,将a mol∙L−1的氨水与0.01 mol∙L−1的盐酸等体积混合,充分反应后溶液中c( )=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=
)=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=___________ 。
II.常温时,分别改变相同物质的量浓度的H2CO3和氨水的pH,H2CO3、 、
、 的物质的量分数(δ)及NH3·H2O、
的物质的量分数(δ)及NH3·H2O、 的物质的量分数(δ)如图所示(不考虑溶液中的CO2和NH3分子),已知:δ=
的物质的量分数(δ)如图所示(不考虑溶液中的CO2和NH3分子),已知:δ=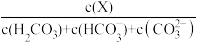 、δ=
、δ=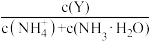 ,根据图象回答下列问题:
,根据图象回答下列问题:
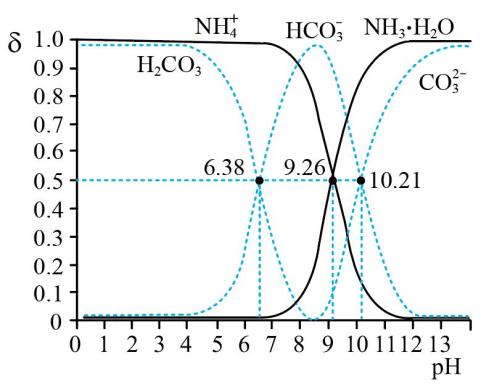
(5)NH4HCO3溶液显___________ 性(填“酸”“碱”或“中”)。
(6)计算反应 +NH3·H2O=
+NH3·H2O= +
+ +H2O的lgK=
+H2O的lgK=___________ 。
| 化学式 | CH3COOH | NH3·H2O | HClO | H2CO3 | H2SO3 |
| Ka | Ka=1.8×10−5 | Kb=1.8×10−5 | Ka=3.0×10−8 | Ka1=4.1×10−7 Ka2=5.6×10−11 | Ka1=1.54×10−2 Ka2=1.02×10−7 |
a.向NaClO溶液中加适量水
b.向NaClO溶液中加适量的NaOH固体
c.向CH3COONa溶液中加适量水
d.向CH3COONa溶液中加适量CH3COONa固体
(2)由表格中的数据判断下列离子方程式正确的是___________。
A.2 +SO2= +SO2= +2CO2+H2O +2CO2+H2O |
B.ClO-+CO2+H2O=HClO+ |
C.ClO-+SO2+H2O=HClO+ |
D.CH3COO-+SO2+H2O=CH3COOH+ |
 浓度相等的NH4Cl、CH3COONH4、NH4HSO4三种溶液,其对应溶液中溶质的物质的量浓度分别为a、b、c(单位为mol∙L−1),三者由大到小的顺序是
浓度相等的NH4Cl、CH3COONH4、NH4HSO4三种溶液,其对应溶液中溶质的物质的量浓度分别为a、b、c(单位为mol∙L−1),三者由大到小的顺序是(4)在25℃下,将a mol∙L−1的氨水与0.01 mol∙L−1的盐酸等体积混合,充分反应后溶液中c(
 )=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=
)=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=II.常温时,分别改变相同物质的量浓度的H2CO3和氨水的pH,H2CO3、
 、
、 的物质的量分数(δ)及NH3·H2O、
的物质的量分数(δ)及NH3·H2O、 的物质的量分数(δ)如图所示(不考虑溶液中的CO2和NH3分子),已知:δ=
的物质的量分数(δ)如图所示(不考虑溶液中的CO2和NH3分子),已知:δ=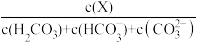 、δ=
、δ=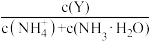 ,根据图象回答下列问题:
,根据图象回答下列问题:
(5)NH4HCO3溶液显
(6)计算反应
 +NH3·H2O=
+NH3·H2O= +
+ +H2O的lgK=
+H2O的lgK=
您最近一年使用:0次

 为
为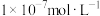 ,此溶液一定呈中性吗
,此溶液一定呈中性吗
 。产物氨气溶于水得到氨水
。产物氨气溶于水得到氨水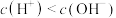

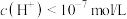
 的浓度为
的浓度为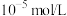 ,则该溶液的pH=
,则该溶液的pH=

