金属铝在酸性或碱性溶液中均可与 发生氧化还原反应,转化关系如图所示:
发生氧化还原反应,转化关系如图所示:
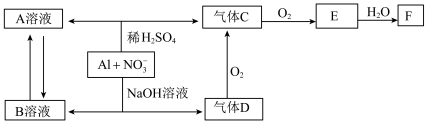
请回答下列问题:
(1)气体D和F反应可生成盐,该盐的化学名称为_____________ 。
(2)C、E排入大气中会造成大气污染,在催化剂存在的情况下,D可以将C、E还原为无毒的气态单质,该单质是_____________ (填化学式)。
(3)将B转化为 的最佳试剂是
的最佳试剂是_____________ (填字母)。
a.CO2 b.NaOH c.HCl d.NH3·H2O
(4)写出D→C反应的化学方程式:__________________________ 。
(5)Al与 在酸性条件下反应的离子方程式为:
在酸性条件下反应的离子方程式为:__________________________ 。
(6)Al与 在碱性条件下反应,Al与被还原的
在碱性条件下反应,Al与被还原的 的物质的量之比为
的物质的量之比为_____________ 。
 发生氧化还原反应,转化关系如图所示:
发生氧化还原反应,转化关系如图所示:
请回答下列问题:
(1)气体D和F反应可生成盐,该盐的化学名称为
(2)C、E排入大气中会造成大气污染,在催化剂存在的情况下,D可以将C、E还原为无毒的气态单质,该单质是
(3)将B转化为
 的最佳试剂是
的最佳试剂是a.CO2 b.NaOH c.HCl d.NH3·H2O
(4)写出D→C反应的化学方程式:
(5)Al与
 在酸性条件下反应的离子方程式为:
在酸性条件下反应的离子方程式为:(6)Al与
 在碱性条件下反应,Al与被还原的
在碱性条件下反应,Al与被还原的 的物质的量之比为
的物质的量之比为
更新时间:2016-12-09 07:36:51
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
【推荐1】 是生产含钼催化剂的重要原料,能溶于氨水和强碱。以钼精矿(主要成分是
是生产含钼催化剂的重要原料,能溶于氨水和强碱。以钼精矿(主要成分是 ,还含有
,还含有 、
、 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图所示:
的工艺流程如图所示: 和
和 发生反应;
发生反应; 元素转化为
元素转化为 、
、 、
、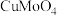 ;
;
②“氨浸”时, 元素以
元素以 的形式进入滤液1中,而
的形式进入滤液1中,而 元素进入滤渣1中;
元素进入滤渣1中;
③ 。
。
回答下列问题:
(1)尾气的成分有 和
和_______ (填化学式)。
(2)“滤渣1”的主要成分是 和
和_______ (填化学式)。
(3)写出“除杂”时反应的离子方程式_______ 。除杂后测得溶液中 ,列式计算并判断
,列式计算并判断 是否沉淀完全
是否沉淀完全_______ 。
(4)“酸沉”时加入 的作用是
的作用是_______ 。
(5)写出四钼酸铵[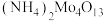 ]发生“焙解”的化学方程式
]发生“焙解”的化学方程式_______ 。
(6) 的结构和
的结构和 相似,如图
相似,如图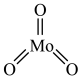 ,易升华,则
,易升华,则 晶体类型为
晶体类型为_______ 。 晶体有多种晶胞,正交相
晶体有多种晶胞,正交相 具有独特的层状结构,层与层之间的作用力为范德华力,根据结构和作用力预测正交相
具有独特的层状结构,层与层之间的作用力为范德华力,根据结构和作用力预测正交相 晶体在日常生活中可用作
晶体在日常生活中可用作_______ 。
(7)工业上还可以在碱性环境下用 溶液和
溶液和 反应制备钼酸盐,同时生成副产品硫酸盐,写出该反应的离子方程式
反应制备钼酸盐,同时生成副产品硫酸盐,写出该反应的离子方程式_______ 。
 是生产含钼催化剂的重要原料,能溶于氨水和强碱。以钼精矿(主要成分是
是生产含钼催化剂的重要原料,能溶于氨水和强碱。以钼精矿(主要成分是 ,还含有
,还含有 、
、 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图所示:
的工艺流程如图所示: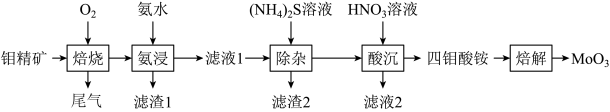
 和
和 发生反应;
发生反应; 元素转化为
元素转化为 、
、 、
、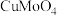 ;
;②“氨浸”时,
 元素以
元素以 的形式进入滤液1中,而
的形式进入滤液1中,而 元素进入滤渣1中;
元素进入滤渣1中;③
 。
。回答下列问题:
(1)尾气的成分有
 和
和(2)“滤渣1”的主要成分是
 和
和(3)写出“除杂”时反应的离子方程式
 ,列式计算并判断
,列式计算并判断 是否沉淀完全
是否沉淀完全(4)“酸沉”时加入
 的作用是
的作用是(5)写出四钼酸铵[
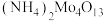 ]发生“焙解”的化学方程式
]发生“焙解”的化学方程式(6)
 的结构和
的结构和 相似,如图
相似,如图 ,易升华,则
,易升华,则 晶体类型为
晶体类型为 晶体有多种晶胞,正交相
晶体有多种晶胞,正交相 具有独特的层状结构,层与层之间的作用力为范德华力,根据结构和作用力预测正交相
具有独特的层状结构,层与层之间的作用力为范德华力,根据结构和作用力预测正交相 晶体在日常生活中可用作
晶体在日常生活中可用作(7)工业上还可以在碱性环境下用
 溶液和
溶液和 反应制备钼酸盐,同时生成副产品硫酸盐,写出该反应的离子方程式
反应制备钼酸盐,同时生成副产品硫酸盐,写出该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】 对神经元有明显的保护作用,在医疗上可用于减轻急性低氧所致的某些神经电流变化。由含钴矿(
对神经元有明显的保护作用,在医疗上可用于减轻急性低氧所致的某些神经电流变化。由含钴矿( 元素主要以
元素主要以 、
、 的形式存在,还含有
的形式存在,还含有 、
、 、
、 、
、 、
、 、
、 元素)制取氯化钴晶体的一种工艺流程如下:
元素)制取氯化钴晶体的一种工艺流程如下:
已知:①焦亚硫酸钠( )是食品中常见的还原剂。
)是食品中常见的还原剂。
②25℃时,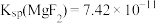 ,
,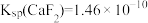 。
。
③部分金属阳离子形成氢氧化物的 见下表:
见下表:
回答下列问题:
(1)操作①的名称为___________ ,浸取时加入Na2S2O5的离子方程式为___________ 。
(2)滤液1中加入 用作氧化剂,
用作氧化剂, 在流程中还具有的作用是
在流程中还具有的作用是___________ 。
(3)加入 溶液调节
溶液调节 至
至 ,若
,若 的范围是3.2~4.0时,则加入
的范围是3.2~4.0时,则加入 溶液生成滤渣2的主要离子方程式为
溶液生成滤渣2的主要离子方程式为___________ 。
(4)滤渣3的主要成分为 和
和 ,则滤液3中
,则滤液3中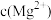 与
与 的比值为
的比值为___________ 。
(5)经过萃取和反萃取操作,溶液5中的阳离子主要含有 和
和 、
、 ,滤液4经过操作3可制备
,滤液4经过操作3可制备 晶体,操作3中包含3个基本实验操作,它们是
晶体,操作3中包含3个基本实验操作,它们是___________ 、___________ 、___________ 。
(6)上述流程中可循环使用的物质是___________ 。
(7)在上述新工艺中,用“稀硫酸和氯酸钠”代替原工艺中“盐酸与硝酸”,其主要优点是___________ 。
 对神经元有明显的保护作用,在医疗上可用于减轻急性低氧所致的某些神经电流变化。由含钴矿(
对神经元有明显的保护作用,在医疗上可用于减轻急性低氧所致的某些神经电流变化。由含钴矿( 元素主要以
元素主要以 、
、 的形式存在,还含有
的形式存在,还含有 、
、 、
、 、
、 、
、 、
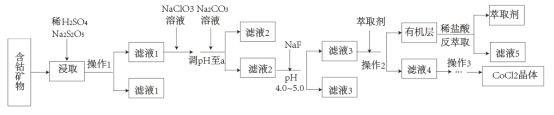
、 元素)制取氯化钴晶体的一种工艺流程如下:
元素)制取氯化钴晶体的一种工艺流程如下:
已知:①焦亚硫酸钠(
 )是食品中常见的还原剂。
)是食品中常见的还原剂。②25℃时,
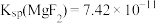 ,
,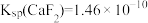 。
。③部分金属阳离子形成氢氧化物的
 见下表:
见下表: |  |  |  |  |  | 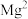 | |
开始沉淀 | 0.3 | 5.5 | 2.7 | 7.2 | 7.6 | 7.6 | 9.6 |
完全沉淀 | 1.1 | 6.6 | 3.2 | 9.2 | 9.6 | 9.2 | 11.1 |
回答下列问题:
(1)操作①的名称为
(2)滤液1中加入
 用作氧化剂,
用作氧化剂, 在流程中还具有的作用是
在流程中还具有的作用是(3)加入
 溶液调节
溶液调节 至
至 ,若
,若 的范围是3.2~4.0时,则加入
的范围是3.2~4.0时,则加入 溶液生成滤渣2的主要离子方程式为
溶液生成滤渣2的主要离子方程式为(4)滤渣3的主要成分为
 和
和 ,则滤液3中
,则滤液3中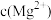 与
与 的比值为
的比值为(5)经过萃取和反萃取操作,溶液5中的阳离子主要含有
 和
和 、
、 ,滤液4经过操作3可制备
,滤液4经过操作3可制备 晶体,操作3中包含3个基本实验操作,它们是
晶体,操作3中包含3个基本实验操作,它们是(6)上述流程中可循环使用的物质是
(7)在上述新工艺中,用“稀硫酸和氯酸钠”代替原工艺中“盐酸与硝酸”,其主要优点是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】垃圾分类正在全国逐渐推广,垃圾资源化是可持续、绿色发展的重要途径。由金属废料(主要含铁、铜和它们的氧化物)制得碱式碳酸铜和摩尔盐[(NH4)2SO4·FeSO4·xH2O]的工艺流程如下图所示:
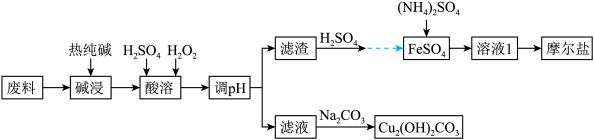
已知:Ksp[Fe(OH)3]=1×10-38 ,Ksp[Cu(OH)2]= 2.2×10-21,一般认为某离子浓度小于或等于10-5mol/L时,该离子转化或去除完全。
请回答下列问题:
(1)热纯碱的作用是_______________ ,H2O2的电子式为___________ 。
(2)调pH步骤可选用的试剂为______________ 。
A.CuO B.Cu(OH)2 C.Fe2O3 D.Fe(OH)3
(3)若所得溶液中c(Cu2+)=0.22 mol·L-1,则需要调节的pH范围是_______________ 。
(4)溶液1经过加热、蒸发至溶液中出现晶体时,自然冷却即可得到晶体,然后抽滤,用酒精洗涤晶体,酒精洗涤的目的是____________________________________ 。
(5)写出该流程中生成碱式碳酸铜的离子方程式________________________________ 。
(6)取3.92g摩尔盐产品,在隔绝空气的条件下加热至135°C时完全失去结晶水,此时固体质量为2.84g,则该摩尔盐结晶水个数x=________ 。

已知:Ksp[Fe(OH)3]=1×10-38 ,Ksp[Cu(OH)2]= 2.2×10-21,一般认为某离子浓度小于或等于10-5mol/L时,该离子转化或去除完全。
请回答下列问题:
(1)热纯碱的作用是
(2)调pH步骤可选用的试剂为
A.CuO B.Cu(OH)2 C.Fe2O3 D.Fe(OH)3
(3)若所得溶液中c(Cu2+)=0.22 mol·L-1,则需要调节的pH范围是
(4)溶液1经过加热、蒸发至溶液中出现晶体时,自然冷却即可得到晶体,然后抽滤,用酒精洗涤晶体,酒精洗涤的目的是
(5)写出该流程中生成碱式碳酸铜的离子方程式
(6)取3.92g摩尔盐产品,在隔绝空气的条件下加热至135°C时完全失去结晶水,此时固体质量为2.84g,则该摩尔盐结晶水个数x=
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】在下列物质转化中,A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如图的转化关系:

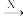
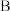

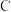

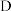
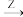
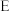
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。请回答:
(1)A是____ ,Y是____ 。
(2)当X是强酸时,B是____ 。写出B生成C的化学方程式:____ 。写出C生成D的化学方程式:____ 。
(3)当X是强碱时,B是____ ,E是____ 。

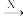
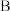

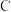

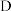
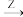
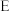
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。请回答:
(1)A是
(2)当X是强酸时,B是
(3)当X是强碱时,B是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E五种元素中只有E为金属元素,五种元素的原子叙述按B、D、C、A、E的顺序依次增大,D、C元素在元素周期表中位置相邻,在一定条件下,B的单质可以分别和A、。C、D的单质化合生成甲、乙、丙化合物,C的单质和D的单质化合物可得丁,戊、己、庚均为化合物。已知乙、丙每个分子中均含有10个电子,下图为相互转化关系。
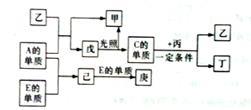
(1)写出实验室制取A的单质的离子反应方程式:____ 。
(2)戊的分子式为___ 。B与D形成的原子个数比为2∶1的化合物中,D原子最外层为8电子结构,请写出该化合物的电子式____ 。
(3)A的单质与丙常温下发生反应生成甲与D的单质,该反应的化学方程式___ 。
(4)实验室配制庚溶液的是按方法是__ 。

(1)写出实验室制取A的单质的离子反应方程式:
(2)戊的分子式为
(3)A的单质与丙常温下发生反应生成甲与D的单质,该反应的化学方程式
(4)实验室配制庚溶液的是按方法是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】I.离子化合物A由三种常见的短周期元素组成,其中两种是金属元素,一种是非金属元素。按以下流程进行实验:

请回答:
(1)组成A的元素为___________ 。(填元素符号)
(2)写出固体C部分溶于NaOH溶液的离子反应方程式___________ 。
(3)A与盐酸发生氧化还原反应,且有无色无味的气体生成,写出该化学反应方程式___________ 。
II.某兴趣小组为了探究84消毒液(主要成分NaClO)和酒精混合使用是否存在安全隐患,利用如图装置进行实验。

请回答:
(1)A中出现黄绿色气体,请写出相应的化学方程式___________ 。(乙醇氧化为乙醛)
(2)有同学用手触碰三颈烧瓶后发现,反应一段时间后装置温度升高,所以提出产生的气体中可能混有O2,该同学为了验证O2,打开弹簧夹,用带火星的木条检验,该操作的错误原因为___________ 。

请回答:
(1)组成A的元素为
(2)写出固体C部分溶于NaOH溶液的离子反应方程式
(3)A与盐酸发生氧化还原反应,且有无色无味的气体生成,写出该化学反应方程式
II.某兴趣小组为了探究84消毒液(主要成分NaClO)和酒精混合使用是否存在安全隐患,利用如图装置进行实验。

请回答:
(1)A中出现黄绿色气体,请写出相应的化学方程式
(2)有同学用手触碰三颈烧瓶后发现,反应一段时间后装置温度升高,所以提出产生的气体中可能混有O2,该同学为了验证O2,打开弹簧夹,用带火星的木条检验,该操作的错误原因为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】铁、铝、铜等金属及其化合物在日常生活中应用广泛。
(1)生铁中含有一种铁碳化合物X,实验室测定该化合物X组成的实验如下,最终得到的固体2是Fe2O3。

①已知固体1有磁性,将其溶于过量盐酸后,溶液中含有的大量阳离子是H+和___________ 。
②X的化学式可表示为___________ ,X与足量的热浓硝酸反应能生成的气体是___________ 。
(2)某溶液中有Mg2+、 、
、 、
、 四种正离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___________(填选项)。
四种正离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___________(填选项)。
(3)氧化铁是重要工业颜料,煅烧FeCO3可得到此颜料。写出在空气中煅烧FeCO3的化学方程式________ 。
(4)向含有1molHNO3和0.7molH2SO4的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。

①a表示的是___________ 的变化曲线。
②n1=___________ 。
③向P点溶液中加入铜粉,最多可溶解铜粉的质量是___________ g。
(1)生铁中含有一种铁碳化合物X,实验室测定该化合物X组成的实验如下,最终得到的固体2是Fe2O3。

①已知固体1有磁性,将其溶于过量盐酸后,溶液中含有的大量阳离子是H+和
②X的化学式可表示为
(2)某溶液中有Mg2+、
 、
、 、
、 四种正离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___________(填选项)。
四种正离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___________(填选项)。| A.Mg2+ | B. | C. | D. |
(3)氧化铁是重要工业颜料,煅烧FeCO3可得到此颜料。写出在空气中煅烧FeCO3的化学方程式
(4)向含有1molHNO3和0.7molH2SO4的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。

①a表示的是
②n1=
③向P点溶液中加入铜粉,最多可溶解铜粉的质量是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
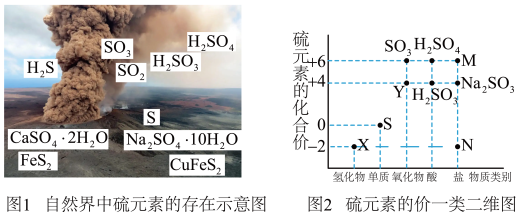
(1)图1中与图2中M、N对应的物质分别是___________ 、___________ 。
(2)在X、Y、S中属于非电解质的是___________ (填化学式);X与Y反应中氧化剂与还原剂的物质的量之比为___________ 。
(3) 溶液易变质,实验室检验。
溶液易变质,实验室检验。 溶液是否变质的基本操作是
溶液是否变质的基本操作是___________ 。
(4)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸以及稀硝酸和 做原料,设计了两种制取胆矾的方案。
做原料,设计了两种制取胆矾的方案。
方案甲: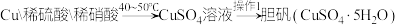
i.该方法中首先要将Cu与稀硫酸和稀硝酸混合,为了只得到 溶液,需向50mL1.0mol/L稀硝酸中加入
溶液,需向50mL1.0mol/L稀硝酸中加入___________ mL1.0mol/L稀硫酸与之混合。
ii.操作1:___________ 、___________ 、过滤、洗涤和干燥
方案乙:
iii.该方法的化学方程式___________ 。
iv.这两种方案,你认为哪一种方案更合理?___________ (填“方案甲”或“方案乙”)。

(1)图1中与图2中M、N对应的物质分别是
(2)在X、Y、S中属于非电解质的是
(3)
 溶液易变质,实验室检验。
溶液易变质,实验室检验。 溶液是否变质的基本操作是
溶液是否变质的基本操作是(4)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸以及稀硝酸和
 做原料,设计了两种制取胆矾的方案。
做原料,设计了两种制取胆矾的方案。方案甲:
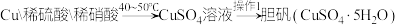
i.该方法中首先要将Cu与稀硫酸和稀硝酸混合,为了只得到
 溶液,需向50mL1.0mol/L稀硝酸中加入
溶液,需向50mL1.0mol/L稀硝酸中加入ii.操作1:
方案乙:

iii.该方法的化学方程式
iv.这两种方案,你认为哪一种方案更合理?
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】亚硝酸钠( )是一种工业盐,外观与食盐非常相似,毒性较强。某化学实验小组用如图装置(略去夹持仪器)制备亚硝酸钠。
)是一种工业盐,外观与食盐非常相似,毒性较强。某化学实验小组用如图装置(略去夹持仪器)制备亚硝酸钠。
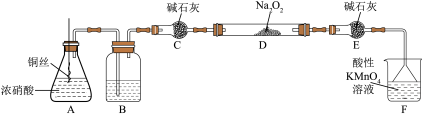
已知: ;酸性条件下,NO、
;酸性条件下,NO、 和
和 均能与
均能与 反应生成
反应生成 和
和 。
。
(1)装置B中发生反应的化学方程式为___________ 。
(2)装置C、E的作用是___________ 。
(3) 反应完全后,为测定产品纯度,该小组取
反应完全后,为测定产品纯度,该小组取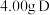 中的产品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用
中的产品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用 酸性
酸性 溶液进行滴定,实验所得数据如表(假设酸性
溶液进行滴定,实验所得数据如表(假设酸性 溶液不与杂质反应):
溶液不与杂质反应):
① 标准溶液应用
标准溶液应用___________ (填“酸式”或“碱式”)滴定管盛装,注入 标准溶液之前,滴定管需要
标准溶液之前,滴定管需要___________ 、洗涤和润洗。
②第一次实验数据出现异常,造成这种异常的原因可能是___________ (填代号)。
a.锥形瓶洗净后未干燥
b.盛装 的滴定管用蒸馏水洗净后未用标准液润洗
的滴定管用蒸馏水洗净后未用标准液润洗
c.滴定前平视读数,滴定终点时俯视读数
d.盛装 的滴定管滴定前有气泡,滴定后气泡消失
的滴定管滴定前有气泡,滴定后气泡消失
③滴定终点的实验现象为___________ ,该产品中亚硝酸钠的质量分数为___________ 。(计算结果保留4位有效数字)
(4)若 未反应完全,则会使产品纯度的测定结果
未反应完全,则会使产品纯度的测定结果___________ (“偏大”“偏小”或“无影响”)。
 )是一种工业盐,外观与食盐非常相似,毒性较强。某化学实验小组用如图装置(略去夹持仪器)制备亚硝酸钠。
)是一种工业盐,外观与食盐非常相似,毒性较强。某化学实验小组用如图装置(略去夹持仪器)制备亚硝酸钠。
已知:
 ;酸性条件下,NO、
;酸性条件下,NO、 和
和 均能与
均能与 反应生成
反应生成 和
和 。
。(1)装置B中发生反应的化学方程式为
(2)装置C、E的作用是
(3)
 反应完全后,为测定产品纯度,该小组取
反应完全后,为测定产品纯度,该小组取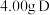 中的产品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用
中的产品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用 酸性
酸性 溶液进行滴定,实验所得数据如表(假设酸性
溶液进行滴定,实验所得数据如表(假设酸性 溶液不与杂质反应):
溶液不与杂质反应):| 滴定次数 | 1 | 2 | 3 | 4 |
消耗 溶液体积/mL 溶液体积/mL | 20.90 | 20.02 | 20.00 | 19.98 |
 标准溶液应用
标准溶液应用 标准溶液之前,滴定管需要
标准溶液之前,滴定管需要②第一次实验数据出现异常,造成这种异常的原因可能是
a.锥形瓶洗净后未干燥
b.盛装
 的滴定管用蒸馏水洗净后未用标准液润洗
的滴定管用蒸馏水洗净后未用标准液润洗c.滴定前平视读数,滴定终点时俯视读数
d.盛装
 的滴定管滴定前有气泡,滴定后气泡消失
的滴定管滴定前有气泡,滴定后气泡消失③滴定终点的实验现象为
(4)若
 未反应完全,则会使产品纯度的测定结果
未反应完全,则会使产品纯度的测定结果
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如下图所示(部分产物已略去)
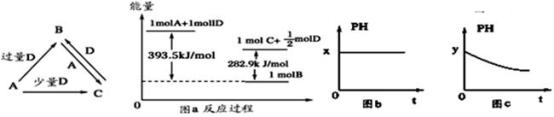
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为____________________ 。
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则 ①C的化学式为_________________________ 。
②反应B+A→C的离子方程式为__________________________ 。
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的蒸发)
①若图b符合事实,则D为________ (填化学式),此时图b中
____ 7(填“﹥”“﹤”“=”)。②若图c符合事实,则其pH变化的原因是__________ (用离子方程式表示)
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出1molA和D反应生成C的反应热为ΔH=_____________ 。

(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则 ①C的化学式为
②反应B+A→C的离子方程式为
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的蒸发)
①若图b符合事实,则D为

(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出1molA和D反应生成C的反应热为ΔH=
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C三种物质中均含有同一种元素,它们之间有如右图所示的转化关系(部分反应物质已略去)。

Ⅰ.(1)若A是一种两性氧化物,B的水溶液呈酸性,请写出反应④的离子方程式:______________ ,B溶液显酸性的原因(用离子方程式表示)_____________ 。
(2)若反应①为置换反应,反应④为化合反应,C物质大量存在于海水中,是人体生理活动不可缺少的物质。工业上可以用C来制取A或B,保存少量单质A的方法 是__________ ,A在氧气中燃烧产物所含的化学键有_______________ ;用C来制取B反应的化学方程式为______________________ 。
(3)若反应①②③均为化合反应,反应④为置换反应。当A为一种金属单质时,请写出反应③可能的离子方程式________________________ 。若只用一种试剂鉴别B、C,可以选的试剂是_____________ 。

Ⅰ.(1)若A是一种两性氧化物,B的水溶液呈酸性,请写出反应④的离子方程式:
(2)若反应①为置换反应,反应④为化合反应,C物质大量存在于海水中,是人体生理活动不可缺少的物质。工业上可以用C来制取A或B,保存少量单质A的方法 是
(3)若反应①②③均为化合反应,反应④为置换反应。当A为一种金属单质时,请写出反应③可能的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】可根据化学试剂相互之间逐滴滴加所产生的现象不同,来检验化学物质。此方法可以检验 和
和 溶液,现按要求回答下列问题:
溶液,现按要求回答下列问题:
(1)向 溶液中逐滴滴入
溶液中逐滴滴入 溶液至过量,产生的现象分别是①
溶液至过量,产生的现象分别是①___________ ②__________ ,对应反应的离子方程式分别是①___________ ②___________ ,并画出相应的图像变化__________
(2)向 溶液中逐滴滴入
溶液中逐滴滴入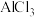 溶液至过量,产生的现象分别是①
溶液至过量,产生的现象分别是①__________ ②_________ ,对应反应的离子方程式分别是①__________ ②___________ ,并画出相应的图像变化_______
 和
和 溶液,现按要求回答下列问题:
溶液,现按要求回答下列问题:(1)向
 溶液中逐滴滴入
溶液中逐滴滴入 溶液至过量,产生的现象分别是①
溶液至过量,产生的现象分别是①(2)向
 溶液中逐滴滴入
溶液中逐滴滴入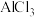 溶液至过量,产生的现象分别是①
溶液至过量,产生的现象分别是①
您最近一年使用:0次



