湿式吸收一电解再生法,是采用氧化一电解的双反应器对含硫化氢的废气进行脱硫制氢。实验表明,双反应器法可以在较宽的范围内实现对硫化氢的有效吸收,并可同时制取氢气和硫磺,该法基本流程见图l,其中氧化吸收器中为FeCl3溶液,电解反应器可实现FeCl3溶液的恢复及H2的制备。
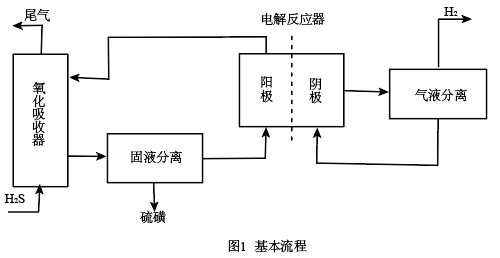
(1)氧化反应器中发生的主要反应的离子有程式为________
(2)电解反应器中,阳极反应式是________
(3)某研究小组在实验室中模拟上述过程,研究FeCl3溶液吸收H2S气体的效率,实验时要先向FeCl3溶液中通入N2,其目的是________ 。对影响吸收效率的因素提出如下假设,请你完成假设二和假设三:
假设一:H2S气体的通入速率;
假设二:______________ ;
假设三:______________ 。
请你设计实验就假设一进行验证,将实验步骤及结论补充完整(注:可用pH计测量溶液中的H+浓度)
(4)将FeCl3溶液吸收H2S气体后的溶液过滤后,取少量向其中加入BaCl2溶液,发现有白色沉淀生成(注:BaS溶于盐酸)。则白色沉淀可能是_______ 你的判断理由是_______

(1)氧化反应器中发生的主要反应的离子有程式为
(2)电解反应器中,阳极反应式是
(3)某研究小组在实验室中模拟上述过程,研究FeCl3溶液吸收H2S气体的效率,实验时要先向FeCl3溶液中通入N2,其目的是
假设一:H2S气体的通入速率;
假设二:
假设三:
请你设计实验就假设一进行验证,将实验步骤及结论补充完整(注:可用pH计测量溶液中的H+浓度)
| 实验步骤及结论 别取等体积、等浓度的FeCl3溶液于不同的试管中; ② ③ ④ ⑤结论: |
(4)将FeCl3溶液吸收H2S气体后的溶液过滤后,取少量向其中加入BaCl2溶液,发现有白色沉淀生成(注:BaS溶于盐酸)。则白色沉淀可能是
更新时间:2016-12-09 07:52:08
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】 是重要的化工原料,由软锰矿制备
是重要的化工原料,由软锰矿制备 的一种工艺流程如图:
的一种工艺流程如图:

资料:①软锰矿的主要成分为 ,主要杂质有
,主要杂质有 和
和 。
。
②金属离子开始沉淀和完全沉淀时的 :
:
③该工艺条件下, 与
与 ,不反应。
,不反应。
(1)溶出
①溶出前,软锰矿需研磨。目的是_______ 。
②溶出时, 的氧化过程及得到
的氧化过程及得到 主要途径如图所示。
主要途径如图所示。
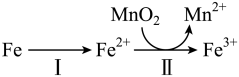
ⅰ.步骤Ⅰ是从软锰矿中溶出 的主要反应,反应的离子方程式是
的主要反应,反应的离子方程式是_______ 。
ⅱ.若 全部来自于反
全部来自于反 ,完全溶出
,完全溶出 所需
所需 与
与 的物质的量比值为2.而实际比值(0.9)小于2,原因是
的物质的量比值为2.而实际比值(0.9)小于2,原因是_______ 。
(2)纯化
已知: 的氧化性与溶液
的氧化性与溶液 有关。纯化时先加入
有关。纯化时先加入 ,后加入
,后加入 ,调溶液
,调溶液 ,说明试剂加入顺序及调节
,说明试剂加入顺序及调节 的原因:
的原因:_______ 。
(3)电解
 纯化液经电解得
纯化液经电解得 。生成
。生成 的电极反应式是
的电极反应式是_______ 。
(4)产品纯度测定
向ag产品中依次加入足量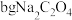 和足量稀
和足量稀 ,加热至充分反应,再用
,加热至充分反应,再用 溶液滴定剩余
溶液滴定剩余 至终点,消耗
至终点,消耗 溶液的体积为dL(已知:
溶液的体积为dL(已知: 及
及 均被还原为
均被还原为 。相对分子质量:
。相对分子质量: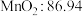 、
、 :)。
:)。
产品纯度为_______ (用质量分数表示)。
 是重要的化工原料,由软锰矿制备
是重要的化工原料,由软锰矿制备 的一种工艺流程如图:
的一种工艺流程如图:
资料:①软锰矿的主要成分为
 ,主要杂质有
,主要杂质有 和
和 。
。②金属离子开始沉淀和完全沉淀时的
 :
: |  |  |  | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
 与
与 ,不反应。
,不反应。(1)溶出
①溶出前,软锰矿需研磨。目的是
②溶出时,
 的氧化过程及得到
的氧化过程及得到 主要途径如图所示。
主要途径如图所示。
ⅰ.步骤Ⅰ是从软锰矿中溶出
 的主要反应,反应的离子方程式是
的主要反应,反应的离子方程式是ⅱ.若
 全部来自于反
全部来自于反 ,完全溶出
,完全溶出 所需
所需 与
与 的物质的量比值为2.而实际比值(0.9)小于2,原因是
的物质的量比值为2.而实际比值(0.9)小于2,原因是(2)纯化
已知:
 的氧化性与溶液
的氧化性与溶液 有关。纯化时先加入
有关。纯化时先加入 ,后加入
,后加入 ,调溶液
,调溶液 ,说明试剂加入顺序及调节
,说明试剂加入顺序及调节 的原因:
的原因:(3)电解
 纯化液经电解得
纯化液经电解得 。生成
。生成 的电极反应式是
的电极反应式是(4)产品纯度测定
向ag产品中依次加入足量
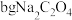 和足量稀
和足量稀 ,加热至充分反应,再用
,加热至充分反应,再用 溶液滴定剩余
溶液滴定剩余 至终点,消耗
至终点,消耗 溶液的体积为dL(已知:
溶液的体积为dL(已知: 及
及 均被还原为
均被还原为 。相对分子质量:
。相对分子质量: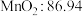 、
、 :)。
:)。产品纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】亚氯酸钠( )常用于纺织、造低业漂白,也用于食品消毒、水处理等。
)常用于纺织、造低业漂白,也用于食品消毒、水处理等。
【资科1】①亚氯酸钠( )受热易分解;②纯
)受热易分解;②纯 易分解爆炸,一般用稀有气体或空气稀释到10%以下;③
易分解爆炸,一般用稀有气体或空气稀释到10%以下;③ 有强烈刺激性气味,易溶于水,不与水反应。
有强烈刺激性气味,易溶于水,不与水反应。
【实验一】制取 晶体
晶体
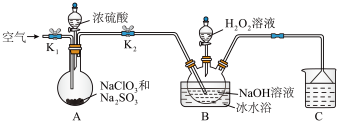
(1)实验过程中需要持续通入空气,目的是_______ 。
(2)装置C中漏斗的作用是_______ 。
(3)装置A的反应中还原剂和氧化剂的物质的量之比为_______ ,还原产物为_______ (填化学式)。
(4)写出装置B中反应的化学方程式并用单线桥法表示电子转移的方向和数目:_______ ;反应结束后,为从溶液中得到 固体,采取减压蒸发而不用常压蒸发,原因是
固体,采取减压蒸发而不用常压蒸发,原因是_______ 。
【实验二】测定亚氯酸钠的含量
【资料2】 ;
;
实验步骤:①准确称取所得亚氯酸钠样品m g于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液配成200 mL待测溶液。②移取50.00 mL待测溶液于锥形瓶中,加几滴淀粉溶液,用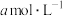
 标准溶液滴定至终点,重复2次,测得消耗标准溶液体积的平均值为V mL。
标准溶液滴定至终点,重复2次,测得消耗标准溶液体积的平均值为V mL。
(5)达到滴定终点时的现象为_______ 。
(6)该样品中 的质量分数为
的质量分数为_______ %(用含m、a、V的代数式表示)。
 )常用于纺织、造低业漂白,也用于食品消毒、水处理等。
)常用于纺织、造低业漂白,也用于食品消毒、水处理等。【资科1】①亚氯酸钠(
 )受热易分解;②纯
)受热易分解;②纯 易分解爆炸,一般用稀有气体或空气稀释到10%以下;③
易分解爆炸,一般用稀有气体或空气稀释到10%以下;③ 有强烈刺激性气味,易溶于水,不与水反应。
有强烈刺激性气味,易溶于水,不与水反应。【实验一】制取
 晶体
晶体
(1)实验过程中需要持续通入空气,目的是
(2)装置C中漏斗的作用是
(3)装置A的反应中还原剂和氧化剂的物质的量之比为
(4)写出装置B中反应的化学方程式并用单线桥法表示电子转移的方向和数目:
 固体,采取减压蒸发而不用常压蒸发,原因是
固体,采取减压蒸发而不用常压蒸发,原因是【实验二】测定亚氯酸钠的含量
【资料2】
 ;
;
实验步骤:①准确称取所得亚氯酸钠样品m g于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液配成200 mL待测溶液。②移取50.00 mL待测溶液于锥形瓶中,加几滴淀粉溶液,用
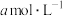
 标准溶液滴定至终点,重复2次,测得消耗标准溶液体积的平均值为V mL。
标准溶液滴定至终点,重复2次,测得消耗标准溶液体积的平均值为V mL。(5)达到滴定终点时的现象为
(6)该样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】原子序数由小到大排列的四种短周期元素X、Y、Z、W四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。M元素与X同主族,与W同周期。
(1)M元素是___________ (填元素符号)。
(2)Z、W形成的气态氢物的稳定性为___________ >___________ 。(填化学式)
(3)写出 的电子式
的电子式___________ ,写出 与水反应的离子方程式
与水反应的离子方程式___________ 。
(4)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为___________ 。
(5)由X、Y、Z、W四种元素组成的一种离子化合物A,已知① 能与足量
能与足量 浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体B,该气体能与氯水反应。则A是
浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体B,该气体能与氯水反应。则A是___________ (填化学式)。写出该气体B与氯水反应的离子方程式___________ 。
(6)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物C, 中含有6mol结晶水。对化合物C进行下实验:
中含有6mol结晶水。对化合物C进行下实验:
a.取C的溶液加入过量浓 溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
b.另取C的溶液,加入过量 溶液产生白色沉淀,加盐酸沉淀不溶解
溶液产生白色沉淀,加盐酸沉淀不溶解
①写出C的化学式为___________ 。
②试写出C与 按物质的量比
按物质的量比 在溶液中反应的化学方程式
在溶液中反应的化学方程式___________ 。
(1)M元素是
(2)Z、W形成的气态氢物的稳定性为
(3)写出
 的电子式
的电子式 与水反应的离子方程式
与水反应的离子方程式(4)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为
(5)由X、Y、Z、W四种元素组成的一种离子化合物A,已知①
 能与足量
能与足量 浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体B,该气体能与氯水反应。则A是
浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体B,该气体能与氯水反应。则A是(6)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物C,
 中含有6mol结晶水。对化合物C进行下实验:
中含有6mol结晶水。对化合物C进行下实验:a.取C的溶液加入过量浓
 溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;b.另取C的溶液,加入过量
 溶液产生白色沉淀,加盐酸沉淀不溶解
溶液产生白色沉淀,加盐酸沉淀不溶解①写出C的化学式为
②试写出C与
 按物质的量比
按物质的量比 在溶液中反应的化学方程式
在溶液中反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组制备硫化亚铁并探究其自燃性质。
实验I 在石棉网上把研细的硫粉和铁粉按一定比例混合均匀,用灼热的玻璃棒触及混合物,当混合物呈红热状态时,移开玻璃棒,得到黑色FeS。
(1)玻璃棒的作用是______________________ 。
(2)常温下,该实验制得的硫化亚铁__________ (填“能”或“不能”)自燃。
实验II 将H2S气体长时间通入硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液中进行硫化,制备硫化亚铁。
装置示意图如下。
(3)B装置的作用是________________ 。
(4)C中反应生成硫化亚铁的离子方程式为________ 。
(5)C中的固液混合物经过滤、洗涤、干燥得到产品。检验过滤所得固体物质是否洗涤干净的方法是________________________ 。
(6)产品分析结果如下表:
①表中x =________ 。
②总铁质量分数大于亚铁质量分数,原因是________
(7)制得的硫化亚铁在常温下能发生缓慢氧化而自燃,写出该过程的化学方程式:________ (写一个)。
实验I 在石棉网上把研细的硫粉和铁粉按一定比例混合均匀,用灼热的玻璃棒触及混合物,当混合物呈红热状态时,移开玻璃棒,得到黑色FeS。
(1)玻璃棒的作用是
(2)常温下,该实验制得的硫化亚铁
实验II 将H2S气体长时间通入硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液中进行硫化,制备硫化亚铁。
装置示意图如下。

(3)B装置的作用是
(4)C中反应生成硫化亚铁的离子方程式为
(5)C中的固液混合物经过滤、洗涤、干燥得到产品。检验过滤所得固体物质是否洗涤干净的方法是
(6)产品分析结果如下表:
| 硫质量分数/% | 总铁质量分数/% | 亚铁质量分数/% | 硫化亚铁质量分数/% |
| 22. 00 | 44.60 | 38.50 | x |
②总铁质量分数大于亚铁质量分数,原因是
(7)制得的硫化亚铁在常温下能发生缓慢氧化而自燃,写出该过程的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】 常用作催化剂、杀虫剂等。一种辉铜矿(难溶于水,主要含
常用作催化剂、杀虫剂等。一种辉铜矿(难溶于水,主要含 ,还含少量
,还含少量 )以为原料制取
)以为原料制取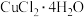 晶体的流程如下图所示:
晶体的流程如下图所示:
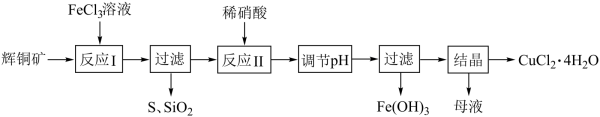
(1)反应Ⅰ中有 、
、 等物质生成。写出该反应的离子方程式:
等物质生成。写出该反应的离子方程式:_______ 。
(2) 是一种常见氧化剂和消毒剂。
是一种常见氧化剂和消毒剂。
①反应Ⅱ可以将稀硝酸换成稀盐酸和 的混合液。写出改为稀盐酸和
的混合液。写出改为稀盐酸和 的混合液后所发生反应的离子方程式:
的混合液后所发生反应的离子方程式:_______ 。
②反应Ⅱ还可以将稀硝酸换成 。与使用稀硝酸和
。与使用稀硝酸和 相比,使用稀盐酸和
相比,使用稀盐酸和 的混合液的优点是
的混合液的优点是_______ 。
(3)调节 的目的是将溶液中的
的目的是将溶液中的 转化为
转化为 沉淀。检验沉淀后的上层清液中是否含有
沉淀。检验沉淀后的上层清液中是否含有 的方法是
的方法是_______ 。
 常用作催化剂、杀虫剂等。一种辉铜矿(难溶于水,主要含
常用作催化剂、杀虫剂等。一种辉铜矿(难溶于水,主要含 ,还含少量
,还含少量 )以为原料制取
)以为原料制取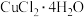 晶体的流程如下图所示:
晶体的流程如下图所示:
(1)反应Ⅰ中有
 、
、 等物质生成。写出该反应的离子方程式:
等物质生成。写出该反应的离子方程式:(2)
 是一种常见氧化剂和消毒剂。
是一种常见氧化剂和消毒剂。①反应Ⅱ可以将稀硝酸换成稀盐酸和
 的混合液。写出改为稀盐酸和
的混合液。写出改为稀盐酸和 的混合液后所发生反应的离子方程式:
的混合液后所发生反应的离子方程式:②反应Ⅱ还可以将稀硝酸换成
 。与使用稀硝酸和
。与使用稀硝酸和 相比,使用稀盐酸和
相比,使用稀盐酸和 的混合液的优点是
的混合液的优点是(3)调节
 的目的是将溶液中的
的目的是将溶液中的 转化为
转化为 沉淀。检验沉淀后的上层清液中是否含有
沉淀。检验沉淀后的上层清液中是否含有 的方法是
的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y.已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
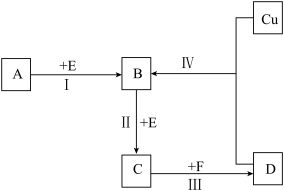
(1)若A、B、C、D均为含X元素的化合物,且A的一个分子中只含有10个电子,则:
①A的分子构型为_____________________ 。
②反应Ⅰ的化学方程式为_________________ 。
③化合物NaX3是合成“达菲”的中间活性物质,NaX3受撞击后生成Na3X和另一种气体单质,请写出该反应的化学方程式_______________________________________ 。
(2)若A、B、C、D均为含Y元素的化合物,且A的摩尔质量为120 g·mol ,则:
,则:
①反应Ⅳ的溶液加热蒸干所得的晶体属于_______ 晶体(填“离子”、“分子”、“原子”).
②反应I的化学方程式为__________________________ 。
③若灼烧6gA产生的B(气态)全部转化为C(气态)时放出9.83 KJ热量,请写第Ⅱ步反应的热化学方程式___________________________________ 。

(1)若A、B、C、D均为含X元素的化合物,且A的一个分子中只含有10个电子,则:
①A的分子构型为
②反应Ⅰ的化学方程式为
③化合物NaX3是合成“达菲”的中间活性物质,NaX3受撞击后生成Na3X和另一种气体单质,请写出该反应的化学方程式
(2)若A、B、C、D均为含Y元素的化合物,且A的摩尔质量为120 g·mol
 ,则:
,则:①反应Ⅳ的溶液加热蒸干所得的晶体属于
②反应I的化学方程式为
③若灼烧6gA产生的B(气态)全部转化为C(气态)时放出9.83 KJ热量,请写第Ⅱ步反应的热化学方程式
您最近一年使用:0次
【推荐1】铍是原子能、火箭、导弹、航空以及冶金工业中不可缺少的宝贵材料。以绿柱石[Be3Al2(SiO3)6]为原料制备两性金属铍的工艺如图:

回答下列问题:
(1)绿柱石写成氧化物的形式为___________ 。
(2)750℃烧结时,Na3FeF6仅与绿柱石中BeO作用生成易溶于水的Na2BeF4,滤渣的主要成分是Fe2O3和___________ 。
(3)“水浸”时“产物压碎磨细”的目的是___________ ,为检验“过滤1”的滤液中是否含有Na+,可选用的方法是___________ (填方法名称)。
(4)“沉氟”的化学方程式为___________ 。
(5)镍坩埚作阴极、石墨作阳极,350~400℃电解NaCl-BeCl2熔融混合物得到金属铍,阳极反应式为___________ ;不能用该电解槽电解熔融氯化铍制金属铍的原因可能是___________ 。

回答下列问题:
(1)绿柱石写成氧化物的形式为
(2)750℃烧结时,Na3FeF6仅与绿柱石中BeO作用生成易溶于水的Na2BeF4,滤渣的主要成分是Fe2O3和
(3)“水浸”时“产物压碎磨细”的目的是
(4)“沉氟”的化学方程式为
(5)镍坩埚作阴极、石墨作阳极,350~400℃电解NaCl-BeCl2熔融混合物得到金属铍,阳极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】按要求写出下列含氯物质转化的方程式。
⑴某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过低,对实验的影响可忽略)。
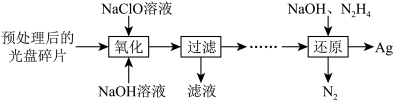
①NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的离子方程式为____ 。
②AgCl所发生“还原”反应的化学方程式为____ 。
⑵Cl2O可用作氯化剂,可由Cl2与潮湿的Na2CO3反应制得,反应的产物之一为NaHCO3。该反应的化学方程式为____ 。
⑶高氯酸钠是强氧化剂,可由电解NaClO3溶液制得。该反应的离子方程式为____ 。
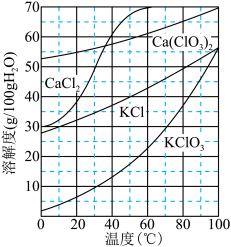
⑷如图所示为几种含氯化合物的溶解度随温度的变化曲线。常温下将其中某两种物质的饱和溶液混合,会发生反应。该反应的化学方程式为____ 。
⑴某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过低,对实验的影响可忽略)。

①NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的离子方程式为
②AgCl所发生“还原”反应的化学方程式为
⑵Cl2O可用作氯化剂,可由Cl2与潮湿的Na2CO3反应制得,反应的产物之一为NaHCO3。该反应的化学方程式为
⑶高氯酸钠是强氧化剂,可由电解NaClO3溶液制得。该反应的离子方程式为
⑷如图所示为几种含氯化合物的溶解度随温度的变化曲线。常温下将其中某两种物质的饱和溶液混合,会发生反应。该反应的化学方程式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3 大量地用于电镀工业中。
(1)在下图装置中,观察到图 1 装置铜电极上产生大量的无色气泡,而图 2 装置中铜电极上无气体产生,铬电极上产生大量有色气体。
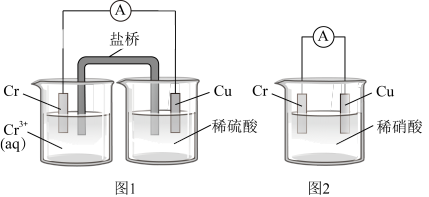
图 2 装置中铬电极的电极反应式______________________
(2)最近赣州酒驾检查特别严,利用 CrO3具有强氧化性,有机物(如酒精)遇到 CrO3时,猛烈反应,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3],另该过程中乙醇被氧化成乙酸,从而增强导电性,根据电流大小可自动换算出酒精含量。写出该反应的化学方程式为_________________________
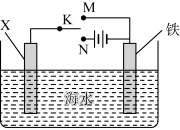
(3)虽然铬加到铁中可将铁做成不锈钢可减少金属腐蚀,但生产成本高,生活中很多情况下还是直接使用钢铁,但易腐蚀,利用右图装置,可以模拟铁的电化学防护。若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于________ 处。若 X 为锌,开关K 置于________ 处。
(4)CrO3和 K2Cr2O7均易溶于水,这是工业上造成铬污染的主要原因。净化处理方法之一是将含+6 价 Cr 的废水放入电解槽内,用铁作阳极,加入 适量的 NaCl 进行电解:阳极区生成的 Fe2+和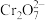 发生反应,生成的 Fe3+和 Cr3+在阴极区与OH-结合生成 Fe(OH)3和 Cr(OH)3沉淀除去【已知某条件下的KspFe (OH)3 = 3.0×10-31, KspCr(OH)3 = 6.0×10-38】。已知电解后的溶液中 c(Fe3+)为 2.0×10-6 mol·L1,则溶液中c(Cr3+)为
发生反应,生成的 Fe3+和 Cr3+在阴极区与OH-结合生成 Fe(OH)3和 Cr(OH)3沉淀除去【已知某条件下的KspFe (OH)3 = 3.0×10-31, KspCr(OH)3 = 6.0×10-38】。已知电解后的溶液中 c(Fe3+)为 2.0×10-6 mol·L1,则溶液中c(Cr3+)为______________ mol·L-1。
(1)在下图装置中,观察到图 1 装置铜电极上产生大量的无色气泡,而图 2 装置中铜电极上无气体产生,铬电极上产生大量有色气体。

图 2 装置中铬电极的电极反应式
(2)最近赣州酒驾检查特别严,利用 CrO3具有强氧化性,有机物(如酒精)遇到 CrO3时,猛烈反应,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3],另该过程中乙醇被氧化成乙酸,从而增强导电性,根据电流大小可自动换算出酒精含量。写出该反应的化学方程式为
(3)虽然铬加到铁中可将铁做成不锈钢可减少金属腐蚀,但生产成本高,生活中很多情况下还是直接使用钢铁,但易腐蚀,利用右图装置,可以模拟铁的电化学防护。若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于

(4)CrO3和 K2Cr2O7均易溶于水,这是工业上造成铬污染的主要原因。净化处理方法之一是将含+6 价 Cr 的废水放入电解槽内,用铁作阳极,加入 适量的 NaCl 进行电解:阳极区生成的 Fe2+和
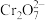 发生反应,生成的 Fe3+和 Cr3+在阴极区与OH-结合生成 Fe(OH)3和 Cr(OH)3沉淀除去【已知某条件下的KspFe (OH)3 = 3.0×10-31, KspCr(OH)3 = 6.0×10-38】。已知电解后的溶液中 c(Fe3+)为 2.0×10-6 mol·L1,则溶液中c(Cr3+)为
发生反应,生成的 Fe3+和 Cr3+在阴极区与OH-结合生成 Fe(OH)3和 Cr(OH)3沉淀除去【已知某条件下的KspFe (OH)3 = 3.0×10-31, KspCr(OH)3 = 6.0×10-38】。已知电解后的溶液中 c(Fe3+)为 2.0×10-6 mol·L1,则溶液中c(Cr3+)为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.某化学学习小组为探究NO2和SO2的反应进行如图所示实验。

(1)图甲两集气瓶中__ (填“上”或“下”)瓶气体颜色深。
(2)图乙中反应的现象是___ 。
(3)图丙中“有红棕色气体产生”说明SO2和NO2反应的产物中有__ ,NO2在该反应中显__ 性。
(4)由图乙和图丙中的现象写出NO2和SO2反应的化学方程式:___ 。
Ⅱ.某课外活动小组欲探究镁与NO2的反应。已知镁与CO2的反应为2Mg+CO2 2MgO+C。
2MgO+C。
(1)该小组类比Mg与CO2的反应对Mg与NO2的反应进行猜测,写出Mg与NO2反应的化学方程式:__ 。
(2)该小组设计如下实验验证上述猜测,实验装置(用于连接玻璃管的乳胶管均内衬锡纸)如图所示。

资料信息:2NO2+2NaOH=NaNO2+NaNO3+H2O
①装置A中的试剂是__ 。
②干燥管和装置B的作用分别是__ 、__ 。
③正确的实验操作步骤是__ 。
a.通入NO2
b.打开弹簧夹
c.点燃酒精灯
d.当硬质玻璃管充满红棕色气体后,关闭弹簧夹

(1)图甲两集气瓶中
(2)图乙中反应的现象是
(3)图丙中“有红棕色气体产生”说明SO2和NO2反应的产物中有
(4)由图乙和图丙中的现象写出NO2和SO2反应的化学方程式:
Ⅱ.某课外活动小组欲探究镁与NO2的反应。已知镁与CO2的反应为2Mg+CO2
 2MgO+C。
2MgO+C。(1)该小组类比Mg与CO2的反应对Mg与NO2的反应进行猜测,写出Mg与NO2反应的化学方程式:
(2)该小组设计如下实验验证上述猜测,实验装置(用于连接玻璃管的乳胶管均内衬锡纸)如图所示。

资料信息:2NO2+2NaOH=NaNO2+NaNO3+H2O
①装置A中的试剂是
②干燥管和装置B的作用分别是
③正确的实验操作步骤是
a.通入NO2
b.打开弹簧夹
c.点燃酒精灯
d.当硬质玻璃管充满红棕色气体后,关闭弹簧夹
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应在实现物质转化的同时还伴随着能量转化,最常见的一种能量变化就是化学能与热能之间的转化。在潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可用于制取氧气。
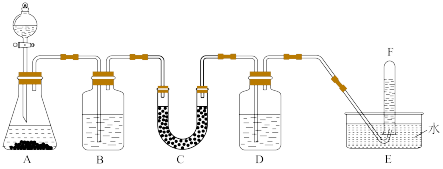
(1)A是用CaCO3制取CO2的装置。写出A中发生反应的离子方程式:_______ 。
(2)按要求填写表中空格:
(3)反应后取D中溶液,向其中逐滴加入稀盐酸,产生的CO2气体体积与所加入盐酸的体积之间的关系如图所示:

则加入盐酸之前D中溶质的成分以及对应物质的量之比是_______ 。
(4)为了达到实验目的,是否需要在B装置之后增加一个吸收水蒸气的装置,请说明理由:_______ 。
(5)研究发现,一定条件下CO2加氢可制备甲酸(HCOOH)。工业上利用甲酸的能量关系转换图如下:
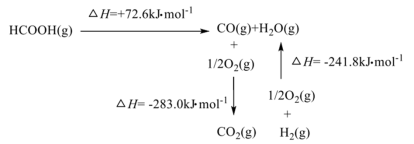
则:反应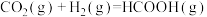 的焓变∆H=
的焓变∆H=_______ 。
(6) 溶液与1.95g锌粉在简易热量计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。
溶液与1.95g锌粉在简易热量计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。
已知: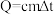 ,溶液的比热容近似为
,溶液的比热容近似为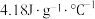 、溶液的密度近似为
、溶液的密度近似为 ,忽略溶液质量的变化、忽略金属吸收的热量。
,忽略溶液质量的变化、忽略金属吸收的热量。
①上述反应放出的热量数值为_______ J。
②请书写上述反应的热化学方程式(以离子方程式形式表示)_______ 。

(1)A是用CaCO3制取CO2的装置。写出A中发生反应的离子方程式:
(2)按要求填写表中空格:
| 仪器编号 | 盛放的试剂(焰色反应均呈黄色) | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | 与CO2反应,产生O2 | |
| D | 吸收未反应的CO2气体 |

则加入盐酸之前D中溶质的成分以及对应物质的量之比是
(4)为了达到实验目的,是否需要在B装置之后增加一个吸收水蒸气的装置,请说明理由:
(5)研究发现,一定条件下CO2加氢可制备甲酸(HCOOH)。工业上利用甲酸的能量关系转换图如下:

则:反应
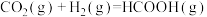 的焓变∆H=
的焓变∆H=(6)
 溶液与1.95g锌粉在简易热量计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。
溶液与1.95g锌粉在简易热量计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。已知:
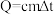 ,溶液的比热容近似为
,溶液的比热容近似为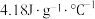 、溶液的密度近似为
、溶液的密度近似为 ,忽略溶液质量的变化、忽略金属吸收的热量。
,忽略溶液质量的变化、忽略金属吸收的热量。①上述反应放出的热量数值为
②请书写上述反应的热化学方程式(以离子方程式形式表示)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某校化学实验兴趣小组为了探究 和浓盐酸反应制备
和浓盐酸反应制备 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。已知:氯气、溴单质、碘单质都易溶于有机溶剂。
挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。已知:氯气、溴单质、碘单质都易溶于有机溶剂。

(1)A中制备氯气的化学反应方程式为:_____ 。
(2)若用含有
 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得的
,制得的 体积总是小于理论值的原因是
体积总是小于理论值的原因是_____ 。
(3)①装置B中盛放的药品为_____ 。
②装置D和E中出现的不同现象说明_____ 。
③装置F的作用是_____ 。
(4)乙同学认为甲同学的实验有缺陷,不能确保最终通入 溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入 溶液的气体只有一种,乙同学提出在F与G之间加一个检验装置,装置中应放
溶液的气体只有一种,乙同学提出在F与G之间加一个检验装置,装置中应放_____ 。
A. 溶液 B.湿润的淀粉
溶液 B.湿润的淀粉 试纸 C.浓硫酸
试纸 C.浓硫酸
 和浓盐酸反应制备
和浓盐酸反应制备 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。已知:氯气、溴单质、碘单质都易溶于有机溶剂。
挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。已知:氯气、溴单质、碘单质都易溶于有机溶剂。
(1)A中制备氯气的化学反应方程式为:
(2)若用含有

 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得的
,制得的 体积总是小于理论值的原因是
体积总是小于理论值的原因是(3)①装置B中盛放的药品为
②装置D和E中出现的不同现象说明
③装置F的作用是
(4)乙同学认为甲同学的实验有缺陷,不能确保最终通入
 溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入 溶液的气体只有一种,乙同学提出在F与G之间加一个检验装置,装置中应放
溶液的气体只有一种,乙同学提出在F与G之间加一个检验装置,装置中应放A.
 溶液 B.湿润的淀粉
溶液 B.湿润的淀粉 试纸 C.浓硫酸
试纸 C.浓硫酸
您最近一年使用:0次



