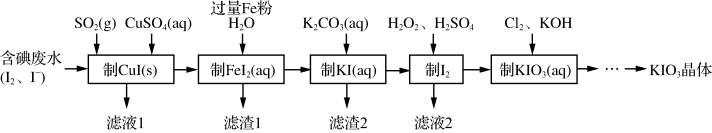
步骤1:在0.750 0 g试样中加入100.00 mL 0.120 0 mol·L-1 KMnO4的酸性溶液,加热,硫元素全部转化为SO42-,铜元素全部转化为Cu2+,滤去不溶性杂质。
步骤2:收集步骤1所得滤液至250 mL容量瓶中,定容。取25.00 mL溶液,用0.100 0 mol·L-1FeSO4溶液滴定至终点,消耗16.00 mL。
步骤3:在步骤2滴定所得溶液中滴加氨水至出现沉淀,然后加入适量NH4HF2溶液(使Fe、Mn元素不参与后续反应),加入约1 g KI固体(过量),轻摇使之溶解并发生反应:2Cu2++4I-===2CuI↓+I2。用0.050 00 mol·L-1 Na2S2O3溶液滴定至终点(离子方程式为2S2O32-+I2===2I-+S4O
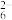 ),消耗14.00 mL。
),消耗14.00 mL。已知:酸性条件下,MnO4-的还原产物为Mn2+。
(1)若步骤3加入氨水产生沉淀时,溶液的pH=2.0,则溶液中c(Fe3+)=________。
(已知室温下Ksp[Fe(OH)3]=2.6×10-39)
(2)步骤3若未除去Fe3+,则测得的Cu2+的物质的量将________(填“偏高”“偏低”或“不变”)。
(3)计算试样中Cu2S和CuS的质量分数(写出计算过程)。
相似题推荐
(1)混合溶液中H+、Cu2+、
 的物质的量浓度分别为:
的物质的量浓度分别为:(2)向溶液中加入铁粉,足够长的时间后,铁粉有剩余,过滤,此时滤液中的Fe2+的物质的量浓度为
(3)取100mL该滤液,向其中加入适量硝酸,再加入足量氢氧化钠溶液,有红褐色沉淀生成。过滤,加热沉淀物至质量不再变化,得到红棕色的残渣。写出残渣的化学式
(1)反应后硫酸的物质的量浓度为
(2)原红色固体粉末中Fe2O3的物质的量为
步骤1:称取1.9640g该配合物晶体,配制成250.00mL溶液。
步骤2:取所配溶液25.00mL于锥形瓶中,加入1mol·L-1硫酸5.0mL,加热到70~85℃,用0.0100mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液48.00mL。
步骤3:向反应后的溶液中加入一定量锌粉。加热至黄色恰好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
步骤4:继续用0.0100mol·L-1KMnO4溶液滴定步骤3所得溶液至终点,消耗KMnO4溶液8.00mL。
(1)步骤2中,KMnO4将C2O
 氧化为CO2,该滴定反应的离子方程式为
氧化为CO2,该滴定反应的离子方程式为(2)步骤3中黄色消失的原因是
(3)配制配合物溶液的过程中,若定容时俯视容量瓶的刻度线,则最终所得晶体组成中水的含量
(4)通过计算确定该三价铁配合物的化学式
(1)FeOCl常用作过碳酸钠分解时的催化剂。FeCl3·6H2O在250℃时分解可得到FeOCl、HCl、H2O,写出该反应的化学方程式:
(2)测定氧泡泡样品中过碳酸钠化学式的实验步骤如下(样品中其他物质不参加反应):
步骤Ⅰ:用电子天平称取两份等质量的样品。
步骤Ⅱ:将一份置于锥形瓶中,加水溶解,用甲基橙作指示剂,用0.2mol·L-1H2SO4溶液滴定至终点,消耗硫酸25.00mL。
步骤Ⅲ:将另一份加水溶解后用稀硫酸酸化,用0.1mol·L-1KMnO4溶液滴定至终点(2MnO
 +5H2O2+6H+=2Mn2++5O2↑+8H2O),消耗KMnO4溶液30.00mL。
+5H2O2+6H+=2Mn2++5O2↑+8H2O),消耗KMnO4溶液30.00mL。①步骤Ⅱ中,滴定终点的现象是
②步骤Ⅲ中,0.1mol·L-1KMnO4溶液盛放在
a.样品溶于水酸化后放置一段时间,然后再进行滴定
b.滴定结束时,仰视滴定管读数
c.滴定前尖嘴部分有气泡,滴定后尖嘴部分充满KMnO4溶液
③通过计算确定该过碳酸钠化学式
(1)在进行饮用水消毒时,ClO2可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,据此说明ClO2具有
(2)液氯也常用作自来水消毒。已知ClO2、Cl2的还原产物均为Cl-,则相同物质的量的ClO2的消毒效率是Cl2的
(3)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg·L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
操作Ⅰ:取一定体积的水样,加入一定量的碘化钾,使碘游离出来。已知:8HCl + 2ClO2 + 10KI === 5I2 + 10KCl + 4H2O。
操作Ⅱ: 加入一定量的Na2S2O3溶液。(已知:2Na2S2O3+I2===Na2S4O6+2NaI)
请回答:
①操作Ⅰ中反应的离子方程式是
②若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10-3 mol·L-1的Na2S2O3溶液10 mL,则水样中ClO2的浓度是
【推荐1】根据题目提供的溶度积数据进行计算并回答下列问题:
(1)已知25℃时,Ksp[Mg(OH)2]=5.6×10﹣12;酸碱指示剂百里酚蓝变色的pH范围如下:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25℃时,在Mg(OH)2饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为
(2)向50mL0.018mol•L﹣1的AgNO3溶液中加入50mL0.020mol•L﹣1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.0×10﹣10,忽略溶液的体积变化,请计算:
①完全沉淀后,溶液中c(Ag+)=
②完全沉淀后,溶液的pH=
③如果向完全沉淀后的溶液中继续加入50mL0.001mol•L﹣1的盐酸,是否有白色沉淀生成?
(3)在某温度下,Ksp(FeS)=6.25×10﹣18,FeS饱和溶液中c(H+)与c(S2﹣)之间存在关系:c2(H+)•c(S2﹣)=1.0×10﹣22,为了使溶液里c(Fe2+)达到1mol•L﹣1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)约为
(1)氯化银在水中存在沉淀溶解平衡:AgCl
 Ag++Cl-。25℃时,氯化银的Ksp(AgCl)=1.8×10-10。现将足量氯化银分别放入下列溶液:①100mL蒸馏水中;②100mL0.1mol·L-1盐酸中;③100mL0.1mol·L-1氯化铝溶液中;④100mL0.1mol·L-1氯化镁溶液中。充分搅拌后,相同温度下,银离子浓度由大到小的顺序是
Ag++Cl-。25℃时,氯化银的Ksp(AgCl)=1.8×10-10。现将足量氯化银分别放入下列溶液:①100mL蒸馏水中;②100mL0.1mol·L-1盐酸中;③100mL0.1mol·L-1氯化铝溶液中;④100mL0.1mol·L-1氯化镁溶液中。充分搅拌后,相同温度下,银离子浓度由大到小的顺序是(2)25℃时,1L水中约能溶解2.4×10-3g硫酸钡。
①试计算25℃时硫酸钡的溶度积Ksp(BaSO4)=
②当人体中钡离子浓度达到2×10-3mol·L-1时会影响健康,那么硫酸钡可作为“钡餐”的原因是
③在25℃时,1L水中约能溶解0.018g碳酸钡,且胃液是酸性的,碳酸钡不能代替硫酸钡作为“钡餐”的理由是
(3)锅炉水垢会降低燃料利用率,还会形成安全隐患,因此要定期除去锅炉水垢。水垢中含有CaSO4[Ksp(CaSO4)=7.10×10-5],若用1mol·L-1碳酸钠溶液处理,使之转化为疏松、易溶于酸的CacCO3[Ksp(CaCO3)=4.96×10-9],试利用Ksp计算反应的平衡常数说明这一转化的原理
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V(NaOH)/mL | 13.00 | 12.90 | 11.40 | 13.10 |
(1)配制100 mL 1.0 mol/L的稀盐酸,需要2.5 mol/L的盐酸的体积为
(2)药片中碳酸钙的质量分数为
(1)18.4mol/L(质量分数0.98,密度1.84g/cm3)浓硫酸是常用的干燥剂,用于吸收潮湿气体中的水蒸气。当浓硫酸浓度降到16 mol/L(密度1.8g/cm3)以下时,则失去干燥能力。
①16 mol/L的硫酸的质量分数为
②50mL质量分数为0.98的浓硫酸作为干燥剂时,最多可吸水
(2)将铁粉与硫粉在隔绝空气条件下反应所得的固体M 9.920 g,与足量稀硫酸反应,收集到气体2.688 L(换算到标准状况),质量为3.440 g。则固体M的成分为
(3)当代硫酸工业大多用接触法制硫酸(设空气中氧气的体积分数为0.20)。
①为使黄铁矿煅烧充分,常通入过量40%的空气,则煅烧后炉气中SO2的体积分数为
②将①中的炉气经净化除尘后直接送入接触室,流量为1.00m3/s,从接触室导出气体的流量为0.95m3/s(同温同压下测定),则SO2的转化率为
(4)接触法制硫酸排放的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2(循环利用)和混合铵盐。为测定此铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
部分测定结果如下:
铵盐质量为10.000 g和20.000 g时,浓硫酸增加的质量相同;
铵盐质量为30.000 g时,浓硫酸质量增重0.680 g;
铵盐质量为40.000 g时,浓硫酸的质量不变。
①计算该混合盐中氮元素的质量分数
②计算上述氢氧化钠溶液的物质的量浓度