下列各选项中所述的两个量,前者一定大于后者的是
| A.室温下,1L0.3mol·L-1CH3COOH溶液和3L0.1 mol·L-1CH3COOH溶液中的H+数 |
| B.纯水在25℃和80℃时的pH |
| C.在NH3+NO→N2+H2O反应中,被氧化和被还原的N原子数 |
| D.相同条件下,H2分别与Cl2、F2反应的反应速率 |
13-14高二·四川·期中 查看更多[5]
夯基提能2020届高三化学选择题对题专练——氧化还原反应的综合分析(基础过关)安徽省合肥第六中学2017-2018学年高二下学期期中考试(理科)化学试题2016届云南省玉溪一中高三第一次月考试题化学试卷2016届山东省临清二中新高三开学初模拟检测化学试卷(已下线)2013-2014四川省宜昌市部分市级示范高中春季期中考试高二化学试卷
更新时间:2016-12-09 08:38:31
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】美、德两国成功合成具有化学特性的氢铝化合物(AlH3)n,关于氢铝化合物的推测不正确的是
| A.氢铝化合物与水反应生成氢氧化铝和氢气 |
| B.与H2O反应生成2.24 LH2(标况下),转移的电子为0.2 mol |
| C.氢铝化合物中氢显-1价 |
| D.氢铝化合物具有强还原性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将几种铁的氧化物的混合物加入100mL、7mol∙L-1的盐酸中。氧化物恰好完全溶解,在所得的溶液中通入0.56L(标况)氯气时,恰好使溶液中的Fe2+完全转化为Fe3+,则该混合物中铁元素的质量分数为
| A.79.0% | B.75.4% | C.71.4% | D.63.6% |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某反应过程的能量变化如图所示,下列说法错误的是( )


| A.该反应为放热反应,∆H>0 |
| B.反应过程b有催化剂参与 |
| C.反应过程a的活化能大于E1 |
| D.该反应可能需要加热才能发生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,发生如下反应:PCl5(g)⇌PCl3(g)+Cl2(g) ΔH=akJ·mol-1(a>0),0~10min保持容器温度不变,10min时改变一种条件,整个过程中PCl5、PCl3、Cl2的物质的量随时间的变化如图所示:
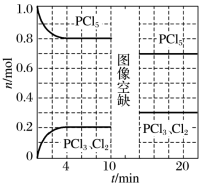
下列说法正确的是

下列说法正确的是
| A.0~4min的平均速率v(PCl3)=0.05mol·L-1·min-1 |
| B.4min反应达平衡时,吸收的热量为0.2akJ |
| C.10min时改变的条件是增加了一定量的PCl5 |
| D.增大压强,活化分子百分数增大,反应速率加快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列相关实验能达到预期目的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 可逆反应FeCl3(aq)+3KSCN(aq)⇌Fe(SCN)3(aq)+3KCl(aq)建立平衡后,在其它条件不变时,加入KCl固体,观察体系颜色的变化 | 验证浓度对化学平衡的影响 |
| B | 相同温度下,将等质量的大理石块、大理石粉末分别加入等体积、等浓度的盐酸和硫酸中,观察气泡产生的快慢 | 验证固体接触面积对化学反应速率的影响 |
| C | 相同温度下,两支试管中装有等体积、等浓度的H2O2溶液,向其中分别加入少量FeCl3固体和少量MnO2固体 | 验证不同催化剂对H2O2分解速率的影响 |
| D | 将SO2气体通入溴水中,观察溶液颜色的变化 | 证明SO2具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设 为阿伏加德罗常数的值.下列说法正确的是
为阿伏加德罗常数的值.下列说法正确的是
 为阿伏加德罗常数的值.下列说法正确的是
为阿伏加德罗常数的值.下列说法正确的是A.常温下,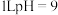 的 的 溶液中,由水电离出的 溶液中,由水电离出的 数目为 数目为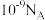 |
B. 重水 重水 中所含质子数、中子数各为 中所含质子数、中子数各为 |
C.标准状况下,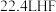 中 中 数目为 数目为 |
D. 和 和 于密闭容器中充分反应后, 于密闭容器中充分反应后, 分子数为 分子数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于电解质溶液归纳总结正确的是
①将等浓度的硫酸和醋酸均升高相同温度(不考虑醋酸的挥发)二者pH均增大
②t℃时,pH=6的溶液中,
③将KCl溶液从常温加热到80℃,溶液的pH变小,但仍然呈中性
④常温下,甲、乙都是强电解质,已知甲溶液的pH是乙溶液pH的两倍,则甲、乙溶液等体积混合,混合液的pH可能等于7
⑤常温下,由水电离出的 ,则该溶液可能是稀盐酸
,则该溶液可能是稀盐酸
⑥用湿润的pH试纸分别测量 和
和 的pH值,
的pH值, 的误差大
的误差大
⑦用pH试纸测量NaClO溶液的pH值为11
⑧常温下pH=10的某碱溶液,取1mL稀释到100mL,稀释后pH为a,则a≥12
⑨某温度下纯水中 ,则该温度下0.1mol/L的盐酸的pH=1
,则该温度下0.1mol/L的盐酸的pH=1
①将等浓度的硫酸和醋酸均升高相同温度(不考虑醋酸的挥发)二者pH均增大
②t℃时,pH=6的溶液中,

③将KCl溶液从常温加热到80℃,溶液的pH变小,但仍然呈中性
④常温下,甲、乙都是强电解质,已知甲溶液的pH是乙溶液pH的两倍,则甲、乙溶液等体积混合,混合液的pH可能等于7
⑤常温下,由水电离出的
 ,则该溶液可能是稀盐酸
,则该溶液可能是稀盐酸⑥用湿润的pH试纸分别测量
 和
和 的pH值,
的pH值, 的误差大
的误差大⑦用pH试纸测量NaClO溶液的pH值为11
⑧常温下pH=10的某碱溶液,取1mL稀释到100mL,稀释后pH为a,则a≥12
⑨某温度下纯水中
 ,则该温度下0.1mol/L的盐酸的pH=1
,则该温度下0.1mol/L的盐酸的pH=1| A.③④⑤⑨ | B.①②④⑧ | C.③⑤⑥⑦ | D.④⑥⑧⑨ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,向20mL0.1mol/L氨水中滴加盐酸,溶液中由水电离出的c(H+)随加入盐酸体积的变化如图所示。则下列说法正确的是
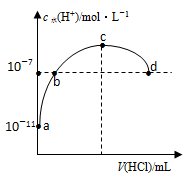

| A.b、d两点为恰好完全反应点 |
B.c点溶液中,c( )=c(Cl-) )=c(Cl-) |
C.a、b之间的任意一点:c(Cl-)>c( ),c(H+)>c(OH-) ),c(H+)>c(OH-) |
| D.常温下,0.1mol/L氨水的电离常数K约为1×10-5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温时,下列说法正确的是
| A.pH=11的氨水和pH=11的Na2CO3溶液中,由水电离产生的c(OH-)均为1×10−11 mol·L−1 |
| B.分别把100 mL pH=11的NaOH溶液和pH=11的氨水加水稀释至1 L,所得溶液pH均为10 |
| C.分别向等体积的0.1 mol·L−1 HCl溶液和0.1 mol·L−1 CH3COOH溶液中加入等浓度的NaOH溶液,恰好为中性时,消耗NaOH溶液的体积相等 |
| D.分别向1 mL pH=3的盐酸和pH=3的CH3COOH溶液中加入少量CH3COONa固体,两溶液的pH均增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于NH4Cl溶液的相关叙述不正确的是( )
| A.0.2mol/LNH4Cl溶液:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B.NH4Cl溶液中:c(Cl-)=c(NH4+)+c(NH3·H2O) |
| C.将NH4C1溶解到氨水中,NH4C1抑制NH3·H2O的电离 |
| D.等物质的量浓度的NH4C1、CH3COONH4溶液中c(NH4+)相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】PAR(用H2R表示)是常用的显色剂和指示剂,在水溶液中以H3R+、H2R、HR-、R2-四种形式存在。关于室温下0.05 mol/LH2R溶液说法错误的是
| A.溶液pH>1 |
B.溶液中存在关系: |
| C.溶液中加入PAR晶体,PAR的电离平衡正向移动,电离度减小 |
| D.该溶液既能和酸反应,又能和碱反应 |
您最近一年使用:0次



