Ⅰ、A、B、C、D是原子序数均小于20的四种元素。A与B同主族,且能形成BA2、BA3两种化合物。B、C、D所形成的简单离子电子层结构相同,且B、C、D离子半径依次减小。请回答下列问题:
①D元素在元素周期表中的位置是______________ 。
②A与D所形成的化合物的电子式为___________________ 。
③将C单质的水溶液滴加到B与D所形成化合物的水溶液中,其反应的化学方程式为_______________ 。
Ⅱ、由短周期元素组成的中学常见的含钠元素的物质A、B、C、D,存在如图转化关系(部分生成物和反应条件已略去)。

(1)若A为金属钠, A与水反应的离子方程式为______________________ 。
(2)若A为过氧化钠, A与水反应的化学方程式为____________________ 。
(3)A不论是Na还是Na2O2,依据转化关系判断物质D是_______________ ,
(4)向30ml某浓度的B溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况(不计CO2的溶解),则曲线B表明M中的溶质为______________ ;原NaOH溶液的物质的量浓度为__________ ;由曲线A、B可知,两次实验通入的CO2的体积比为___________ 。
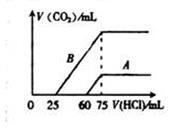
(5)请你设计一实验证明Na2CO3溶液碱性比NaHCO3溶液的碱性强:__________________ 。
①D元素在元素周期表中的位置是
②A与D所形成的化合物的电子式为
③将C单质的水溶液滴加到B与D所形成化合物的水溶液中,其反应的化学方程式为
Ⅱ、由短周期元素组成的中学常见的含钠元素的物质A、B、C、D,存在如图转化关系(部分生成物和反应条件已略去)。

(1)若A为金属钠, A与水反应的离子方程式为
(2)若A为过氧化钠, A与水反应的化学方程式为
(3)A不论是Na还是Na2O2,依据转化关系判断物质D是
(4)向30ml某浓度的B溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况(不计CO2的溶解),则曲线B表明M中的溶质为

(5)请你设计一实验证明Na2CO3溶液碱性比NaHCO3溶液的碱性强:
更新时间:2016-12-09 10:16:32
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】元素及其化合物的知识是“化学I”的重点内容。A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示:
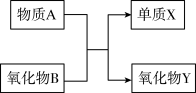
试写出符合下列条件的化学方程式:
(1)若物质A为氧化物:_________ ;
(2)若A为金属单质,B为金属氧化物:_______ ;
(3)若A为金属单质,B为非金属氧化物:__________ ;
(4)若A和X均为非金属单质:________ ;

试写出符合下列条件的化学方程式:
(1)若物质A为氧化物:
(2)若A为金属单质,B为金属氧化物:
(3)若A为金属单质,B为非金属氧化物:
(4)若A和X均为非金属单质:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】NBICS化学学习小组为探究由三种元素构成的化合物X的组成和性质,设计并完成如下实验(假设各步反应均完全,反应中气体完全逸出),已知B为气体,E的焰色为黄色,C为两种正盐的混合物
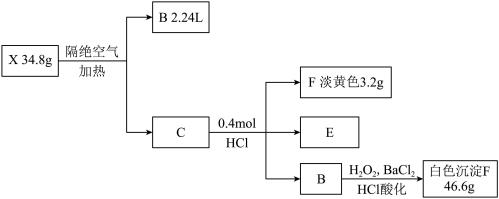
请回答下列问题:
(1)固体X的化学式是___________
(2)写出X受热分解的化学方程式:___________ 。
(3)写出混合物C与稀硫酸反应产生F的离子方程式:___________ 。
(4)请设计实验方案,检验气体B常见的化学性质(三种):___________ 。

请回答下列问题:
(1)固体X的化学式是
(2)写出X受热分解的化学方程式:
(3)写出混合物C与稀硫酸反应产生F的离子方程式:
(4)请设计实验方案,检验气体B常见的化学性质(三种):
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】金属铝在酸性或碱性溶液中均可与 发生氧化还原反应,转化关系如图所示:
发生氧化还原反应,转化关系如图所示:
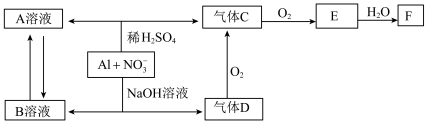
请回答下列问题:
(1)气体D和F反应可生成盐,该盐的化学名称为_____________ 。
(2)C、E排入大气中会造成大气污染,在催化剂存在的情况下,D可以将C、E还原为无毒的气态单质,该单质是_____________ (填化学式)。
(3)将B转化为 的最佳试剂是
的最佳试剂是_____________ (填字母)。
a.CO2 b.NaOH c.HCl d.NH3·H2O
(4)写出D→C反应的化学方程式:__________________________ 。
(5)Al与 在酸性条件下反应的离子方程式为:
在酸性条件下反应的离子方程式为:__________________________ 。
(6)Al与 在碱性条件下反应,Al与被还原的
在碱性条件下反应,Al与被还原的 的物质的量之比为
的物质的量之比为_____________ 。
 发生氧化还原反应,转化关系如图所示:
发生氧化还原反应,转化关系如图所示:
请回答下列问题:
(1)气体D和F反应可生成盐,该盐的化学名称为
(2)C、E排入大气中会造成大气污染,在催化剂存在的情况下,D可以将C、E还原为无毒的气态单质,该单质是
(3)将B转化为
 的最佳试剂是
的最佳试剂是a.CO2 b.NaOH c.HCl d.NH3·H2O
(4)写出D→C反应的化学方程式:
(5)Al与
 在酸性条件下反应的离子方程式为:
在酸性条件下反应的离子方程式为:(6)Al与
 在碱性条件下反应,Al与被还原的
在碱性条件下反应,Al与被还原的 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C是由周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图1所示的关系,完成下列空白:
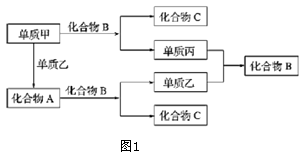
(1)向酚酞试液中加入化合物A的粉末,现象为_____________ 。
(2)单质甲与化合物B反应的离子方程式为_______________ 。
(3)向20mL某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图2图示两种情况。
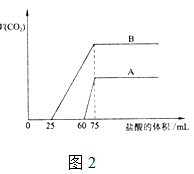
①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为_________ 。
②由B表明,原溶液通入CO2气体后,所得溶液中的溶质的化学式为________ 。
③由A、B可知,两次实验通入的CO2的体积比为__________ 。

(1)向酚酞试液中加入化合物A的粉末,现象为
(2)单质甲与化合物B反应的离子方程式为
(3)向20mL某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图2图示两种情况。

①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为
②由B表明,原溶液通入CO2气体后,所得溶液中的溶质的化学式为
③由A、B可知,两次实验通入的CO2的体积比为
您最近一年使用:0次
【推荐2】回答下列问题:
(1)为鉴定硅产品中是否含有微量铁单质,将硅产品用稀盐酸溶解,取上层清液后需要加入的试剂是_____________ (填字母代号)。
a.氯水 b.NaOH溶液 c.KSCN溶液 d.Na2SO3溶液
(2)用下图装置来验证浓硫酸与木炭在加热条件下反应的产物中含有SO2和CO2。
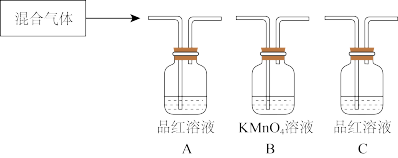
①可观察到A瓶溶液中的现象为__________________________ 。
②写出B瓶中的离子反应方程式为__________________________ 。
③C瓶溶液的作用是___________________________ 。
(3)取A、B两份物质的量浓度相等的NaOH溶液,体积均为50mL,分别向其中通入一定量的CO2后,再分别稀释为100mL,在稀释后的溶液中分别逐滴加入0.1mol·L-1的盐酸,产生的CO2的体积(标准状况)与所加盐酸的体积关系如图所示:
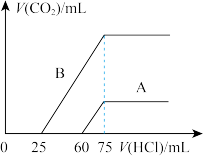
①A曲线表明,原NaOH溶液通入CO2后,所得溶液中的溶质的化学式为______ 。
②对B曲线来说,写出横坐标上0~25 mL这一段反应的离子方程式_________ 。
(1)为鉴定硅产品中是否含有微量铁单质,将硅产品用稀盐酸溶解,取上层清液后需要加入的试剂是
a.氯水 b.NaOH溶液 c.KSCN溶液 d.Na2SO3溶液
(2)用下图装置来验证浓硫酸与木炭在加热条件下反应的产物中含有SO2和CO2。

①可观察到A瓶溶液中的现象为
②写出B瓶中的离子反应方程式为
③C瓶溶液的作用是
(3)取A、B两份物质的量浓度相等的NaOH溶液,体积均为50mL,分别向其中通入一定量的CO2后,再分别稀释为100mL,在稀释后的溶液中分别逐滴加入0.1mol·L-1的盐酸,产生的CO2的体积(标准状况)与所加盐酸的体积关系如图所示:

①A曲线表明,原NaOH溶液通入CO2后,所得溶液中的溶质的化学式为
②对B曲线来说,写出横坐标上0~25 mL这一段反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】碳酸钠是一种重要的化工原料,在生产、生活和实验研究中均有广泛应用。下面是与碳酸钠溶液相关问题的探讨,请按要求回答问题。
(1)实验室需配制240 mL 1.5 mol/LNa2CO3溶液,请回答下列问题:
①实验中除了用到托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管外,还需用到的玻璃仪器有_______ 。
②通过计算可知,该实验需要用托盘天平称量_______ g Na2CO3·10H2O。
③经测定实际配得溶液的浓度为1.4 mol/L,原因不可能_______ (填序号)。
a.转移溶液前容量瓶内有少量蒸馏水 b.定容摇匀后,发现液面下降,继续加水至刻度线
c.转移溶液后未洗涤烧杯 d.定容时俯视刻度线
(2)FeCO3与砂糖混用可以作补血剂,工业上用Na2CO3溶液和FeSO4溶液发生复分解反应制备。(已知溶液pH大于8.8时,Fe2+转化为Fe(OH)2沉淀,实验中所用Na2CO3溶液的pH=10)。
①在烧杯中混合上述溶液制备 FeCO3沉淀时的具体操作为_______ 。
②将FeSO4溶液缓慢加入到盛有NaHCO3溶液的烧杯中也能得到FeCO3沉淀,同时在实验中观察到有无色无味的气体产生,该反应的离子方程式为_______ 。
(3)某同学在常温下,向100 mL NaOH溶液中通入一定量的CO2气体制备Na2CO3溶液。为测定溶液成分,该同学向所得溶液中逐滴加入0.3 mol/L的盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图所示。请你帮他仔细分析实验结果。
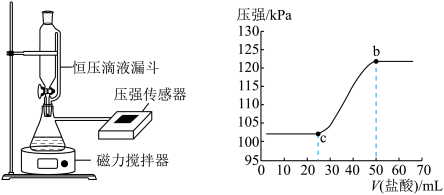
①该同学所得溶液的溶质成分为_______ 。
②该同学使用的NaOH溶液的物质的量浓度不低于_______ mol/L
(1)实验室需配制240 mL 1.5 mol/LNa2CO3溶液,请回答下列问题:
①实验中除了用到托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管外,还需用到的玻璃仪器有
②通过计算可知,该实验需要用托盘天平称量
③经测定实际配得溶液的浓度为1.4 mol/L,原因不可能
a.转移溶液前容量瓶内有少量蒸馏水 b.定容摇匀后,发现液面下降,继续加水至刻度线
c.转移溶液后未洗涤烧杯 d.定容时俯视刻度线
(2)FeCO3与砂糖混用可以作补血剂,工业上用Na2CO3溶液和FeSO4溶液发生复分解反应制备。(已知溶液pH大于8.8时,Fe2+转化为Fe(OH)2沉淀,实验中所用Na2CO3溶液的pH=10)。
①在烧杯中混合上述溶液制备 FeCO3沉淀时的具体操作为
②将FeSO4溶液缓慢加入到盛有NaHCO3溶液的烧杯中也能得到FeCO3沉淀,同时在实验中观察到有无色无味的气体产生,该反应的离子方程式为
(3)某同学在常温下,向100 mL NaOH溶液中通入一定量的CO2气体制备Na2CO3溶液。为测定溶液成分,该同学向所得溶液中逐滴加入0.3 mol/L的盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图所示。请你帮他仔细分析实验结果。

①该同学所得溶液的溶质成分为
②该同学使用的NaOH溶液的物质的量浓度不低于
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】下图中的每一个方格表示有关的一种反应物或生成物,其中A、C为无色气体
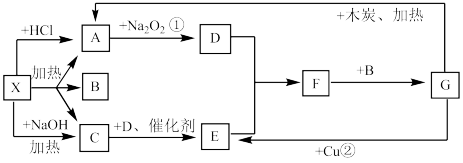
(1)写出有关物质的化学式X:_______ ;F_______
(2)写出A→D的化学方程式____________
(3)写出实验室制备C的化学方程式_______
(4)C可用于制备尿素,尿素CO(NH2)2适用于各种土壤,在土壤中尿素发生水解,生成两种气体,其水解的化学方程式是______
(5)分别取两份50mLNaOH溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入0.1mol/L的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl的体积之间的关系如图所示,试分析:
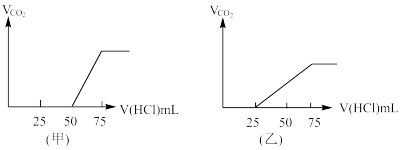
①NaOH在吸收A气体后,乙图所示溶液中存在的溶质是:_____ ,其物质的量之比是:_________
②原NaOH溶液的物质的量浓度是_______ mol/L,甲图所示溶液最多还能吸收A体积为_____ mL(标准状况)。

(1)写出有关物质的化学式X:
(2)写出A→D的化学方程式
(3)写出实验室制备C的化学方程式
(4)C可用于制备尿素,尿素CO(NH2)2适用于各种土壤,在土壤中尿素发生水解,生成两种气体,其水解的化学方程式是
(5)分别取两份50mLNaOH溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入0.1mol/L的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl的体积之间的关系如图所示,试分析:

①NaOH在吸收A气体后,乙图所示溶液中存在的溶质是:
②原NaOH溶液的物质的量浓度是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】往100mL的NaOH溶液中通入 充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M。通入的
充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M。通入的 的体积V(标准状况)与M的质量W的关系如下图所示。试解答下列问题:
的体积V(标准状况)与M的质量W的关系如下图所示。试解答下列问题:
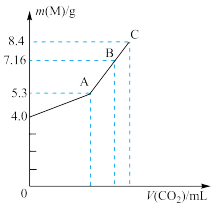
(1)A点时,白色固体M的化学式为_________ ,通入的 的体积为
的体积为_________ mL(标准状况下,下同)。
(2)C点时,白色固体M的化学式为__________ ,通入的 的体积为
的体积为__________ mL。
(3)B点时M的组成成分为_________ ,物质的量之比为_________ ,通入的 的体积为
的体积为__________ mL。
(4)该NaOH溶液的物质的量浓度为_________ 。
 充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M。通入的
充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M。通入的 的体积V(标准状况)与M的质量W的关系如下图所示。试解答下列问题:
的体积V(标准状况)与M的质量W的关系如下图所示。试解答下列问题:
(1)A点时,白色固体M的化学式为
 的体积为
的体积为(2)C点时,白色固体M的化学式为
 的体积为
的体积为(3)B点时M的组成成分为
 的体积为
的体积为(4)该NaOH溶液的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】现有NaCl、Na2CO3·10H2O和NaHCO3三种固体组成的混合物,为了测定各组分的含量,设计如下实验,取一定质量的样品,测量反应前后②和③装置质量的变化,可以计算出各组分的含量。

(1)U形管①中装有碱石灰,作用是___________ ;
(2)U形管②的作用是___________ ;U形管③中装有___________ ;
(3)球形干燥管中盛装碱石灰的作用是___________ ,若取消球形干燥管,则会使___________ 的质量分数偏高。
(4)若将U形管①换成装有NaOH溶液的洗气瓶,则会使测得的NaCl的含量___________ (填“偏高、偏低、无影响”)。
(5)硬质玻璃管在加热前,应关闭___________ (填 a 或 b,下同),打开___________ ,再___________ ,至排出的气体不再使澄清石灰水变浑浊。
(6)写出 NaHCO3 受热分解的反应式______
(7)若实验结束后,装置②增加5.4g,装置③增加8.8g,则可计算原混合物中Na2CO3·10H2O的质量为___________ g 。

(1)U形管①中装有碱石灰,作用是
(2)U形管②的作用是
(3)球形干燥管中盛装碱石灰的作用是
(4)若将U形管①换成装有NaOH溶液的洗气瓶,则会使测得的NaCl的含量
(5)硬质玻璃管在加热前,应关闭
(6)写出 NaHCO3 受热分解的反应式
(7)若实验结束后,装置②增加5.4g,装置③增加8.8g,则可计算原混合物中Na2CO3·10H2O的质量为
您最近一年使用:0次



