榴石矿石可以看作由CaO、FeO、Fe2O3、Al2O3、SiO2组成。工业上对其进行综合利用的流程如下:
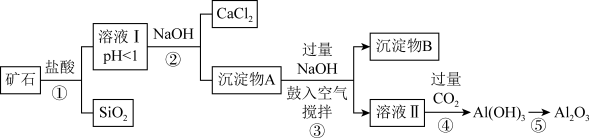
(1)溶液Ⅰ中除了Ca2+外,还可能含有的金属阳离子有__________________ ;
(2)步骤③中NaOH参加反应的离子方程式____________________________ ,鼓入空气并充分搅拌的目的是(用化学方程式表示)____________________ ;
(3)在工业生产中,步骤④通入过量CO2而不加入盐酸的原因是_____________________ 。

(1)溶液Ⅰ中除了Ca2+外,还可能含有的金属阳离子有
(2)步骤③中NaOH参加反应的离子方程式
(3)在工业生产中,步骤④通入过量CO2而不加入盐酸的原因是
更新时间:2016-12-09 10:43:29
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】铬铁矿的成分主要为FeCr2O4,另含有少量Al2O3和SiO2。从铬铁矿中提取铁、铬的化合物,并获得副产物的工艺流程如下:
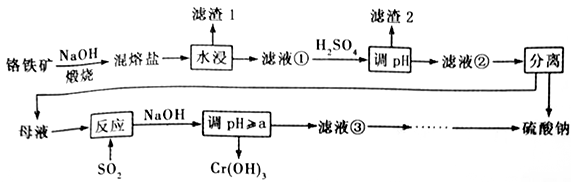
已知“混熔盐”中含有Na2CrO4和NaFeO2,其中NaFeO2极易水解。试回答下列问题:
(1)“滤渣1”为红褐色沉淀,其化学式为_________________ ;向滤液①中加H2SO4“调pH”的目的:一是使CrO42-转化为Cr2O72- ;二是____________________________ 。
(2)“煅烧”铬铁矿时,主要反应的化学方程式为_______________________________ 。
(3)根据右图溶解度(S)~温度(T)曲线判断,对滤液②进行的最佳“分离”方法为_________ (填序号)。
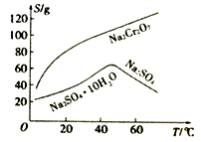
A.蒸发结晶 B.蒸发浓缩,趁热过滤 C.蒸发浓缩,冷却结晶,过滤
(4)“反应”的离子方程式为_______________________________ 。
(5)Cr(OH)3溶于盐酸生成配离子[CrCln(H2O) 6-n]x+。0.0015 mol [CrCln(H2O) 6-n]x+与氢离子交换树脂(HR)完全发生离子交换:
[CrCln(H2O) 6-n]x++xHR→Rx[CrCln(H2O) 6-n]+xH+,生成的H+可与25.00 mL0.1200 mol·L -1NaOH溶液恰好中和。则该配离子的化学式为__________________ 。
(6)已知25℃时,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=1.0×10-32。则使Cr3+恰好完全沉淀,即溶液中c(Cr3+) =1.0×10-5 mol·L -1时,应调节溶液pH的最小值a为多少? (列式计算)____________________________________________ 。

已知“混熔盐”中含有Na2CrO4和NaFeO2,其中NaFeO2极易水解。试回答下列问题:
(1)“滤渣1”为红褐色沉淀,其化学式为
(2)“煅烧”铬铁矿时,主要反应的化学方程式为
(3)根据右图溶解度(S)~温度(T)曲线判断,对滤液②进行的最佳“分离”方法为

A.蒸发结晶 B.蒸发浓缩,趁热过滤 C.蒸发浓缩,冷却结晶,过滤
(4)“反应”的离子方程式为
(5)Cr(OH)3溶于盐酸生成配离子[CrCln(H2O) 6-n]x+。0.0015 mol [CrCln(H2O) 6-n]x+与氢离子交换树脂(HR)完全发生离子交换:
[CrCln(H2O) 6-n]x++xHR→Rx[CrCln(H2O) 6-n]+xH+,生成的H+可与25.00 mL0.1200 mol·L -1NaOH溶液恰好中和。则该配离子的化学式为
(6)已知25℃时,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=1.0×10-32。则使Cr3+恰好完全沉淀,即溶液中c(Cr3+) =1.0×10-5 mol·L -1时,应调节溶液pH的最小值a为多少? (列式计算)
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】Cr(OH)3可用于油漆颜料及羊毛处理。工业上以高铁铬铁矿(主要成分为Cr2O3,含Fe2O3、SiO2、Al2O3等杂质)为原料生产Cr(OH)3和金属A1的工艺流程如图。回答下列问题:
已知:①焙烧时A12O3转化为可溶性的钠盐;
②“加入Na2S”析铬时,硫离子转化为 。
。
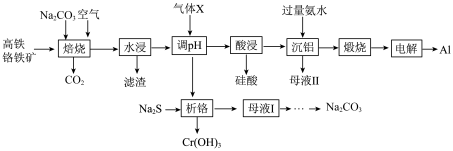
(1)为提高焙烧效率,可以采取的措施为________ (填一种方法即可);“焙烧时,Cr2O3转化为Na2CrO4,请写出该转化过程的化学方程式________ 。
(2)“水浸”后滤渣主要成分为________ (填化学式,下同)。
(3)“调pH”时通入的“气体X”是________ 。
(4)用稀硫酸进行“酸浸”后,再进行“沉铝”操作,所得的母液Ⅱ的主要成分为_______ 。
(5)过滤得到母液I经_______ 、________ 、过滤、洗涤、干燥得到碳酸钠晶体,失去结晶水得到碳酸钠固体。
(6)加入“Na2S”析铬, 被还原的离子方程式为
被还原的离子方程式为________ 。
已知:①焙烧时A12O3转化为可溶性的钠盐;
②“加入Na2S”析铬时,硫离子转化为
 。
。
(1)为提高焙烧效率,可以采取的措施为
(2)“水浸”后滤渣主要成分为
(3)“调pH”时通入的“气体X”是
(4)用稀硫酸进行“酸浸”后,再进行“沉铝”操作,所得的母液Ⅱ的主要成分为
(5)过滤得到母液I经
(6)加入“Na2S”析铬,
 被还原的离子方程式为
被还原的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】硼泥主要由MgO和SiO2组成,含有少量的Fe2O3,FeO、Al2O3等杂质。用硼泥生产氢氧化镁的工艺流程如图所示:

已知某些氢氧化物沉淀的PH如下表所示:
(1)MgO的电子式为____ 。
(2)滤渣2的主要成分是____ ,向滤渣2中继续加入过量的NaOH溶液,发生的离子方程式为______ 。
(3)加入NaOH调节pH=12.0时,发生的离子方程式为___________ 。
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为______ 。
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为__ (用含有a、b的代数式表示)。

已知某些氢氧化物沉淀的PH如下表所示:
| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
(1)MgO的电子式为
(2)滤渣2的主要成分是
(3)加入NaOH调节pH=12.0时,发生的离子方程式为
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:

(1)FeS2的化学名称为___________ ,在___________ 矿中含量丰富。
(2)焙烧过程中产生SO2的化学方程式为___________ ,用足量NaOH溶液吸收SO2的离子方程式为___________ 。
(3)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如图所示。
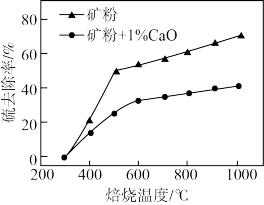
已知:多数金属硫酸盐的分解温度都高于600 ℃;硫去除率=(1- )×100%
)×100%
700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是___________ 。(用化学方程式解释)
(4)“碱浸”后的溶液中,铝元素存在的形式为___________ (填化学式),“过滤”所需的实验仪器有___________ 。
(5)“过滤”得到的滤渣中含大量的Fe2O3.Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应生成的n(Fe3O4)∶n(SO2)=___________ 。

(1)FeS2的化学名称为
(2)焙烧过程中产生SO2的化学方程式为
(3)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如图所示。

已知:多数金属硫酸盐的分解温度都高于600 ℃;硫去除率=(1-
 )×100%
)×100%700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是
(4)“碱浸”后的溶液中,铝元素存在的形式为
(5)“过滤”得到的滤渣中含大量的Fe2O3.Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应生成的n(Fe3O4)∶n(SO2)=
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】硅孔雀石是一种含铜矿石,含铜形态为CuCO3、Cu(OH)2和CuSiO3∙2H2O,同时含有SiO2、FeCO3、Fe2O3、A12O3等杂质。以其为原料制取硫酸铜的工艺流程如下图所示:
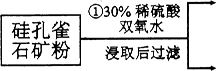

(1)步骤1中先加入足量稀硫酸,再加入双氧水。则双氧水参与该反应的离子方程式是_________________ 。
(2)步骤②调节溶液pH,可以选用的试剂是________ 。(填字母编号)
A.A12O3 B.CuO C.CuCO3·Cu(OH)2
(3)有关氢氧化物开始沉淀和完全沉淀的pH如下表:
则滤液B中含有的阳离子是__________________________ 。
(4)将滤液B通过_______ 、________ 、过滤等操作可得到硫酸铜晶体。
(5)硫酸铜也可用硫化铜和氧气在高温、催化剂条件下化合制得,该反应的化学方程式是______________ 。取384g CuS在一定条件下和氧气完全反应,若发生2CuS+3O2=2CuO+2SO2和4CuS+5O2=2Cu2O+4SO2两个反应,在所得固体中Cu和O的物质的量之比n(Cu):n(O)=4:a,此时消耗空气的物质的量为bmol。则a=__________ 。(氧气占空气体积的五分之一)
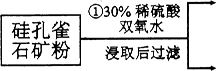

(1)步骤1中先加入足量稀硫酸,再加入双氧水。则双氧水参与该反应的离子方程式是
(2)步骤②调节溶液pH,可以选用的试剂是
A.A12O3 B.CuO C.CuCO3·Cu(OH)2
(3)有关氢氧化物开始沉淀和完全沉淀的pH如下表:
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |
则滤液B中含有的阳离子是
(4)将滤液B通过
(5)硫酸铜也可用硫化铜和氧气在高温、催化剂条件下化合制得,该反应的化学方程式是
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】我国是最早制得和使用金属锌的国家。一种以锌精矿(主要成分是ZnS,还有Fe3O4、CuO、PbO2等杂质)为原料制备锌的工艺流程如下:

已知: 25°C时相关物质的Ksp如下表:
回答下列问题:
(1)滤渣I的主要成分除过量MnO2外,还有S和___________ ( 填化学式)。“浸出” 时,MnO2氧化ZnS的离子方程式为___________ 。
(2)“沉铁”时,滴加氨水需要调节pH最低为___________ (残留在溶液中离子浓度≤10-5mol·L-1时,沉淀完全)。
(3)“萃取,反萃取”时发生的反应是
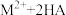 (有机萃取剂)
(有机萃取剂)
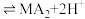 ,有机萃取剂可以分离ZnSO4和MnSO4.写出反萃取剂X的化学式
,有机萃取剂可以分离ZnSO4和MnSO4.写出反萃取剂X的化学式___________ 。
(4)“深度净化”中加Zn的目的是___________ 。
(5)用惰性电极电解ZnSO4溶液,“电解沉积” 后的溶液中可循环利用的物质为___________ 。
(6)锌元素位于元素周期表___________ 区,Zn的价层电子排布式为___________ 。
(7)S与
 形成的某化合物晶体的晶胞(实心点表示
形成的某化合物晶体的晶胞(实心点表示
 ,空心点表示S)如图所示:
,空心点表示S)如图所示:
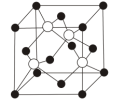
已知该晶胞的晶胞参数为 ,阿伏伽德罗常数为NA,则该晶胞的密度为
,阿伏伽德罗常数为NA,则该晶胞的密度为___________  。
。

已知: 25°C时相关物质的Ksp如下表:
| 物质 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | Cu(OH)2 |
| Ksp | 5×10-18 | 5×10-17 | 1×10-38 | 2× 10-13 | 2×10-20 |
(1)滤渣I的主要成分除过量MnO2外,还有S和
(2)“沉铁”时,滴加氨水需要调节pH最低为
(3)“萃取,反萃取”时发生的反应是
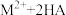 (有机萃取剂)
(有机萃取剂)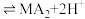 ,有机萃取剂可以分离ZnSO4和MnSO4.写出反萃取剂X的化学式
,有机萃取剂可以分离ZnSO4和MnSO4.写出反萃取剂X的化学式(4)“深度净化”中加Zn的目的是
(5)用惰性电极电解ZnSO4溶液,“电解沉积” 后的溶液中可循环利用的物质为
(6)锌元素位于元素周期表
(7)S与
 形成的某化合物晶体的晶胞(实心点表示
形成的某化合物晶体的晶胞(实心点表示 ,空心点表示S)如图所示:
,空心点表示S)如图所示:
已知该晶胞的晶胞参数为
 ,阿伏伽德罗常数为NA,则该晶胞的密度为
,阿伏伽德罗常数为NA,则该晶胞的密度为 。
。
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】辛烯醛是一种重要化工原料,某小组拟用正丁醛制备辛烯醛并探究其结构。制备实验:

已知:①正丁醛的沸点为 。辛烯醛沸点为
。辛烯醛沸点为 ,密度为
,密度为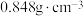 ,难溶于水。
,难溶于水。
②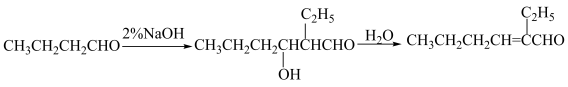
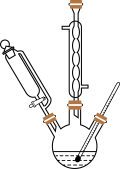
(1)在如图三颈烧瓶中加入 溶液,在充分搅拌下,从滴液漏斗慢慢滴入
溶液,在充分搅拌下,从滴液漏斗慢慢滴入 正丁醛。采用适宜加热方式是
正丁醛。采用适宜加热方式是_________ ;使用冷凝管的目的是_________ 。
(2)判断有机相已洗涤至中性的操作方法:_________ 。
(3)操作2的名称是_________ ;固体A的摩尔质量为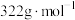 ,固体A的化学式为
,固体A的化学式为_________ 。
(4)利用“减压蒸馏”操作获取产品。温度计示数一定_________ (填“高于”“等于”或“低于”) 。
。
(5)为了证明辛烯醛含有碳碳双键,设计能达到实验目的的方案:_________ 。

已知:①正丁醛的沸点为
 。辛烯醛沸点为
。辛烯醛沸点为 ,密度为
,密度为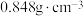 ,难溶于水。
,难溶于水。②

(1)在如图三颈烧瓶中加入
 溶液,在充分搅拌下,从滴液漏斗慢慢滴入
溶液,在充分搅拌下,从滴液漏斗慢慢滴入 正丁醛。采用适宜加热方式是
正丁醛。采用适宜加热方式是
(2)判断有机相已洗涤至中性的操作方法:
(3)操作2的名称是
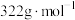 ,固体A的化学式为
,固体A的化学式为(4)利用“减压蒸馏”操作获取产品。温度计示数一定
 。
。(5)为了证明辛烯醛含有碳碳双键,设计能达到实验目的的方案:
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】氧化钪(Sc2O3)是一种稀土氧化物,广泛地应用于航天、激光、导弹等尖端科学领域。钛铁矿主要成分为TiO2、FeO、Fe2O3,还含有Mg、Si、Sc等元素,从钛铁矿中提取Sc2O3的流程如图:
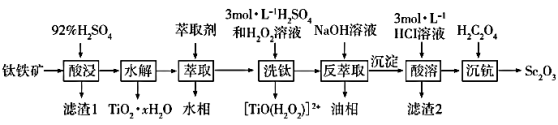
已知:①当离子浓度减小至10-5 mol·L-1时可认为沉淀完全。
②室温下TiO2+完全沉淀的pH为1.05
③Ksp[Fe(OH)3]=4.0×10-38,Ksp[Sc(OH)3]=1.25×10-33,lg2=0.3。
回答下列问题:
(1)“酸浸”时,要适当升高温度或将钛铁矿粉碎等措施,其目的是___________ 。
(2)“酸浸”后Ti元素转化为TiOSO4,其水解反应的化学方程式是
___________ 。
(3)“洗钛”时H2O2的作用之一是与TiO2+反应生成[TiO(H2O2)]2+,该离子为橘黄色的稳定离子,Ti的化合价为___________ ,H2O2还起到的作用是___________ 。
(4)“酸溶”后滤液中存在的金属阳离子Sc3+、TiO2+、Fe3+浓度均小于0.01 mol·L-1,再用氨水调节溶液pH使TiO2+、Fe3+沉淀完全而Sc3+不沉淀,则调pH应控制的范围是___________ 。
(5)加草酸“沉钪”的离子方程式为___________ ,获得Sc2O3的实验操作方法是___________ 。

已知:①当离子浓度减小至10-5 mol·L-1时可认为沉淀完全。
②室温下TiO2+完全沉淀的pH为1.05
③Ksp[Fe(OH)3]=4.0×10-38,Ksp[Sc(OH)3]=1.25×10-33,lg2=0.3。
回答下列问题:
(1)“酸浸”时,要适当升高温度或将钛铁矿粉碎等措施,其目的是
(2)“酸浸”后Ti元素转化为TiOSO4,其水解反应的化学方程式是

(3)“洗钛”时H2O2的作用之一是与TiO2+反应生成[TiO(H2O2)]2+,该离子为橘黄色的稳定离子,Ti的化合价为
(4)“酸溶”后滤液中存在的金属阳离子Sc3+、TiO2+、Fe3+浓度均小于0.01 mol·L-1,再用氨水调节溶液pH使TiO2+、Fe3+沉淀完全而Sc3+不沉淀,则调pH应控制的范围是
(5)加草酸“沉钪”的离子方程式为
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】溴化钙晶体(CaBr2·2H2O)为白色固体,易溶于水,可用于制造灭火剂、制冷剂等。一种制备溴化钙晶体的工艺流程如下:
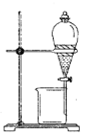
(1)实验室模拟海水提溴的过程中,用苯萃取溶液中的溴,分离溴的苯溶液与水层的操作是(装置如下图):使玻璃塞上的凹槽对准漏斗上的小孔,将活塞拧开,使下面的水层慢慢流下,待有机层和水层界面与活塞上口相切即关闭活塞,______________ 。
(2)“合成”的化学方程式为___________________ 。 “合成”温度控制在70℃以下,其原因是__________ 。投料时控制n(Br2):n(NH3)= 1:0.8,其目的是__________________ 。
(3)“滤渣”的主要成分为_________________ (填化学式)。
(4)“滤液”呈强碱性,其中含有少量BrO-、BrO3-,请补充从“滤液”中提取CaBr2·2H2O的实验操作:加热驱除多余的氨,______________ 。[实验中须使用的试剂有:氢溴酸、活性炭、乙醇;除常用仪器外须使用的仪器有:砂芯漏斗,真空干燥箱]
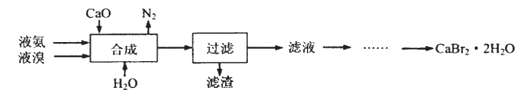
(1)实验室模拟海水提溴的过程中,用苯萃取溶液中的溴,分离溴的苯溶液与水层的操作是(装置如下图):使玻璃塞上的凹槽对准漏斗上的小孔,将活塞拧开,使下面的水层慢慢流下,待有机层和水层界面与活塞上口相切即关闭活塞,
(2)“合成”的化学方程式为
(3)“滤渣”的主要成分为
(4)“滤液”呈强碱性,其中含有少量BrO-、BrO3-,请补充从“滤液”中提取CaBr2·2H2O的实验操作:加热驱除多余的氨,
您最近半年使用:0次



