下列叙述正确的是
| A.将纯水加热,水的离子积变大、pH变小、溶液呈酸性 |
| B.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
| C.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)相等 |
| D.中和体积和pH都相等的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |
14-15高二上·广东肇庆·期末 查看更多[4]
江苏省盐城市伍佑中学2019-2020学年高二下学期第一次阶段考试化学试题2015-2016学年陕西省宝鸡市岐山县高二上学期期末理化学试卷(已下线)2013-2014福建省三明一中下学期期中考试高二化学试卷(已下线)2013-2014学年广东省肇庆市高二上学期末考试化学试卷
更新时间:2016-12-09 10:54:51
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列溶液呈酸性的是( )
| A.含有H+的溶液 | B.c(OH-)=1×10-8mol/L的溶液 |
| C.pH小于7的溶液 | D.c(OH-)<c(H+)的溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】室温下,各离子组一定能大量共存的是
A.强碱性溶液中:K+、Al3+、Cl-、 |
B.pH=0的溶液中:Na+、Fe3+、 、 、 |
C.含有1mol·L−1Fe3+的溶液中:K+、Mg2+、I-、 |
D.由水电离的c(H+)=1×10−14的溶液中:K+、Ca2+、Cl-、 |
您最近一年使用:0次
【推荐1】下列实验合理的是
| A.用湿润的pH试纸测定CH3COONa溶液的pH |
| B.用蒸馏的方法分离乙醇(沸点为78.3℃)和苯(沸点为80.1℃)的混合物 |
| C.用淀粉-KI试纸鉴别碘水和FeCl3溶液 |
| D.用Na2CO3溶液鉴别CaCl2溶液、NaCl溶液和稀硫酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法正确的是( )
| A.强酸的水溶液中不存在OH- |
| B.pH=0的溶液是酸性最强的溶液 |
| C.25℃时溶液中由水电离出的c(H+)=1×10-11mol·L-1,该溶液显碱性 |
| D.温度不变时,加水稀释氢氧化钠溶液,溶液中离子浓度不能都减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】醋酸溶液中存在电离平衡: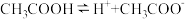 ,下列叙述不正确的是
,下列叙述不正确的是
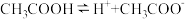 ,下列叙述不正确的是
,下列叙述不正确的是A.加水稀释, 增大 增大 |
| B.0.10mol/L的CH3COOH溶液加水稀释,溶液中c(OH-)增大 |
| C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D.25℃时,欲使醋酸溶液的pH和电离程度都减小,可加入少量冰醋酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】“天宫课堂”中王亚平老师在空间站“变”出奥运五环,在透明的五环模型中第一次、第二次分别加入的溶液如下表所示[已知溴百里酚蓝变色的pH范围:6.0(黄)~7.6(蓝)]。下列叙述正确的是

| 1号环 | 2号环 | 3号环 | 4号环 | 5号环 | |
| 第一次加入 | Na2CO3溶液 | KI和KIO3溶液 | 乙酸溶液 | Na2CO3溶液 | Na2CO3溶液 |
| 第二次加入 | 溴百里酚蓝 | 淀粉溶液,乙酸 | 甲基橙 | 甲基橙 | 甲基橙、溴百里酚蓝 |

A.1号环中 水解的离子方程式为 水解的离子方程式为 +2H2O=H2CO3+2OH- +2H2O=H2CO3+2OH- |
B.2号环中发生的离子反应为5I-+ +6H+=3I2+3H2O +6H+=3I2+3H2O |
| C.3号环中溶液的pH若为a,将其稀释10倍则pH变为a+1 |
| D.5号环最后溶液呈现的绿色是黄色与蓝色的混合色 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 把 溶液滴到 溶液滴到 试纸上 试纸上 |  |  溶液水解显碱性 溶液水解显碱性 |
| B | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体 固体 | 溶液红色变浅 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| C | 常温下,用 计分别测定1 计分别测定1 和0.1 和0.1  溶液的 溶液的 |  均为7 均为7 | 同温下,不同浓度的 溶液中水的电离程度相同 溶液中水的电离程度相同 |
| D | 两支试管各盛0.1 4 4 酸性高锰酸钾溶液,分别加入0.1 酸性高锰酸钾溶液,分别加入0.1 2 2 草酸溶液和0.2 草酸溶液和0.2 2 2 草酸溶液 草酸溶液 | 加入0.2 草酸溶液试管中,高锰酸钾溶液褪色更快 草酸溶液试管中,高锰酸钾溶液褪色更快 | 反应物浓度越大,反应速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】“类比”思想在化学领域有广泛应用,下列有关“类比”合理的是
| 选项 | 已知 | 类比 |
| A |  |  |
| B | 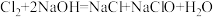 | 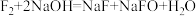 |
| C | 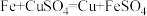 | 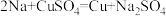 |
| D | 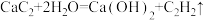 | 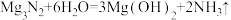 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】某化学小组的同学测定0.1mol•L-1Na2SO3溶液在先升温再降温过程中的pH(不考虑温度变化过程中溶液体积的变化),数据如表:
下列说法中正确的是
| 时刻 | ① | ② | ③ | ④ |
| 温度/℃ | 25 | 30 | 40 | 25 |
| pH | 9.66 | 9.52 | 9.37 | 9.25 |
A.Na2SO3溶液中存在水解平衡:SO +2H2O +2H2O H2SO3+2OH- H2SO3+2OH- |
B.④的pH与①不同,是SO 浓度减小造成的 浓度减小造成的 |
| C.①→③的过程中,温度和浓度的变化对水解平衡移动方向的影响一致 |
| D.取①④时刻的溶液,加入BaCl2溶液,产生沉淀的物质的量不相等 |
您最近一年使用:0次

 H++In-(黄色) ΔH>0,在含有HIn的水溶液中,某同学加入以下物质能使溶液显黄色的是
H++In-(黄色) ΔH>0,在含有HIn的水溶液中,某同学加入以下物质能使溶液显黄色的是

