某化学小组的同学测定0.1mol•L-1Na2SO3溶液在先升温再降温过程中的pH(不考虑温度变化过程中溶液体积的变化),数据如表:
下列说法中正确的是
| 时刻 | ① | ② | ③ | ④ |
| 温度/℃ | 25 | 30 | 40 | 25 |
| pH | 9.66 | 9.52 | 9.37 | 9.25 |
A.Na2SO3溶液中存在水解平衡:SO +2H2O +2H2O H2SO3+2OH- H2SO3+2OH- |
B.④的pH与①不同,是SO 浓度减小造成的 浓度减小造成的 |
| C.①→③的过程中,温度和浓度的变化对水解平衡移动方向的影响一致 |
| D.取①④时刻的溶液,加入BaCl2溶液,产生沉淀的物质的量不相等 |
更新时间:2022-11-10 22:06:19
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】甲醇是重要的化工原料,应用前景广阔。研究表明,二氧化碳与氢气反应可以合成甲醇,反应为: ,有利于提高平衡时
,有利于提高平衡时 转化率的措施
转化率的措施
 ,有利于提高平衡时
,有利于提高平衡时 转化率的措施
转化率的措施| A.使用催化剂 | B.增大 和 和 的初始投料比 的初始投料比 |
| C.加压 | D.等容下通入稀有气体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】一定温度下,向三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应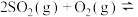
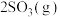 (正反应放热),测得反应的相关数据如下:
(正反应放热),测得反应的相关数据如下:
下列说法正确的是
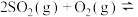
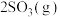 (正反应放热),测得反应的相关数据如下:
(正反应放热),测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2 mol 、1 mol 、1 mol | 4mol | 2 mol 、1 mol 、1 mol |
平衡时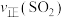 / /(mol·L  ·s ·s ) ) |  |  |  |
平衡时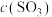 /(mol·L  ) ) |  |  | 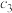 |
| 平衡时体系总压强p/Pa |  |  |  |
物质的平衡转化率 | 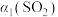 | 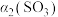 | 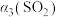 |
| 平衡常数K |  |  |  |
A. , , | B. , ,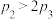 |
C. , ,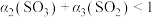 | D. , ,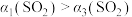 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】对于可逆反应:mA(g)+nB(g) pC(g)+qD(g);△H<0;已知m+n>p+q,若反应由A与B组成的混合物开始,并分别在下列情况下达到平衡:在100℃、1×106Pa时,A的转化率为α1;在200℃、1×106Pa时,A的转化率为α2;在100℃、1×107Pa时,A的转化率为α3;则α1、α2、α3之间的大小关系是
pC(g)+qD(g);△H<0;已知m+n>p+q,若反应由A与B组成的混合物开始,并分别在下列情况下达到平衡:在100℃、1×106Pa时,A的转化率为α1;在200℃、1×106Pa时,A的转化率为α2;在100℃、1×107Pa时,A的转化率为α3;则α1、α2、α3之间的大小关系是
 pC(g)+qD(g);△H<0;已知m+n>p+q,若反应由A与B组成的混合物开始,并分别在下列情况下达到平衡:在100℃、1×106Pa时,A的转化率为α1;在200℃、1×106Pa时,A的转化率为α2;在100℃、1×107Pa时,A的转化率为α3;则α1、α2、α3之间的大小关系是
pC(g)+qD(g);△H<0;已知m+n>p+q,若反应由A与B组成的混合物开始,并分别在下列情况下达到平衡:在100℃、1×106Pa时,A的转化率为α1;在200℃、1×106Pa时,A的转化率为α2;在100℃、1×107Pa时,A的转化率为α3;则α1、α2、α3之间的大小关系是| A.α1>α2>α3 | B.α3>α2>α1 | C.α3>α1>α2 | D.α1>α3>α2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列事实不能用勒夏特列原理解释的是
| A.黄绿色的氯水光照后颜色变浅 |
B.CaCO3(s) CaO(s)+CO2(g),平衡时将容器的体积缩小至一半,新平衡的 CaO(s)+CO2(g),平衡时将容器的体积缩小至一半,新平衡的 浓度与原平衡相同 浓度与原平衡相同 |
| C.用浓氨水和氢氧化钠固体可快速制取氨气 |
| D.打开汽水瓶时,有大量气泡溢出 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】W、X、Y、Z为原子序数依次增大的四种短周期元素,A、B、C、D为上述四种元素中的两种或三种所组成的化合物,E为单质,五种物质间的转化关系如图所示。已知室温下,0.1mol•L-1A的水溶液pH为1,B分子中含有10个电子,C为一种盐,D为一种常见的具有漂白性的物质。下列说法正确的是
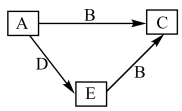
| A.C的溶液显碱性 | B.Z元素在同周期主族元素中原子半径最小 |
| C.X、Y形成的二元化合物只有两种 | D.D中各原子均满足最外层8e-稳定结构 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】关于小苏打水溶液的表述正确的是
A.存在的电离平衡为 +H2O +H2O H2CO3+OH- H2CO3+OH- |
B.c(Na+)+c(H+)=c( )+c( )+c( )+c(OH-) )+c(OH-) |
C. 的电离程度大于 的电离程度大于 的水解程度 的水解程度 |
D.c(Na+)=c( )+c( )+c( )+c(H2CO3) )+c(H2CO3) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】铬(VI)在 溶液中可以多种形式存在。25°C时,调节初始浓度为0.1mol·L-1的Na2CrO4溶液的pH,平衡时铬(VI)在水溶液中各种存在形式的物质的量分数δ(X)与pH的关系如图所示。已知溶液中存在反应2CrO + 2H+
+ 2H+ Cr2O
Cr2O + H2O。下列说法正确的是
+ H2O。下列说法正确的是

 + 2H+
+ 2H+ Cr2O
Cr2O + H2O。下列说法正确的是
+ H2O。下列说法正确的是
| A.铬酸(H2CrO4)的第一步电离为完全电离 |
B.a点处,δ(CrO ) =δ(Cr2O ) =δ(Cr2O )> )> |
| C.Ka2(H2CrO4)的数量级为10-6 |
| D.NaHCrO4溶液电离小于水解 |
您最近一年使用:0次

 2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是
2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是

