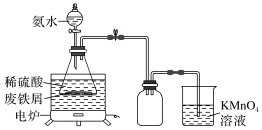
在空气中加热S粉和Fe粉的混合物,可观察到下列现象:
(1)有淡蓝色火焰,且生成刺激性气味的气体。
(2)混合粉末变红,放出热量,最后变成黑色固体。
(3)不时有火星从混合物中射出。
请分别写出以上三种情况发生反应的化学方程式:__________ 、__________ 、__________ 。
(1)有淡蓝色火焰,且生成刺激性气味的气体。
(2)混合粉末变红,放出热量,最后变成黑色固体。
(3)不时有火星从混合物中射出。
请分别写出以上三种情况发生反应的化学方程式:
9-10高一·全国·单元测试 查看更多[4]
更新时间:2016-12-09 00:20:01
|
相似题推荐
【推荐1】氧化剂和还原剂在生产生活中广泛使用。
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=5Br2+2MnBr2+2KBr+8H2O
①用单线桥表示电子转移的方向和数目_______ 。
②若有8个Br-离子参加反应,则转移电子的数目是_______ 个。
③HBr在上述反应中显示出来的性质是_______ 。
A.氧化性 B.还原性 C.酸性 D.碱性
(2)①请配平化学方程式______ 。
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2+_______Cl2↑+_______H2O
②写出NaClO与酸性FeSO4溶液混合发生氧化还原反应的离子方程式:_______
(3)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。利用H3PO2进行化学镀银反应中,氧化剂与还原剂物质的量之比为4∶1,则氧化产物为_______ 。
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=5Br2+2MnBr2+2KBr+8H2O
①用单线桥表示电子转移的方向和数目
②若有8个Br-离子参加反应,则转移电子的数目是
③HBr在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(2)①请配平化学方程式
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2+_______Cl2↑+_______H2O
②写出NaClO与酸性FeSO4溶液混合发生氧化还原反应的离子方程式:
(3)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。利用H3PO2进行化学镀银反应中,氧化剂与还原剂物质的量之比为4∶1,则氧化产物为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】工业上用MnO2和KOH为原料制取高锰酸钾,主要生产过程分两步进行:第一步将 MnO2 和固体 KOH 粉碎,混合均匀,在空气中加热至熔化,并连续搅拌,制取 K2MnO4;第二步将 K2MnO4 的浓溶液进行电解,制取 KMnO4。试回答以下问题:
(1)写出第一步的反应方程式_______ ;连续搅拌的目的是_______ ;
(2)电解 K2MnO4 的浓溶液时,两极发生的电极反应式:阴极是_______ , 阳极是_______ ,电解总的反应方程式是_______ 。
(1)写出第一步的反应方程式
(2)电解 K2MnO4 的浓溶液时,两极发生的电极反应式:阴极是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学计量在化学中占有重要地位。请回答下列问题:
(1)0.3 mol NH3分子中所含原子数与约__________ 个H2O分子中所含原子数相等。
(2)V mL含a g Al3+的Al2(SO4)3溶液中所含SO42−的物质的量浓度为_____ mol·L−1。
(3)在一定温度和压强下,1体积气体X2与3体积Y2化合生成2体积气态化合物,该化合物的化学式为_________ 。
(4)将各0.3 mol的钠、镁、铝分别放入100 mL 1 mol·L−1的盐酸中,同温同压下产生气体的体积比为_____________ 。
(5)锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,当生成1 mol硝酸锌时,参加反应的硝酸的物质的量为_________ mol。
(1)0.3 mol NH3分子中所含原子数与约
(2)V mL含a g Al3+的Al2(SO4)3溶液中所含SO42−的物质的量浓度为
(3)在一定温度和压强下,1体积气体X2与3体积Y2化合生成2体积气态化合物,该化合物的化学式为
(4)将各0.3 mol的钠、镁、铝分别放入100 mL 1 mol·L−1的盐酸中,同温同压下产生气体的体积比为
(5)锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,当生成1 mol硝酸锌时,参加反应的硝酸的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)写出元素符号:
①________ ,②________ ,⑨________ 。
(2)写出下列反应的化学方程式:
⑤的单质跟④的氢氧化物溶液反应:________________________________________ 。
⑥的单质在③的单质中燃烧:__________________________________________ 。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 四 | ⑨ |
①
(2)写出下列反应的化学方程式:
⑤的单质跟④的氢氧化物溶液反应:
⑥的单质在③的单质中燃烧:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据题意完成下列问题:
(1)做实验时皮肤上不小心粘了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为: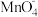 +
+ 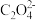 + H+ → CO2↑+ Mn2+ +
+ H+ → CO2↑+ Mn2+ + 
①该反应的氧化剂是_____ 右边方框内的产物是_____
②完成并配平该离子方程式__________________ 电子转移总数是_____ e-
(2)如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。单质A能与某气态单质化合生成化合物B。
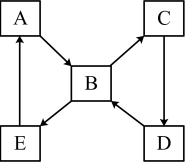
若化合物B是造成酸雨的主要污染物,化合物D是组成单质A元素的最高价氧化物对应水化物,则单质A是_________ (物质名称),将化合物B通入溴水中观察到的现象是_________ ,该现象说明化合物B具有_______ 性。
(1)做实验时皮肤上不小心粘了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为:
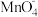 +
+ 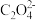 + H+ → CO2↑+ Mn2+ +
+ H+ → CO2↑+ Mn2+ + 
①该反应的氧化剂是
②完成并配平该离子方程式
(2)如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。单质A能与某气态单质化合生成化合物B。

若化合物B是造成酸雨的主要污染物,化合物D是组成单质A元素的最高价氧化物对应水化物,则单质A是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)实验室中的Na2SiO3溶液长期放置,瓶底会出现白色沉淀,则形成沉淀的离子方程式是___________ 。取瓶中的上层清液加入稀盐酸,观察到既有气泡产生又有沉淀生成,其离子方程式分别为___________ , ___________ 。
(2)硫有一些特殊的化学性质,从而决定了在生活中特殊的用途。例如硫单质易与不活泼金属汞、银化合,在家庭、医务室等场所不小心有水银温度计打碎而有汞撒落的时候,可用硫粉处理。
①请写出硫粉与汞的反应方程式___________ 。
②某次实验后试管内壁上粘附有一些硫晶体,除去的方法是___________ 。
(3)将浓H2SO4表现的性质填入横线内。
A.酸性 B.强氧化性 C.脱水性 D.吸水性
①用磷矿粉[主要成分Ca3(PO4)2]和硫酸反应制磷酸_____
②热的浓硫酸与铜片反应___
③浓H2SO4不能干燥NH3、H2S、HI等气体____
④浓H2SO4能吸收H2或SO2气体中的水分____
⑤浓硫酸使湿润的蓝色石蕊试纸先变红后变黑____
(2)硫有一些特殊的化学性质,从而决定了在生活中特殊的用途。例如硫单质易与不活泼金属汞、银化合,在家庭、医务室等场所不小心有水银温度计打碎而有汞撒落的时候,可用硫粉处理。
①请写出硫粉与汞的反应方程式
②某次实验后试管内壁上粘附有一些硫晶体,除去的方法是
(3)将浓H2SO4表现的性质填入横线内。
A.酸性 B.强氧化性 C.脱水性 D.吸水性
①用磷矿粉[主要成分Ca3(PO4)2]和硫酸反应制磷酸
②热的浓硫酸与铜片反应
③浓H2SO4不能干燥NH3、H2S、HI等气体
④浓H2SO4能吸收H2或SO2气体中的水分
⑤浓硫酸使湿润的蓝色石蕊试纸先变红后变黑
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】学习化学应该明确“从生活中来,到生活中去”道理。在生产生活中,我们会遇到各种各样的化学物质和化学反应。请按要求填空
(1)计算机芯片的主要成分是___ (填名称),节日的烟花是利用___ 。
(2)请你写出工业上用氯气和消石灰反应制取漂白粉的化学反应方程式:___ 。
(3)玉石的主要成分基本都属于硅酸盐,如某种翡翠的主要成分为NaAlSi2O6,将其表示为氧化物形式可写为___ 。
(4)沾有水的铁质器皿在加热时会发黑,该反应的化学方程式是___ 。
(5)补铁剂中的Fe2+易被氧化成Fe3+,服用时医生常建议同时服用维生素C,这是利用维生素C的___ 。
(1)计算机芯片的主要成分是
(2)请你写出工业上用氯气和消石灰反应制取漂白粉的化学反应方程式:
(3)玉石的主要成分基本都属于硅酸盐,如某种翡翠的主要成分为NaAlSi2O6,将其表示为氧化物形式可写为
(4)沾有水的铁质器皿在加热时会发黑,该反应的化学方程式是
(5)补铁剂中的Fe2+易被氧化成Fe3+,服用时医生常建议同时服用维生素C,这是利用维生素C的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)钠的金属活动性比铝的______ (填“强”或“弱)。
(2)Fe跟Cl2在一定条件下反应,所得产物的化学式是_____ 。
(3)Na、Mg、Al分别与足量的盐酸反应,当生成气体的质量相同时,消耗Na、Mg、Al的物质的量之比为________ 。
(4)等质量的铝分别与足量的盐酸、氢氧化钠反应产生氢气在同温同压的体积之比为______ 。
(2)Fe跟Cl2在一定条件下反应,所得产物的化学式是
(3)Na、Mg、Al分别与足量的盐酸反应,当生成气体的质量相同时,消耗Na、Mg、Al的物质的量之比为
(4)等质量的铝分别与足量的盐酸、氢氧化钠反应产生氢气在同温同压的体积之比为
您最近一年使用:0次