原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为24。
(1)F原子基态的价电子排布式为_______________ 。
(2)在A、B、C三种元素中,电负性由大到小的顺序是______ >______ >_____ (用元素符号回答)。
(3)元素C的简单气态氢化物的沸点远高于元素E的简单气态氢化物的沸点,其主要原因是________________________ 。
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的空间构型为_____________ 。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为_______________ 。
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为________________________ 。

(1)F原子基态的价电子排布式为
(2)在A、B、C三种元素中,电负性由大到小的顺序是
(3)元素C的简单气态氢化物的沸点远高于元素E的简单气态氢化物的沸点,其主要原因是
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的空间构型为
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为

14-15高三上·江苏·期末 查看更多[7]
(已下线)2014届江苏省苏北四市高三上期末统考化学试卷(已下线)2013-2014山东省东营市高三第二次模拟理科综合化学试卷2015届江苏省扬州中学高三4月双周测化学试卷2016届四川省乐山市高中高三上学期第二次调研考试化学试卷2016届四川省成都七中等两校高三第二次模拟化学试卷2016-2017学年山东省淄博市淄川中学高二下学期学分认定(期中)考试化学试卷(已下线)二轮复习 专题17 物质结构与性质 押题专练
更新时间:2016-12-09 14:35:19
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】祖母绿被称为绿宝石之王,是国际珠宝世界公认的四大名贵宝石之一,其化学式为Be3Al2Si6O18。回答下列问题:
(1)基态Be原子的电子排布图为____________ ,基态Al原子核外电子占据________ 个轨道,其中能量最高能级的原子轨道的形状为__________ 。
(2)Al、Si、O的第一电离能由大到小的排序为____________________ 。
(3)SO3分子中硫原子的杂化类型是_____ ,SO3分子的空间构型是________ 。
(4)工业上,电解制取金属铝,不能用熔融的AlCl3,AlCl3的晶体类型是__________ ,将Be3Al2Si6O18写为氧化物的式子是_____________________ 。
(5)LiAlH4在有机合成中可将羧基还原成羟基。甲酸和乙醇的熔、沸点如图所示:
1mol甲酸分子中σ键与π键的比值为________________ ,甲酸和乙醇的熔点相差较大的主要原因是____________________________________________ 。
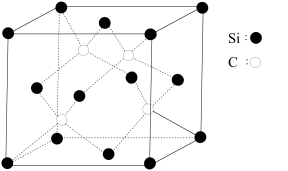
(6)碳化硅的晶体类型类似金刚石,晶胞结构如图所示。已知:碳化硅的晶体密度为ag/cm3,NA代表阿伏加 德罗常数的数值。该晶胞边长为_____________ pm。
(1)基态Be原子的电子排布图为
(2)Al、Si、O的第一电离能由大到小的排序为
(3)SO3分子中硫原子的杂化类型是
(4)工业上,电解制取金属铝,不能用熔融的AlCl3,AlCl3的晶体类型是
(5)LiAlH4在有机合成中可将羧基还原成羟基。甲酸和乙醇的熔、沸点如图所示:
| 甲酸 | 乙醇 | |
| 相对分子质量 | 46 | 46 |
| 熔点/°C | 8.6 | -114.3 |
| 沸点/°C | 101 | 78.4 |

(6)碳化硅的晶体类型类似金刚石,晶胞结构如图所示。已知:碳化硅的晶体密度为ag/cm3,NA代表阿伏加 德罗常数的数值。该晶胞边长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C、D、E 为原子序数依次增大的前四周期元素。已知前四种元素的基态原子p能级都有2个单电子,E 的原子序数等于A、B、C三种元素原子序数之和。
试回答下列问题:
(1)基态E原子外围电子排布图为_________ ;其中M 能层有_____ 种能量不同的电子。
(2)从原子结构角度解释B 电负性大于D的原因是:_______________ 。
(3) 含A元素的化合物中,A 的原子间常有π键,但是含C元素的化合物中,C的原子间只能存在σ键,其主要原因是___________________ 。
(4)H2D2B8是一种具有强氧化性的二元酸(其中分子结构中有2个B原子显-1价),则H2D2B8的结构式为___________ ,分子中采取sp3杂化的B原子有______ 个。
(5)E 晶胞内粒子的堆积模型如图所示。

已知:E 晶胞的密度为ρg/cm3,NA代表阿伏伽德罗常数值,E 的相对原子质量为M。
①E 粒子的配位数为_______ 。
②E 粒子半径为_______ pm。
③E 晶胞中粒子的空间利用率φ=_____ (用含π 的式子表示)。
试回答下列问题:
(1)基态E原子外围电子排布图为
(2)从原子结构角度解释B 电负性大于D的原因是:
(3) 含A元素的化合物中,A 的原子间常有π键,但是含C元素的化合物中,C的原子间只能存在σ键,其主要原因是
(4)H2D2B8是一种具有强氧化性的二元酸(其中分子结构中有2个B原子显-1价),则H2D2B8的结构式为
(5)E 晶胞内粒子的堆积模型如图所示。

已知:E 晶胞的密度为ρg/cm3,NA代表阿伏伽德罗常数值,E 的相对原子质量为M。
①E 粒子的配位数为
②E 粒子半径为
③E 晶胞中粒子的空间利用率φ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】(1)下列说法正确的是________ (填字母)。
A.HOCH2CH(OH)CH2OH与CH3CHClCH2CH3都是手性分子
B. 和CH4的立体构型相似
和CH4的立体构型相似
C.BF3与 都是平面形分子
都是平面形分子
D.CO2和H2O都是直线形分子
(2)石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。
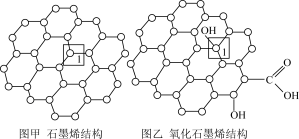
①图甲中,1号C与相邻C形成σ键的个数为________ 。
②图乙中,1号C的杂化方式是________ ,该C与相邻C形成的键角________ (填“>”“<”或“=”)图甲中1号C与相邻C形成的键角。
(3)碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:

①金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为____________ 。
②金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________ 、________ 。
A.HOCH2CH(OH)CH2OH与CH3CHClCH2CH3都是手性分子
B.
 和CH4的立体构型相似
和CH4的立体构型相似C.BF3与
 都是平面形分子
都是平面形分子D.CO2和H2O都是直线形分子
(2)石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。

①图甲中,1号C与相邻C形成σ键的个数为
②图乙中,1号C的杂化方式是
(3)碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:

①金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为
②金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】铁( )、钴(
)、钴( )、镍(
)、镍( )是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
)是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为___________ 。
(2)铁系元素能与 形成
形成 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点
为浅黄色液体,沸点 ,则
,则 中含有的化学键类型包括___________。
中含有的化学键类型包括___________。
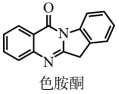
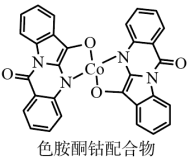
(3)以甲醇为溶剂, 可与色胺酮分子配位结合形成对
可与色胺酮分子配位结合形成对 具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素(
具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素( 、
、 、
、 、
、 )第一电离能由大到小的顺序为
)第一电离能由大到小的顺序为___________ ,色氨酮分子中 原子的杂化类型为
原子的杂化类型为___________ 。 射线衍射分析显示色胺酮钴配合物晶胞中还含有一个
射线衍射分析显示色胺酮钴配合物晶胞中还含有一个 分子,
分子, 是通过
是通过___________ 作用与色胺酮钴配合物相结合。

(4) 、
、 、
、 与
与 都位于第四周期且最外层电子数相同,但相应单质的熔点,
都位于第四周期且最外层电子数相同,但相应单质的熔点, 、
、 、
、 明显高于
明显高于 ,其原因是
,其原因是___________ 。
(5) 是一种使用广泛的荧光材料。已知立方
是一种使用广泛的荧光材料。已知立方 的晶胞结构如下图所示:
的晶胞结构如下图所示:
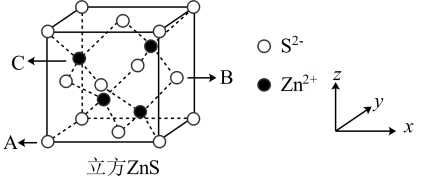
①已知 、
、 点的原子坐标分别为(0,0,0)和(1,1/2,1/2),则
点的原子坐标分别为(0,0,0)和(1,1/2,1/2),则 点的原子坐标为
点的原子坐标为___________ ;
②立方 的晶胞参数
的晶胞参数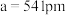 ,则其晶体密度为
,则其晶体密度为___________  。(列出计算表达式)
。(列出计算表达式)
 )、钴(
)、钴( )、镍(
)、镍( )是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
)是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为(2)铁系元素能与
 形成
形成 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点
为浅黄色液体,沸点 ,则
,则 中含有的化学键类型包括___________。
中含有的化学键类型包括___________。| A.极性共价键 | B.离子键 | C.配位键 | D.金属键 |
 可与色胺酮分子配位结合形成对
可与色胺酮分子配位结合形成对 具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素(
具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素( 、
、 、
、 、
、 )第一电离能由大到小的顺序为
)第一电离能由大到小的顺序为 原子的杂化类型为
原子的杂化类型为 射线衍射分析显示色胺酮钴配合物晶胞中还含有一个
射线衍射分析显示色胺酮钴配合物晶胞中还含有一个 分子,
分子, 是通过
是通过


(4)
 、
、 、
、 与
与 都位于第四周期且最外层电子数相同,但相应单质的熔点,
都位于第四周期且最外层电子数相同,但相应单质的熔点, 、
、 、
、 明显高于
明显高于 ,其原因是
,其原因是(5)
 是一种使用广泛的荧光材料。已知立方
是一种使用广泛的荧光材料。已知立方 的晶胞结构如下图所示:
的晶胞结构如下图所示:
①已知
 、
、 点的原子坐标分别为(0,0,0)和(1,1/2,1/2),则
点的原子坐标分别为(0,0,0)和(1,1/2,1/2),则 点的原子坐标为
点的原子坐标为②立方
 的晶胞参数
的晶胞参数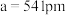 ,则其晶体密度为
,则其晶体密度为 。(列出计算表达式)
。(列出计算表达式)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
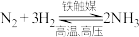
(1)基态氢原子中,核外电子的电子云轮廓图形状为___________ 。
(2)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ 。 分子的电子式为
分子的电子式为___________ 。
② 分子中,与
分子中,与 原子相连的
原子相连的 显正电性。则电负性:
显正电性。则电负性:
___________  。(填“>”或“<”)。
。(填“>”或“<”)。 分子的VSEPR模型的名称为
分子的VSEPR模型的名称为___________ ,其分子的空间结构为___________ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中 区的元素是
区的元素是___________ 。
②比较第一电离能的大小:
___________  (填“>”或“<”)。
(填“>”或“<”)。
③下表的数据从上到下是三种金属元素逐级失去电子的电离能。
(a)请解释:为什么原子的逐级电离能越来越大:___________ 。
(b)元素B的常见化合价为:___________ 。
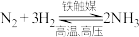
(1)基态氢原子中,核外电子的电子云轮廓图形状为
(2)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
 分子的电子式为
分子的电子式为②
 分子中,与
分子中,与 原子相连的
原子相连的 显正电性。则电负性:
显正电性。则电负性:
 。(填“>”或“<”)。
。(填“>”或“<”)。 分子的VSEPR模型的名称为
分子的VSEPR模型的名称为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。①上述氧化物所涉及的元素中,处于元素周期表中
 区的元素是
区的元素是②比较第一电离能的大小:

 (填“>”或“<”)。
(填“>”或“<”)。③下表的数据从上到下是三种金属元素逐级失去电子的电离能。
| 元素 | A | B | C |
电离能 | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(b)元素B的常见化合价为:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】(1)铁离子(Fe3+)最外层电子排布式为______ ,其核外共有______ 种不同运动状态的电子。
(2)硒、砷、溴三种元素的第一电离能从大到小的顺序为___________ (用元素符号表示)。
(3)两种三角锥形气态氢化物PH3和NH3的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因_____________________________________________________________ 。
(4)常温下PCl5是白色晶体,在148℃时熔化成能导电的熔体。该熔体由A、B两种微粒构成,A、B分别与CCl4、SF6互为等电子体,则A的化学式为__________________ ,其中心原子杂化方式为_______________ 。
(5)Cu与Au的某种合金可形成面心立方最密堆积的晶体(密度为ρg·cm-3),在该晶胞中Cu原子处于面心,用NA表示阿伏伽德罗常数的值。

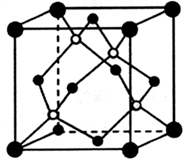
①与Au距离最近的Cu个数为________ 。
②该晶体具有储氢功能,氢原子 可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为__________ ,则晶胞中Cu原子与Au原子中心的最短距离d=________ cm。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为__________ ( )。
)。
(2)硒、砷、溴三种元素的第一电离能从大到小的顺序为
(3)两种三角锥形气态氢化物PH3和NH3的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因
(4)常温下PCl5是白色晶体,在148℃时熔化成能导电的熔体。该熔体由A、B两种微粒构成,A、B分别与CCl4、SF6互为等电子体,则A的化学式为
(5)Cu与Au的某种合金可形成面心立方最密堆积的晶体(密度为ρg·cm-3),在该晶胞中Cu原子处于面心,用NA表示阿伏伽德罗常数的值。


①与Au距离最近的Cu个数为
②该晶体具有储氢功能,氢
 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】按要求填空。
(1)下列原子或离子的电子排布式或排布图正确的是_______ (填序号,下同),违反能量最低原理的是_______ ,违反洪特规则的是_______ ,违反泡利原理的是_______ 。
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P:
④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C: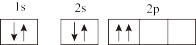
(2) 互为等电子体的离子为
互为等电子体的离子为_______ (只写一个);
(3)Ni与CO能形成配合物Ni(CO)4,该分子中π键与σ键个数比为_______ ;
(4)BF3能与NH3反应生成BF3·NH3.BF3·NH3中B原子的杂化轨道类型为_______ ,B与N之间形成_______ 键。硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,[B(OH)4]-中B的原子杂化类型为_______ ,不考虑空间构型,[B(OH)4]-的结构可用示意图表示为_______ ;
(5)氨气溶于水时,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为_______ ;
A.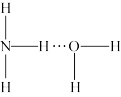 B.
B.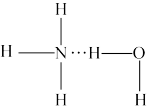 C.
C.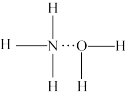 D.
D.
氨水和次氯酸盐溶液在弱碱性介质中反应可生成氯胺(H2NCl),分子结构类似于NH3,H2NCl分子的空间构型为_______ ,电子式为_______ ,H2NCl中氯的化合价为_______ 。
(1)下列原子或离子的电子排布式或排布图正确的是
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P:

④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C:
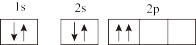
(2)
 互为等电子体的离子为
互为等电子体的离子为(3)Ni与CO能形成配合物Ni(CO)4,该分子中π键与σ键个数比为
(4)BF3能与NH3反应生成BF3·NH3.BF3·NH3中B原子的杂化轨道类型为
(5)氨气溶于水时,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为
A.
 B.
B. C.
C. D.
D.
氨水和次氯酸盐溶液在弱碱性介质中反应可生成氯胺(H2NCl),分子结构类似于NH3,H2NCl分子的空间构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铜是重要的金属,广泛应用于电气、机械制造和国防等领域。铜的化合物在科学研究和工农业生产中有许多用途。回答下列问题:
(1) 原子的价层电子排布式为
原子的价层电子排布式为___________ 。
(2) 晶体中S原子的杂化方式为
晶体中S原子的杂化方式为___________ , 的立体构型为
的立体构型为___________ 。
(3)向 溶液中加入过量氨水,可生成
溶液中加入过量氨水,可生成 。下列说法正确的是___________(填标号)。
。下列说法正确的是___________(填标号)。
(4)葡萄糖与新制 的碱性溶液反应生成红色
的碱性溶液反应生成红色 沉淀。在1个
沉淀。在1个 晶胞中(结构如图所示),所包含的
晶胞中(结构如图所示),所包含的 原子的数目为
原子的数目为___________ ;每个氧原子与___________ 个铜原子配位。氧化亚铜在稀硫酸中很不稳定,得到蓝色溶液和一种固体,试写出其变化的离子方程式:___________ 。

(5)已知铜和氧的原子半径分别为a和b,试用a、b、 等表示
等表示 的密度(只要求写出计算式)
的密度(只要求写出计算式)___________ 。
(1)
 原子的价层电子排布式为
原子的价层电子排布式为(2)
 晶体中S原子的杂化方式为
晶体中S原子的杂化方式为 的立体构型为
的立体构型为(3)向
 溶液中加入过量氨水,可生成
溶液中加入过量氨水,可生成 。下列说法正确的是___________(填标号)。
。下列说法正确的是___________(填标号)。A.氨气极易溶于水,是因为 分子和 分子和 分子之间形成了3种不同的氢键 分子之间形成了3种不同的氢键 |
B. 分子和 分子和 分子的分子空间构型不同,氨气分子的键角大于水分子的键角 分子的分子空间构型不同,氨气分子的键角大于水分子的键角 |
C. 所含有的化学键有离子键、极性共价键和配位键 所含有的化学键有离子键、极性共价键和配位键 |
D. 的组成元素中,电负性最大的是氮元素 的组成元素中,电负性最大的是氮元素 |
 的碱性溶液反应生成红色
的碱性溶液反应生成红色 沉淀。在1个
沉淀。在1个 晶胞中(结构如图所示),所包含的
晶胞中(结构如图所示),所包含的 原子的数目为
原子的数目为
(5)已知铜和氧的原子半径分别为a和b,试用a、b、
 等表示
等表示 的密度(只要求写出计算式)
的密度(只要求写出计算式)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】二茂铁[Fe(C5H5)2]可用作火箭燃料添加剂、汽油的抗爆剂和橡胶的熟化剂,也可作紫外线吸收剂。可由环戊二烯( )和FeCl2在三乙胺[(C2H5)3N]存在下反应制得。
)和FeCl2在三乙胺[(C2H5)3N]存在下反应制得。
(1)在元素周期表中,与Fe既同周期又同族且价层电子总数为10的元素是_____ (填元素符号),该元素基态原子核外N层电子的自旋状态_______ (填“相同”或“相反”)。
(2)三乙胺中电负性最小的元素是________ (填元素符号);C元素的_______ 杂化轨道与H元素的________ 轨道形成_______ 键。
(3)下列状态的Cl中,电离最外层一个电子所需能量最大的是______ (填序号)。
A. [Ne] B. [Ne]
B. [Ne] 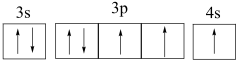
C. [Ne]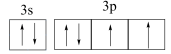 D. [Ne]
D. [Ne] 
(4)已知:分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成的大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成的大π键的电子数(如苯分子中的大π键可表示为 ),则环戊二烯负离子(
),则环戊二烯负离子( )中的大π键应表示为
)中的大π键应表示为________ 。
(5)二茂铁易升华且可溶于有机溶剂中,其晶体类型为________ ,二茂铁的晶胞结构如图所示(未画出微粒),密度为pg·cm-3,则一个晶胞中Fe(C5H5)2。数目的计算表达式为______ (设阿伏加 德罗常数的值为NA)。

 )和FeCl2在三乙胺[(C2H5)3N]存在下反应制得。
)和FeCl2在三乙胺[(C2H5)3N]存在下反应制得。(1)在元素周期表中,与Fe既同周期又同族且价层电子总数为10的元素是
(2)三乙胺中电负性最小的元素是
(3)下列状态的Cl中,电离最外层一个电子所需能量最大的是
A. [Ne]
 B. [Ne]
B. [Ne] 
C. [Ne]
 D. [Ne]
D. [Ne] 
(4)已知:分子中的大π键可用符号
 表示,其中m代表参与形成大π键的原子数,n代表参与形成的大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成的大π键的电子数(如苯分子中的大π键可表示为 ),则环戊二烯负离子(
),则环戊二烯负离子( )中的大π键应表示为
)中的大π键应表示为(5)二茂铁易升华且可溶于有机溶剂中,其晶体类型为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】金属晶体、离子晶体、共价晶体、分子晶体等模型都是典型的晶体结构模型,大多数实际晶体结构要复杂得多。
(1) 的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是____ 。
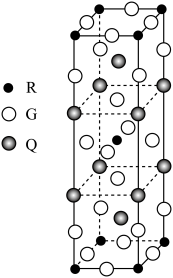
(2)如图是由Q、R、G三种元素组成的一种高温超导体的晶胞结构,其中R为+2价,G为-2价,则Q的化合价为_____ 。
(3)铜和氧形成的一种离子化合物是良好的半导体材料.晶胞结构如图所示:

铜离子的电荷数为______ ,其配位数为_______ ,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中a原子和b原子坐标分别为 、
、 ,则c原子分数坐标为
,则c原子分数坐标为______ ,若晶体密度为d g∙cm-3,设NA为阿伏加德罗常数的值,则晶胞中阴、阳离子最短距离为_____ nm(列出计算式即可)。
(1)
 的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |

(3)铜和氧形成的一种离子化合物是良好的半导体材料.晶胞结构如图所示:

铜离子的电荷数为
 、
、 ,则c原子分数坐标为
,则c原子分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】当下新能源汽车电池的发展加大了对金属钴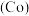 的需求,辉钴矿(主要成分是
的需求,辉钴矿(主要成分是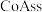 )是一种重要的含钴矿石。回答下列问题:
)是一种重要的含钴矿石。回答下列问题:
(1) 原子序数为33,基态砷原子价电子排布式为
原子序数为33,基态砷原子价电子排布式为___________ ,钴原子序数为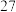 ,
, 有
有___________ 个未成对电子。
(2) 原子第一电离能高于34号元素的原因是
原子第一电离能高于34号元素的原因是___________ 。
(3)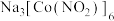 是一种检验
是一种检验 的试剂,其中
的试剂,其中 中N原子为
中N原子为___________ 杂化,空间构型名称为___________ 。
(4)一种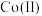 的配合物结构如下图,下列说法错误的是
的配合物结构如下图,下列说法错误的是___________ 。 配位数为6
配位数为6
b.结构中所有N原子均为 杂化
杂化___________ ,钴原子的配位数为___________ 。已知A点坐标为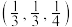 ,则B点坐标为
,则B点坐标为___________ ,晶胞参数分别为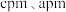 ,设
,设 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为___________  (列出计算式即可)。
(列出计算式即可)。
 的需求,辉钴矿(主要成分是
的需求,辉钴矿(主要成分是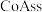 )是一种重要的含钴矿石。回答下列问题:
)是一种重要的含钴矿石。回答下列问题:(1)
 原子序数为33,基态砷原子价电子排布式为
原子序数为33,基态砷原子价电子排布式为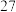 ,
, 有
有(2)
 原子第一电离能高于34号元素的原因是
原子第一电离能高于34号元素的原因是(3)
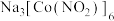 是一种检验
是一种检验 的试剂,其中
的试剂,其中 中N原子为
中N原子为(4)一种
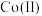 的配合物结构如下图,下列说法错误的是
的配合物结构如下图,下列说法错误的是
 配位数为6
配位数为6b.结构中所有N原子均为
 杂化
杂化c.结构
 中所有原子共平面
中所有原子共平面
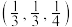 ,则B点坐标为
,则B点坐标为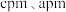 ,设
,设 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 (列出计算式即可)。
(列出计算式即可)。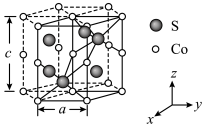
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
A的化合价_______ B的化合价(填“>”、“<”或“=”)。
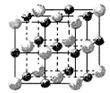
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如上图所示),其中3种离子晶体的晶格能数据如下表:
则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是:__________ 。其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有________ 个。
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是_________ 。
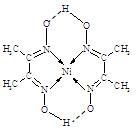
(4)某配合物的分子结构如上图所示,则N原子的杂化方式为________ ;基态Ni原子的电子排布式______________ 。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
A的化合价

(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如上图所示),其中3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是:
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是

(4)某配合物的分子结构如上图所示,则N原子的杂化方式为
您最近一年使用:0次



