加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。

①写出H2O2在二氧化锰作用下发生反应的化学方程式___________ 。
②实验时放出气体的总体积是________ mL。
③放出1/3气体所需时间为________ min。
④反应放出3/4气体所需时间约为_______ min。
⑤A、B、C、D各点反应速率由快到慢的顺序为_________ 。
⑥解释反应速率变化的原因____________ 。
⑦计算H2O2的初始物质的量浓度___________ 。(请保留两位有效数字)

①写出H2O2在二氧化锰作用下发生反应的化学方程式
②实验时放出气体的总体积是
③放出1/3气体所需时间为
④反应放出3/4气体所需时间约为
⑤A、B、C、D各点反应速率由快到慢的顺序为
⑥解释反应速率变化的原因
⑦计算H2O2的初始物质的量浓度
9-10高一下·吉林长春·阶段练习 查看更多[1]
(已下线)09~10学年长春外国语学校高一下学期第二次月考理科化学卷
更新时间:2010-06-28 14:41:38
|
相似题推荐
填空题
|
较易
(0.85)
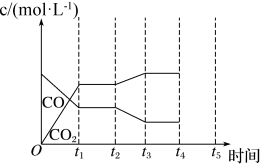
【推荐1】为顺应全球应对气候变化趋势和中国国情,我国提出了碳达峰碳中和的工作战略。以CO2生产甲醇(CH3OH)是实现“碳中和”的重要途径。在体积为2L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应得到CH3OH(g)和H2O(g),测得反应物CO2和CH3OH(g)的物质的量随时间的变化如图所示。

(1)写出该容器中物质发生反应的化学方程式_______
(2)0~3min内,υ(CH3OH)=_______ (保留两位有效数字) mol∙L−1∙min−1
(3)A点处的正反应速率比逆反应速率_______ (填“大”或“小”)
(4)10min后,能使该反应速率加快的措施有_______(填序号)。
(5)在相同温度、容积不变的条件下,不能 说明该反应已达平衡状态的是_______。
(6)若合成甲醇1.6t,则理论上可吸收工厂排放的CO2_______ L(标准状况下)。

(1)写出该容器中物质发生反应的化学方程式
(2)0~3min内,υ(CH3OH)=
(3)A点处的正反应速率比逆反应速率
(4)10min后,能使该反应速率加快的措施有_______(填序号)。
| A.降低反应温度 | B.充入2molCO2 | C.加入高效的催化剂 | D.充入适量氦气 |
| A.CO2、H2的浓度均不再变化 |
| B.体系压强不变 |
| C.n(CH3OH)∶n(H2O)=1∶1 |
| D.H2的消耗速率与CH3OH的生成速率之比为3∶1 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
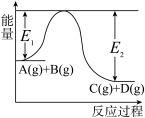
(1)该反应是__ 反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率_ (填“增大”“减小”“不变”),原因是__ 。
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_ ,E2_ ,ΔH_ (填“增大”“减小”“不变”)。
 C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是
(2)当反应达到平衡时,升高温度,A的转化率
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
(1)实验过程如下图所示,分析判断:________ 段化学反应速率最快,_______ 段收集的二氧化碳气体最多。
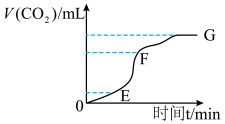
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是( )
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答两种)_______________
(1)实验过程如下图所示,分析判断:

(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答两种)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响,在常温下按照如下方案完成实验。
(1)催化剂能加快化学反应速率的原因_______ 。
(2)实验①和②的目的是_______ 。
(3)写出实验③的化学反应方程式:_______ 。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol • L-1 FeCl3溶液 |
| ④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol • L-1 FeCl3溶液 |
| ⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol • L-1 FeCl3溶液 |
(2)实验①和②的目的是
(3)写出实验③的化学反应方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】化学反应速率的影响因素
(1)内因
在相同条件下,反应速率首先是由反应物_______ 决定的。
(2)浓度对化学反应速率的影响
①浓度对化学反应速率的微观解释
反应物浓度增大→单位体积内活化分子数目_______ →单位时间内有效碰撞几率_______ →反应速率_______ ;反之,反应速率减慢。

②气体反应体系中充入惰性气体(不参与反应)时对反应速率的影响
恒容:充入“惰性气体”→总压_______ →物质浓度_______ (活化分子浓度不变)→反应速率_______ 。
恒压:充入“惰性气体”→体积_______ →物质浓度_______ (活化分子浓度减小)→反应速率_______ 。
(3)压强对化学反应速率的影响
①研究对象——气体模型的理解
对于气体来说,在一定温度下,一定质量的气体所占的体积与压强成_______ 。如图所示:
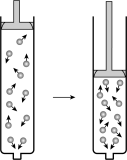
对于有气体参加的反应,在密闭容器中保持温度不变时,增大压强,气体体积_______ ,反应物浓度_______ ,化学反应速率_______ 。
②微观解释
增大压强→气体体积_______ →反应物浓度_______ →单位体积内活化分子数_______ →单位时间内有效碰撞几率_______ →反应速率_______ ;反之,反应速率_______ 。
(4)温度对化学反应速率的影响
①实验探究
②影响规律:其他条件相同时,升高温度,化学反应速率_______ ;降低温度,化学反应速率_______ 。经验规律,一般温度每升高10 K,反应速率可增加2~4倍。
③微观解释

反之,反应速率减小。
(5)催化剂对反应速率的影响
①实验探究。
②影响规律:当其他条件不变时,使用催化剂,化学反应速率_______ 。FeCl3、MnO2对H2O2的分解都有催化作用,都能加快H2O2的分解速率。
③用过渡态理论解释催化剂使化学反应速率增大
(1)内因
在相同条件下,反应速率首先是由反应物
(2)浓度对化学反应速率的影响
| 实验操作 |  |
| 实验现象 | 均出现浑浊,先后顺序为A、B、C |
| 实验结论 | c(Na2S2O3)增大,产生浑浊的速率加快 |
| 规律总结 | 其他条件相同时,增大反应物的浓度,反应速率 |
反应物浓度增大→单位体积内活化分子数目

②气体反应体系中充入惰性气体(不参与反应)时对反应速率的影响
恒容:充入“惰性气体”→总压
恒压:充入“惰性气体”→体积
(3)压强对化学反应速率的影响
①研究对象——气体模型的理解
对于气体来说,在一定温度下,一定质量的气体所占的体积与压强成

对于有气体参加的反应,在密闭容器中保持温度不变时,增大压强,气体体积
②微观解释
增大压强→气体体积
(4)温度对化学反应速率的影响
①实验探究
| 实验操作 |  |
| 实验现象 | 溶液紫红色褪去所需时间长短: |
| 实验结论 | 其他条件相同时,反应物的温度越高,反应速率越 |
③微观解释

反之,反应速率减小。
(5)催化剂对反应速率的影响
①实验探究。
| 原理 | 2H2O2 2H2O+O2↑ 2H2O+O2↑ |
| 实验操作 |   A B C |
| 实验现象 | A试管中有气泡产生;B试管中迅速产生大量气泡;C试管中只观察到有少量气泡产生 |
| 结论 | MnO2和FeCl3对H2O2分解都有催化作用,但MnO2催化作用较强,加入合适的催化剂能加快化学反应速率 |
③用过渡态理论解释催化剂使化学反应速率增大
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图所示:
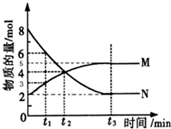
(1)比较t2时刻,正逆反应速率大小v正___________ v逆。(填“>”、“=”、“<”)
(2)若t2=2min,计算反应开始至t2时刻,M的平均化学反应速率为:___________
(3)t3时刻如果升高温度则v逆___________ (填增大、减小或不变)。

(1)比较t2时刻,正逆反应速率大小v正
(2)若t2=2min,计算反应开始至t2时刻,M的平均化学反应速率为:
(3)t3时刻如果升高温度则v逆
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】一定条件下,在容积为2L的密闭容器中发生反应:A(g)+3B(g)⇌2C(g)。开始时加入0.4molA,0.6molB,0.2molC,在2min末测得C的物质的量是0.3mol。
(1)用A的浓度变化表示反应的平均速率:_______ ,2min内A的转化率:_______ 。
(2)在2min末,B的浓度为_______ 。
(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”“不变”)
a.升高温度,化学反应速率_______ ;
b.充入1molB,化学反应速率_______ ;
c.将容器的容积变为3L,化学反应速率_______ 。
(1)用A的浓度变化表示反应的平均速率:
(2)在2min末,B的浓度为
(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”“不变”)
a.升高温度,化学反应速率
b.充入1molB,化学反应速率
c.将容器的容积变为3L,化学反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】T℃、2L密闭容器中某一反应不同时刻各物质的量如图(E为固体,其余为气体).回答下列问题:
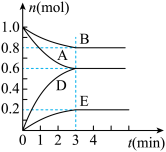
(1)写出该反应的化学方程式______________________________________ .
(2)反应开始至3min时,用D表示的平均反应速率为______ mol/(L•min).
(3)若升高温度,则v(正)________ ,v(逆)________ (填“加快”或“减慢”)。
(4)若反应在甲、乙两个相同容器内同时进行,分别测得甲中v(A)=0.3 mol·L-1·min-1,乙中v(B)=0.2 mol·L-1·min-1,则________ 容器中反应更快。

(1)写出该反应的化学方程式
(2)反应开始至3min时,用D表示的平均反应速率为
(3)若升高温度,则v(正)
(4)若反应在甲、乙两个相同容器内同时进行,分别测得甲中v(A)=0.3 mol·L-1·min-1,乙中v(B)=0.2 mol·L-1·min-1,则
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】结合教材“使用催化剂前后得活化能数据以及反应速率常数之比”有关数据,讨论交流:催化剂对化学反应速率有怎样的影响____ ?与其他因素相比,催化剂的影响程度如何____ ?为什么____ ?
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
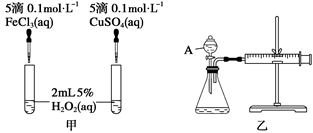
(1)定性分析:
①如图甲可通过观察_____________________________________ ,定性比较得出结论。
②有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是__________________ ,
③若H2O2在二氧化锰催化作用下发生反应,曾检测出有物质MnO3出现,写出整个反应过程的两个化学方程式:___________________________ ,________________________ 。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为________ ,实验中需要测量的数据是_________________ 。

(1)定性分析:
①如图甲可通过观察
②有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
③若H2O2在二氧化锰催化作用下发生反应,曾检测出有物质MnO3出现,写出整个反应过程的两个化学方程式:
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】氮及其化合物在工农业中应用非常广泛。
(1)1828年,德国化学家维勒(Friedrich Wohler)首次用加热的方法使无机物氰酸铵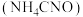 转化为有机化合物尿素
转化为有机化合物尿素 。已知氰酸铵在热水中就能发生分解,尿素加热至
。已知氰酸铵在热水中就能发生分解,尿素加热至 分解,分解时均产生氨气。
分解,分解时均产生氨气。
①氰酸铵属于_______ 化合物(选填“离子”或“共价”)。
②鉴别氰酸铵和尿素的实验方法是_______ 。
(2)液氨是富氢物质,是氢能的理想载体,利用合成氨可以实现储氢和输氢。合成氨时,在 催化剂作用下的反应历程如下表(*表示吸附态):其中,
催化剂作用下的反应历程如下表(*表示吸附态):其中, 的吸附分解反应速率慢,决定了合成氨的整体反应速率。
的吸附分解反应速率慢,决定了合成氨的整体反应速率。
①采用液化空气分离的方法可获得原料气中 。先将空气液化后再汽化,液态空气汽化时首先分离出
。先将空气液化后再汽化,液态空气汽化时首先分离出_______ 。
②高温高压时,在催化剂作用下,已知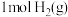 参加反应生成
参加反应生成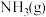 放出
放出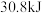 的热量。则合成氨的热化学方程式为
的热量。则合成氨的热化学方程式为_______ 。
③实际生产中,原料气中 和
和 物质的量之比为1∶2.8。试分析说明原料气中
物质的量之比为1∶2.8。试分析说明原料气中 适度过量有利于提高整体反应速率的原因:
适度过量有利于提高整体反应速率的原因:_______ 。
(3)在低温,加压的条件下,氨气与二氧化碳可以合成尿素。试写出氨气与二氧化碳生成尿素和水的化学方程式:_______ 。
(1)1828年,德国化学家维勒(Friedrich Wohler)首次用加热的方法使无机物氰酸铵
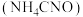 转化为有机化合物尿素
转化为有机化合物尿素 。已知氰酸铵在热水中就能发生分解,尿素加热至
。已知氰酸铵在热水中就能发生分解,尿素加热至 分解,分解时均产生氨气。
分解,分解时均产生氨气。①氰酸铵属于
②鉴别氰酸铵和尿素的实验方法是
(2)液氨是富氢物质,是氢能的理想载体,利用合成氨可以实现储氢和输氢。合成氨时,在
 催化剂作用下的反应历程如下表(*表示吸附态):其中,
催化剂作用下的反应历程如下表(*表示吸附态):其中, 的吸附分解反应速率慢,决定了合成氨的整体反应速率。
的吸附分解反应速率慢,决定了合成氨的整体反应速率。| 化学吸附 |  | 表面反应 |  | 脱附 |
 | 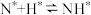 | 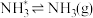 | ||
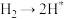 | 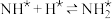 | |||
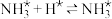 |
 。先将空气液化后再汽化,液态空气汽化时首先分离出
。先将空气液化后再汽化,液态空气汽化时首先分离出②高温高压时,在催化剂作用下,已知
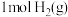 参加反应生成
参加反应生成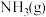 放出
放出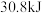 的热量。则合成氨的热化学方程式为
的热量。则合成氨的热化学方程式为③实际生产中,原料气中
 和
和 物质的量之比为1∶2.8。试分析说明原料气中
物质的量之比为1∶2.8。试分析说明原料气中 适度过量有利于提高整体反应速率的原因:
适度过量有利于提高整体反应速率的原因:(3)在低温,加压的条件下,氨气与二氧化碳可以合成尿素。试写出氨气与二氧化碳生成尿素和水的化学方程式:
您最近一年使用:0次

 H2(g)+CO2(g)
H2(g)+CO2(g)