下列四组溶液的pH前者大于后者的是
| A.物质的量浓度相同的盐酸和CH3COOH溶液 |
| B.物质的量浓度相同的NaOH溶液和氨水 |
| C.pH=3的盐酸和pH=3的NH4Cl溶液均稀释100倍所得溶液 |
| D.pH=10的NaOH溶液和pH=10的CH3COONa溶液均稀释100倍所得溶液 |
10-11高二上·湖南·阶段练习 查看更多[1]
(已下线)2010年海南省嘉积中学高二上学期第二次月考化学试卷
更新时间:2016-12-09 01:19:33
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】常温时,下列溶液的pH等于8或大于8的是
| A.0.1 mol·L-1的NaOH溶液滴定稀盐酸,用酚酞做指示剂滴定到终点 |
| B.pH=6的醋酸用水稀释100倍 |
| C.pH=10的氢氧化钠溶液稀释1000倍 |
| D.0.1 mol·L-1的硫酸100 mL跟0.2 mol·L-1 NaOH溶液150 mL完全反应 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】 时,用浓度为
时,用浓度为 的
的 溶液滴定体积均是
溶液滴定体积均是 、浓度均为
、浓度均为 的三种酸
的三种酸 、
、 、
、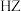 ,滴定曲线如图所示,下列说法
,滴定曲线如图所示,下列说法不正确 的是

 时,用浓度为
时,用浓度为 的
的 溶液滴定体积均是
溶液滴定体积均是 、浓度均为
、浓度均为 的三种酸
的三种酸 、
、 、
、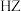 ,滴定曲线如图所示,下列说法
,滴定曲线如图所示,下列说法
A.酸性由强到弱的顺序是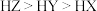 |
B.HZ为强酸,将pH=6的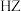 溶液加水稀释 溶液加水稀释 倍, 倍, 为 为 |
C. 为弱酸,其电离常数数量级约为 为弱酸,其电离常数数量级约为 |
D.加入 溶液时,均恰好完全反应,溶液均呈中性 溶液时,均恰好完全反应,溶液均呈中性 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】常温下,将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A.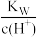 >1.0×10-7 mol·L-1 >1.0×10-7 mol·L-1 |
B.c(Na+)=c( )+c( )+c( )+c(H2CO3) )+c(H2CO3) |
C.c(H+)+c( )=c(OH-)+c( )=c(OH-)+c( )+2c( )+2c( ) ) |
D.c(Cl-)>c( )>c( )>c( )>c( )>c( ) ) |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】现有常温下的四份溶液:①0.01 mol/L CH3COOH;②0.01 mol/L HCl;③pH=12的氨水;④pH=12的NaOH溶液。下列说法正确的是
| A.①中水的电离程度最小,③中水的电离程度最大 |
| B.将②、③混合,若有pH=7,则消耗溶液的体积:②>③ |
| C.将①、④混合,若有c(CH3COO-)>c(H+),则混合液一定呈碱性 |
| D.将四份溶液稀释相同倍数后,溶液的pH:③>④,①>② |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数Ka1=4×10-7,H2S的电离平衡常数Ka1=6×10-8。若溶液混合引起的体积变化可忽略,则室温时下列指定溶液中微粒物质的量浓度关系正确的是
A.0.1mol·L-1的NH4HS溶液:c(HS-)>c( )>c(NH3·H2O)>c(H2S) )>c(NH3·H2O)>c(H2S) |
B.0.1mol·L-1的NH4HS溶液和0.1mol·L-1的NH4HCO3溶液等体积混合:c( )+c(NH3·H2O)=c(H2CO3)+c( )+c(NH3·H2O)=c(H2CO3)+c( )+c( )+c( )+c(H2S)+c(HS-)+c(S2-) )+c(H2S)+c(HS-)+c(S2-) |
C.0.1mol·L-1的(NH4)2CO3和0.1mol·L-1的NH4HCO3溶液等体积混合:c(HCO )+2c(CO )+2c(CO )<0.15mol·L-1 )<0.15mol·L-1 |
D.0.4mol·L-1氨水和0.2mol·L-1的NH4HCO3溶液等体积混合:c(NH3·H2O)+c(OH-)+c(CO )=0.1mol·L-1+c(H2CO3)+c(H+) )=0.1mol·L-1+c(H2CO3)+c(H+) |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】 易水解,是常见的抗氧化剂。实验室以
易水解,是常见的抗氧化剂。实验室以 为原料制备
为原料制备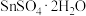 的流程如下:
的流程如下:

下列说法错误的是
 易水解,是常见的抗氧化剂。实验室以
易水解,是常见的抗氧化剂。实验室以 为原料制备
为原料制备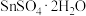 的流程如下:
的流程如下:
下列说法错误的是
A.溶解时,将 固体直接溶解在热水里 固体直接溶解在热水里 |
B.反应1的离子方程式为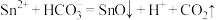 |
C.可用 酸化的 酸化的 溶液检验SnO沉淀是否已被洗涤干净 溶液检验SnO沉淀是否已被洗涤干净 |
| D.操作1为蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.向稀醋酸溶液中加入少量醋酸钠固体,醋酸的电离程度增大 |
| B.电镀时,通常把待镀金属制品作阴极,镀层金属作阳极 |
| C.常温下,2NO2(g)=2NO(g)+O2(g)不能自发进行,则该反应的△H>0 |
D.工业通过反应“Na(l) +KCl(l)  NaCl(l)+K(g)”冶炼钾,说明钠的金属性强于钾 NaCl(l)+K(g)”冶炼钾,说明钠的金属性强于钾 |
您最近一年使用:0次


 2NH3(g)平衡体系中加入催化剂,N2的反应速率和转化率均增大
2NH3(g)平衡体系中加入催化剂,N2的反应速率和转化率均增大

