空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
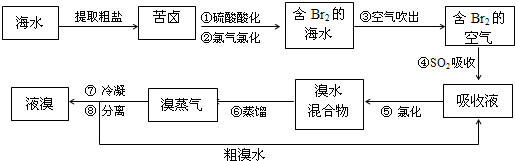
(1)步骤①中叫硫酸酸化可提高Cl2的利用率,理由是_______________ 。
(2)步骤④利用了SO2的还原性,反应的离子方程式为_______________ 。
(3)步骤⑥的蒸馏过程中,温度应控制在80〜90℃。温度过高或过低都不利于生产,请解释原因_______ 。
(4)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是______ 。
(5)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是_____ 。

(1)步骤①中叫硫酸酸化可提高Cl2的利用率,理由是
(2)步骤④利用了SO2的还原性,反应的离子方程式为
(3)步骤⑥的蒸馏过程中,温度应控制在80〜90℃。温度过高或过低都不利于生产,请解释原因
(4)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是
(5)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是
更新时间:2016-09-06 13:37:36
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.磷酸亚铁锂( )可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,以钛铁矿(主要成分为
)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,以钛铁矿(主要成分为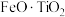 ,还含有MgO、CaO、
,还含有MgO、CaO、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如下,回答下列问题:
)的工艺流程如下,回答下列问题:

(1)在周期表中,根据对角线规则Li与Mg、Be与Al、B与Si的化学性质相似,写出 与NaOH反应的化学方程式
与NaOH反应的化学方程式_______ 。
(2)元素Fe基态原子的价层电子轨道表示式为_______ 。
(3)①“溶钛”过程反应温度不能太高,其原因是_______ 。
②“煅烧”制备 过程中,
过程中, 和
和 的理论投入量的物质的量之比为
的理论投入量的物质的量之比为_______ 。
Ⅱ.氮的相关化合物在材料等方面有重要用途。回答下列问题:
(4)科学家从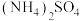 中检出一种组成为
中检出一种组成为 的物质,经测定,该物质易溶于水,在水中以
的物质,经测定,该物质易溶于水,在水中以 和
和 两种离子的形式存在。
两种离子的形式存在。 的空间构型与
的空间构型与 相同,写出
相同,写出 的结构式
的结构式_______ 。
(5)科学家合成了一种阳离子为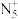 ,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键,呈V形;此后又合成了一种含有
,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键,呈V形;此后又合成了一种含有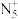 化学式为
化学式为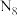 的离子晶体,其阳离子电子式为
的离子晶体,其阳离子电子式为_______ ,阴离子的空间构型为_______ 。
 )可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,以钛铁矿(主要成分为
)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,以钛铁矿(主要成分为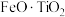 ,还含有MgO、CaO、
,还含有MgO、CaO、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如下,回答下列问题:
)的工艺流程如下,回答下列问题:
(1)在周期表中,根据对角线规则Li与Mg、Be与Al、B与Si的化学性质相似,写出
 与NaOH反应的化学方程式
与NaOH反应的化学方程式(2)元素Fe基态原子的价层电子轨道表示式为
(3)①“溶钛”过程反应温度不能太高,其原因是
②“煅烧”制备
 过程中,
过程中, 和
和 的理论投入量的物质的量之比为
的理论投入量的物质的量之比为Ⅱ.氮的相关化合物在材料等方面有重要用途。回答下列问题:
(4)科学家从
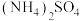 中检出一种组成为
中检出一种组成为 的物质,经测定,该物质易溶于水,在水中以
的物质,经测定,该物质易溶于水,在水中以 和
和 两种离子的形式存在。
两种离子的形式存在。 的空间构型与
的空间构型与 相同,写出
相同,写出 的结构式
的结构式(5)科学家合成了一种阳离子为
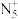 ,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键,呈V形;此后又合成了一种含有
,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键,呈V形;此后又合成了一种含有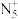 化学式为
化学式为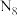 的离子晶体,其阳离子电子式为
的离子晶体,其阳离子电子式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硼氢化钠(NaBH4)具有优良的还原性,在有机化学和无机化学领域有着广泛的应用。利用硼精矿(主要成分为B2O3,含有少量Al2O3、SiO2、FeCl3等 制取NaBH4的流程如图:
制取NaBH4的流程如图:

已知:偏硼酸钠(NaBO2)易溶于水,不溶于醇,在碱性条件下稳定存在,回答下列问题:
(1)写出加快硼精矿溶解速率的措施______  写一种
写一种 。
。
(2)操作1为______ ,滤渣主要成分为______ 。
(3)除硅铝步骤加入CaO而不加入CaCl2的原因有:①能将硅、铝以沉淀除去;②______ .
(4)氢化镁(MgH2)中H元素的化合价为______ ;MgH2与NaBO2在一定条件下发生反应1,其化学方程式为:______ 。
(5)如图在碱性条件下,在阴极上电解NaBO2也可制得硼氢化钠,写出阴极室的电极反应式______ 。

(6)硼氢化钠是一种强还原剂,碱性条件可处理电镀废液中的硫酸铜制得纳米铜,从而变废为宝,写出该反应的离子方程式______ 。
 制取NaBH4的流程如图:
制取NaBH4的流程如图:
已知:偏硼酸钠(NaBO2)易溶于水,不溶于醇,在碱性条件下稳定存在,回答下列问题:
(1)写出加快硼精矿溶解速率的措施
 写一种
写一种 。
。(2)操作1为
(3)除硅铝步骤加入CaO而不加入CaCl2的原因有:①能将硅、铝以沉淀除去;②
(4)氢化镁(MgH2)中H元素的化合价为
(5)如图在碱性条件下,在阴极上电解NaBO2也可制得硼氢化钠,写出阴极室的电极反应式

(6)硼氢化钠是一种强还原剂,碱性条件可处理电镀废液中的硫酸铜制得纳米铜,从而变废为宝,写出该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】钼酸钠晶体( )可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为
)可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为 ,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。

请回答下列问题:
(1) 中Mo的化合价为
中Mo的化合价为___________
(2)“焙烧”时,有 生成,反应的化学方程式为
生成,反应的化学方程式为___________ ,氧化产物是___________
(3)“碱浸”生成 和另外一种物质,
和另外一种物质, 的电子式为
的电子式为___________ ,另外一种生成物的化学式为___________
(4)若“除重金属离子”时加入的沉淀剂为 ,则废渣的成分为
,则废渣的成分为___________  填化学式
填化学式
(5)测得“除重金属离子”中部分离子的浓度: “结晶”前应先除去
“结晶”前应先除去 ,方法是加入
,方法是加入 固体。假设加入
固体。假设加入 固体后溶液体积不变,当
固体后溶液体积不变,当 开始沉淀时,去除的
开始沉淀时,去除的 的质量分数为
的质量分数为___________  已知
已知
 )可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为
)可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为 ,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
请回答下列问题:
(1)
 中Mo的化合价为
中Mo的化合价为(2)“焙烧”时,有
 生成,反应的化学方程式为
生成,反应的化学方程式为(3)“碱浸”生成
 和另外一种物质,
和另外一种物质, 的电子式为
的电子式为(4)若“除重金属离子”时加入的沉淀剂为
 ,则废渣的成分为
,则废渣的成分为 填化学式
填化学式
(5)测得“除重金属离子”中部分离子的浓度:
 “结晶”前应先除去
“结晶”前应先除去 ,方法是加入
,方法是加入 固体。假设加入
固体。假设加入 固体后溶液体积不变,当
固体后溶液体积不变,当 开始沉淀时,去除的
开始沉淀时,去除的 的质量分数为
的质量分数为 已知
已知
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】某研究小组以硫化铜精矿(含Zn、Fe元素的杂质)为主要原料制备Cu粉,按如下流程开展实验:
已知:

①硫化铜精矿在酸性条件下与氧气反应:
②金属离子开始沉淀和沉淀完全的pH值如下表所示:
(1)步骤Ⅰ,通入 采用高压的原因是
采用高压的原因是___________ ;
(2)下列有关说法正确的是___________。
(3)步骤Ⅰ、Ⅲ需要高压反应釜装置如图。步骤Ⅲ中,首先关闭出气口,向高压反应釜中通入固定流速的 ,然后通过控制气阀
,然后通过控制气阀 或
或 ,维持反应釜中的压强为
,维持反应釜中的压强为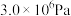 。请给出反应过程中的操作排序:
。请给出反应过程中的操作排序:______
g→___________→___________→___________→c→___________。

a.开启气阀 b.开启气阀
b.开启气阀 ,通入高压
,通入高压 c.关闭气阀
c.关闭气阀 d.开启气阀
d.开启气阀 e.开启气阀
e.开启气阀 ,通入高压
,通入高压 f.关闭气阀
f.关闭气阀 g.开启搅拌器 h.拆下罐体
g.开启搅拌器 h.拆下罐体
(4)步骤Ⅲ,高压 可以从滤液中置换出金属Cu,而无法置换出金属Zn。请结合方程式说明其原因是
可以从滤液中置换出金属Cu,而无法置换出金属Zn。请结合方程式说明其原因是___________ ;
(5)铜纯度的测定
步骤1:取0.200g粗铜,加入一定量浓 、浓HCl,微热至粗铜完全溶解后,控制溶液pH为3~4,加热除去未反应的
、浓HCl,微热至粗铜完全溶解后,控制溶液pH为3~4,加热除去未反应的 ,冷却;
,冷却;
步骤2:将步骤1所得溶液加水定容至250mL,量取25.00mL置于锥形瓶中,加入过量KI溶液,再加入少量淀粉溶液,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液30.00mL。
溶液30.00mL。
已知: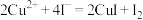 ,
,
①产品中铜的质量分数为___________ ;
②测定过程中,下列说法正确的是___________ 。
A.步骤1中若未反应的 未除尽,则导致滴定结果偏低
未除尽,则导致滴定结果偏低
B.步骤2中应先用蒸馏水洗涤酸式滴定管后,再用硫代硫酸钠标准液润洗
C.滴定过程中,若向锥形瓶内加少量蒸馏水,则滴定结果偏低
D.滴定前平视刻度线,滴定后仰视,则测定的结果偏高
已知:

①硫化铜精矿在酸性条件下与氧气反应:

②金属离子开始沉淀和沉淀完全的pH值如下表所示:
 |  |  |  |
| 开始沉淀pH | 1.9 | 4.2 | 6.2 |
| 沉淀完全pH | 3.2 | 6.7 | 8.2 |
(1)步骤Ⅰ,通入
 采用高压的原因是
采用高压的原因是(2)下列有关说法正确的是___________。
| A.步骤Ⅰ,过滤得到的滤渣中含有S |
B.步骤Ⅱ, 调节pH至4,使 调节pH至4,使 、 、 沉淀完全 沉淀完全 |
| C.步骤Ⅲ,增加溶液的酸度不利于Cu生成 |
| D.为加快过滤速率,需用玻璃棒对漏斗中的沉淀进行充分搅拌 |
(3)步骤Ⅰ、Ⅲ需要高压反应釜装置如图。步骤Ⅲ中,首先关闭出气口,向高压反应釜中通入固定流速的
 ,然后通过控制气阀
,然后通过控制气阀 或
或 ,维持反应釜中的压强为
,维持反应釜中的压强为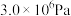 。请给出反应过程中的操作排序:
。请给出反应过程中的操作排序:g→___________→___________→___________→c→___________。

a.开启气阀
 b.开启气阀
b.开启气阀 ,通入高压
,通入高压 c.关闭气阀
c.关闭气阀 d.开启气阀
d.开启气阀 e.开启气阀
e.开启气阀 ,通入高压
,通入高压 f.关闭气阀
f.关闭气阀 g.开启搅拌器 h.拆下罐体
g.开启搅拌器 h.拆下罐体(4)步骤Ⅲ,高压
 可以从滤液中置换出金属Cu,而无法置换出金属Zn。请结合方程式说明其原因是
可以从滤液中置换出金属Cu,而无法置换出金属Zn。请结合方程式说明其原因是(5)铜纯度的测定
步骤1:取0.200g粗铜,加入一定量浓
 、浓HCl,微热至粗铜完全溶解后,控制溶液pH为3~4,加热除去未反应的
、浓HCl,微热至粗铜完全溶解后,控制溶液pH为3~4,加热除去未反应的 ,冷却;
,冷却;步骤2:将步骤1所得溶液加水定容至250mL,量取25.00mL置于锥形瓶中,加入过量KI溶液,再加入少量淀粉溶液,用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液30.00mL。
溶液30.00mL。已知:
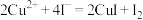 ,
,
①产品中铜的质量分数为
②测定过程中,下列说法正确的是
A.步骤1中若未反应的
 未除尽,则导致滴定结果偏低
未除尽,则导致滴定结果偏低B.步骤2中应先用蒸馏水洗涤酸式滴定管后,再用硫代硫酸钠标准液润洗
C.滴定过程中,若向锥形瓶内加少量蒸馏水,则滴定结果偏低
D.滴定前平视刻度线,滴定后仰视,则测定的结果偏高
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】某地以高硫铝土矿 主要含Al2O3、Fe2O3、SiO2和少量的FeS2等
主要含Al2O3、Fe2O3、SiO2和少量的FeS2等 提取氧化铝和磁性氧化铁,直接碱溶法往往形成铝硅酸钠沉淀[NamAlmSinO16(OH)5]而造成铝损失。一种改进后的流程如下:
提取氧化铝和磁性氧化铁,直接碱溶法往往形成铝硅酸钠沉淀[NamAlmSinO16(OH)5]而造成铝损失。一种改进后的流程如下:
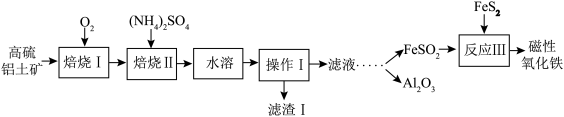
⑴铁在元素周期表中的位置是________________ ;NamAlmSinO16(OH)5中的m和n之间满足什么样的代数式________ ;写出滤渣Ⅰ主要成分的一种用途:________________________ ;反应Ⅲ加入FeS2的目的是作为________________________  填“氧化剂”或“还原剂”
填“氧化剂”或“还原剂” 。
。
⑵焙烧Ⅰ过程中会产生大量红棕色烟尘和SO2气体,写出产生这一现象的化学方程式:________________________________________________ 。
⑶焙烧Ⅱ由氧化铝、氧化铁制得可溶性的NH4Al(SO4)2、NH4Fe(SO4)2。提取率随温度、时间变化曲线如图所示,最佳的焙烧时间与温度是________________ 。若以NH4R(SO4)2表示NH4Al(SO4)2、NH4Fe(SO4)2,相关的化学反应方程式为________________________ 。
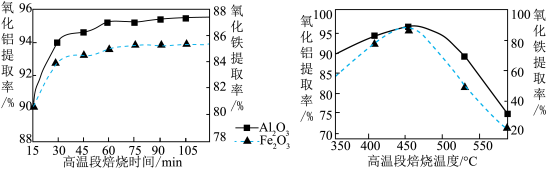
⑷下列有关铝硅酸钠[NamAlmSinO16(OH)5]中所含元素性质的说法正确的是________ 。
A.因为原子半径:Na > S,所以离子半径:Na+ > S2-
B.因为非金属性:S > Si,所以简单气态氢化物稳定性:SiH4 < H2S
C.因为非金属性:O > S,所以沸点; H2S > H2O
D.因为金属性:Na > Al,所以碱性:NaOH > Al(OH)3
⑸为了测定Wg高硫铝土矿中铝元素的含量,将流程中制取的Al2O3溶解于足量稀硫酸,配成250mL溶液,取出25mL,加入c mol·L-1 EDTA标准溶液amL,调节溶液pH约为4.2,煮沸,冷却后用b mol·L-1 CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液V mL(已知Al3+、Cu2+与EDTA反应的化学计量比均为1:1)。则Wg高硫铝土矿中铝元素的质量分数为________________________  用含V、W、a、b、c的代数式表示
用含V、W、a、b、c的代数式表示 。
。
 主要含Al2O3、Fe2O3、SiO2和少量的FeS2等
主要含Al2O3、Fe2O3、SiO2和少量的FeS2等 提取氧化铝和磁性氧化铁,直接碱溶法往往形成铝硅酸钠沉淀[NamAlmSinO16(OH)5]而造成铝损失。一种改进后的流程如下:
提取氧化铝和磁性氧化铁,直接碱溶法往往形成铝硅酸钠沉淀[NamAlmSinO16(OH)5]而造成铝损失。一种改进后的流程如下: 
⑴铁在元素周期表中的位置是
 填“氧化剂”或“还原剂”
填“氧化剂”或“还原剂” 。
。⑵焙烧Ⅰ过程中会产生大量红棕色烟尘和SO2气体,写出产生这一现象的化学方程式:
⑶焙烧Ⅱ由氧化铝、氧化铁制得可溶性的NH4Al(SO4)2、NH4Fe(SO4)2。提取率随温度、时间变化曲线如图所示,最佳的焙烧时间与温度是

⑷下列有关铝硅酸钠[NamAlmSinO16(OH)5]中所含元素性质的说法正确的是
A.因为原子半径:Na > S,所以离子半径:Na+ > S2-
B.因为非金属性:S > Si,所以简单气态氢化物稳定性:SiH4 < H2S
C.因为非金属性:O > S,所以沸点; H2S > H2O
D.因为金属性:Na > Al,所以碱性:NaOH > Al(OH)3
⑸为了测定Wg高硫铝土矿中铝元素的含量,将流程中制取的Al2O3溶解于足量稀硫酸,配成250mL溶液,取出25mL,加入c mol·L-1 EDTA标准溶液amL,调节溶液pH约为4.2,煮沸,冷却后用b mol·L-1 CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液V mL(已知Al3+、Cu2+与EDTA反应的化学计量比均为1:1)。则Wg高硫铝土矿中铝元素的质量分数为
 用含V、W、a、b、c的代数式表示
用含V、W、a、b、c的代数式表示 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】某含钒石煤中钒的主要存在形式为V2O3,采取钙法焙烧提钒并制备V2O5的工艺流程如下:
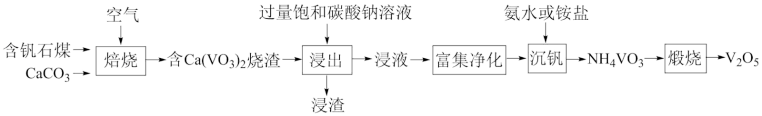
回答下列问题:
(1)写出一种可加快“焙烧”速率的方法___________ ,“焙烧”过程中发生反应的化学方程式为___________ 。
(2)“浸出”过程发生的离子方程式为___________ 。
(3)NH4VO3溶解度较小,可以晶体形式析出。“沉钒”时,要使所加铵盐应过量,目的是___________ 。
(4)“煅烧”过程中的副产物可在“___________ ”过程中循环使用。
(5)VOSO4是制作钒电池的重要原料,可在硫酸溶液中用SO2将V2O5还原得到,该反应的化学方程式为___________ ;已知钒电池的工作原理为 +V2++2H+
+V2++2H+ VO2++V3++H2O,则该电池放电时的正极反应式为
VO2++V3++H2O,则该电池放电时的正极反应式为___________ 。

回答下列问题:
(1)写出一种可加快“焙烧”速率的方法
(2)“浸出”过程发生的离子方程式为
(3)NH4VO3溶解度较小,可以晶体形式析出。“沉钒”时,要使所加铵盐应过量,目的是
(4)“煅烧”过程中的副产物可在“
(5)VOSO4是制作钒电池的重要原料,可在硫酸溶液中用SO2将V2O5还原得到,该反应的化学方程式为
 +V2++2H+
+V2++2H+ VO2++V3++H2O,则该电池放电时的正极反应式为
VO2++V3++H2O,则该电池放电时的正极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】海水是一种重要的自然资源,利用海水可得到一系列产品。根据下列流程回答问题:

熔点:MgO 2800℃;MgCl2 712℃。
(1)从海水中获得淡水的主要方法有电渗析法、蒸馏法和________ (填一种方法)。
(2)工业上常用的一种“提溴”技术叫做“吹出法”,其过程主要包括氧化、吹出、吸收、蒸馏等环节,“氧化”工序中发生的主要反应是________ (用离子方程式表示)。
(3)“产品A”的主要成分是______ (填化学式)。
(4)“提镁”工序获取氢氧化镁操作的名称是_____ ;由氢氧化镁进一步加工获得的MgCl2可用于电解法获取镁单质。冶炼镁时,电解熔融MgCl2而不电解熔融MgO的原因是______ 。将铝和镁作电极插入氢氧化钠溶液中,作负极的是______ (填化学式);写出正极的电极反应式:______ 。
(5)侯德榜是我国近代化学工业的奠基人,在经过数百次的试验后,侯德榜终于确定了制备纯碱的新工艺。该新工艺制备纯碱的方法为将二氧化碳和氨气通入饱和食盐水中获得碳酸氢钠和氯化铵,为了提高产率,应往饱和食盐水中先通入______ (填化学式,下同),后通入______ ,写出该方法中获得碳酸氢钠和氯化铵的化学方程式:______ 。

熔点:MgO 2800℃;MgCl2 712℃。
(1)从海水中获得淡水的主要方法有电渗析法、蒸馏法和
(2)工业上常用的一种“提溴”技术叫做“吹出法”,其过程主要包括氧化、吹出、吸收、蒸馏等环节,“氧化”工序中发生的主要反应是
(3)“产品A”的主要成分是
(4)“提镁”工序获取氢氧化镁操作的名称是
(5)侯德榜是我国近代化学工业的奠基人,在经过数百次的试验后,侯德榜终于确定了制备纯碱的新工艺。该新工艺制备纯碱的方法为将二氧化碳和氨气通入饱和食盐水中获得碳酸氢钠和氯化铵,为了提高产率,应往饱和食盐水中先通入
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】溴及其化合物广泛用于医药、塑料阻燃剂等,苦卤提溴的工业流程如下:

(1)Cl2和苦卤中的Br-反应生成Br2的离子方程式是_____ 。
(2)结合元素周期律解释Cl的非金属性强于Br的原因:_____ 。
(3)吸收塔中,A吸收了Br2后的溶液中含有Br-和BrO ,则A是
,则A是_____ (填序号)。
a.NaCl溶液 b.Na2CO3溶液 c.SO2气体
(4)从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是_____ 。

(1)Cl2和苦卤中的Br-反应生成Br2的离子方程式是
(2)结合元素周期律解释Cl的非金属性强于Br的原因:
(3)吸收塔中,A吸收了Br2后的溶液中含有Br-和BrO
 ,则A是
,则A是a.NaCl溶液 b.Na2CO3溶液 c.SO2气体
(4)从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是
您最近一年使用:0次
【推荐3】海洋资源的利用具有非常广阔的前景。
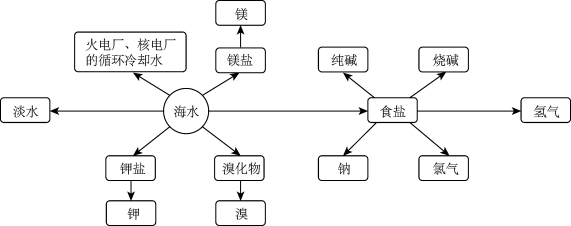
回答下列问题:
Ⅰ.海水制盐
(1)粗盐中可溶性杂质离子包含 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂、操作的顺序可为
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂、操作的顺序可为_______ (填字母)。
a.NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸、过滤
b.NaOH溶液、Na2CO3溶液、BaCl2溶液、过滤、盐酸
c.BaCl2溶液、Na2CO3溶液、NaOH溶液、过滤、盐酸
(2)精盐可用于工业冶炼钠,请写出相应化学方程式_______ 。
Ⅱ.海水提溴
(3)工业上常用“吹出法”提溴,请写出用SO2吸收Br2的化学反应方程式_______ 。
(4)含Br2的海水经“空气吹出、SO2吸收、通入氯气”后再蒸馏的目的是_______ 。
Ⅲ.从海带中提取碘的实验过程如下图所示:
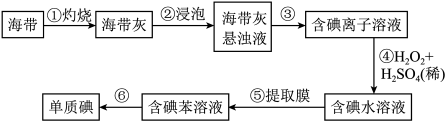
(5)步骤①中灼烧海带时,应将海带放入_______ (填仪器名称)中灼烧。
(6)请写出步骤④反应的离子方程式_______ 。
Ⅳ.海水提镁
(7)工业上为了将MgCl2溶液转化为Mg(OH)2,应加入的试剂为_______ (填化学式)。最后冶炼镁是将Mg(OH)2转化为_______ (填化学式)电解。

回答下列问题:
Ⅰ.海水制盐
(1)粗盐中可溶性杂质离子包含
 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂、操作的顺序可为
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂、操作的顺序可为a.NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸、过滤
b.NaOH溶液、Na2CO3溶液、BaCl2溶液、过滤、盐酸
c.BaCl2溶液、Na2CO3溶液、NaOH溶液、过滤、盐酸
(2)精盐可用于工业冶炼钠,请写出相应化学方程式
Ⅱ.海水提溴
(3)工业上常用“吹出法”提溴,请写出用SO2吸收Br2的化学反应方程式
(4)含Br2的海水经“空气吹出、SO2吸收、通入氯气”后再蒸馏的目的是
Ⅲ.从海带中提取碘的实验过程如下图所示:

(5)步骤①中灼烧海带时,应将海带放入
(6)请写出步骤④反应的离子方程式
Ⅳ.海水提镁
(7)工业上为了将MgCl2溶液转化为Mg(OH)2,应加入的试剂为
您最近一年使用:0次



