 )可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,以钛铁矿(主要成分为
)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,以钛铁矿(主要成分为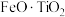 ,还含有MgO、CaO、
,还含有MgO、CaO、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如下,回答下列问题:
)的工艺流程如下,回答下列问题:
(1)在周期表中,根据对角线规则Li与Mg、Be与Al、B与Si的化学性质相似,写出
 与NaOH反应的化学方程式
与NaOH反应的化学方程式(2)元素Fe基态原子的价层电子轨道表示式为
(3)①“溶钛”过程反应温度不能太高,其原因是
②“煅烧”制备
 过程中,
过程中, 和
和 的理论投入量的物质的量之比为
的理论投入量的物质的量之比为Ⅱ.氮的相关化合物在材料等方面有重要用途。回答下列问题:
(4)科学家从
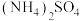 中检出一种组成为
中检出一种组成为 的物质,经测定,该物质易溶于水,在水中以
的物质,经测定,该物质易溶于水,在水中以 和
和 两种离子的形式存在。
两种离子的形式存在。 的空间构型与
的空间构型与 相同,写出
相同,写出 的结构式
的结构式(5)科学家合成了一种阳离子为
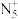 ,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键,呈V形;此后又合成了一种含有
,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键,呈V形;此后又合成了一种含有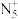 化学式为
化学式为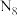 的离子晶体,其阳离子电子式为
的离子晶体,其阳离子电子式为相似题推荐
(1)在第二周期中(稀有气体除外),第一电离能最大的元素的原子结构示意图是
(2)第四周期元素中,4p轨道半充满的元素是
(3)中国古代四大发明之一——黑火药,它的爆炸反应方程式为:
2KNO3+3C+S
 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)①除K、S外,上述方程式中出现的元素形成氢化物的稳定性从大到小依次为
②写出K的基态电子排布式
(1)Fe位于元素周期表的
(2)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色。该反应在有的教材中用方程式FeCl3+3KSCN=Fe(SCN)3+3KCl表示。经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
①所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子显红色。含该离子的配合物的化学式是
②铁的另一种配合物铁氰化钾K3[Fe(CN)6]俗称赤血盐,可用于检验Fe2+,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理
(3)Cu的某种化合物的结构如图所示,该化合物中既含有配位键,又含有氢键,其中配位键和氢键均采用虚线表示。
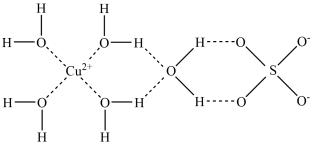
0.5mol该化合物中含有σ键的个数为
回答下列问题:
(1)X是
(2)P-的电子排布式
(3)在Z、W、P三种元素的简单离子中,半径最小的是
(4)向含Q离子的硫酸盐浴液中滴加氨水,有沉淀析出,再向溶液中滴加足量氨水,沉淀逐渐溶解,分别写出上述实验现象涉及的两个离子反应方程式:

(1)元素Na的价电子被激发到相邻高能级后形成激发态Na原子,其价电子轨道表示式为
(2)除了NaCl,Cl元素还能形成多种价态的化合物,如NaClO、NaClO2、NaClO3、NaClO4,这四种钠盐对应的酸的酸性依次增强,试解释HClO4的酸性强于HClO3的原因:
(3)在适当的条件下,电解NaCl水溶液可制得NaClO3。
①NaCl水溶液中,不存在的微粒间作用力有
A.离子键 B.极性键 C.配位键 D.氢键 E.范德华力
②根据价层电子对互斥理论,预测
 的空间构型为
的空间构型为 的等电子体的化学符号
的等电子体的化学符号(4)在NaCl晶体中,Na+位于Cl-所围成的
(5)Na+半径与Cl-半径的比值是
 =1. 414)。
=1. 414)。
(1)Cr的外围电子排布图为
(2)SO2分子的空间构型为
(3)SCN的电子式为
(4)四种分子:①CH4、②SO3、③H2O、④NH3,键角由大到小的排列顺序是
(5)NH3分子可以与H+ 结合生成NH4+,这个过程发生改变的是
a. 微粒的空间构型 b. N原子的杂化类型 c. H-N-H的键角 d. 微粒的电子数
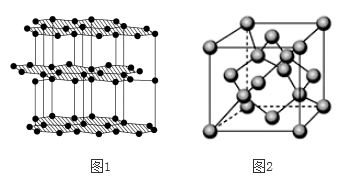
(6)由碳元素形成的某种单质的片状和层状结构如图1所示,由碳元素形成的某种晶体的晶胞结构如图2所示,试回答:
①在图1中,碳原子所形成的六元环数、C原子数、C-C键数之比为
②在图2中,已知阿伏伽德罗常数为NA,晶体密度为ρ g/cm3,则该晶体的棱长为
(1)B原子核外电子排布式为
(2)A与E化合时原子间以
(3)写出A、C的单质直接化合形成的化合物与E单质反应的离子方程式为
(4)A与B形成化合物时,中心原子采取

(1)写出“酸浸”时,杂质Fe3O4与稀硫酸反应的化学方程式:
(2)“氧化”时除了使用MnO2外,还可以使用的一种试剂为
(3)简述加入MnCO3“除铁”的原理:
(4)“沉铜”时,若溶液中c(Mn2+)=2.8mol·L-1,加入Na2S固体,使溶液中Cu2+完全沉淀,即溶液中c(Cu2+)=1.0×10-5mol·L-1,此时是否有MnS沉淀生成?请通过计算判断:
(5)“沉锰”时,发生反应的离子方程式为
(6)为确定所得硫酸锰晶体中含有的结晶水,称取纯化后的MnSO4·xH2O晶体8.45g,加热至完全脱去结晶水,固体减重0.9g,则该硫酸锰晶体的化学式为
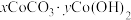 是制备高纯钴系列产品的中间物料,以高钴渣[主要成分为
是制备高纯钴系列产品的中间物料,以高钴渣[主要成分为 ,含
,含 以及
以及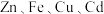 (镉)等的化合物]为原料回收
(镉)等的化合物]为原料回收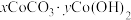 并利用副产物制备绿矾的工艺流程如下:
并利用副产物制备绿矾的工艺流程如下:
回答下列问题:
(1)“控电位浸出”时
 与稀硫酸反应转化为
与稀硫酸反应转化为 ,同时有气体物质生成,写出该反应的化学方程式:
,同时有气体物质生成,写出该反应的化学方程式: 的关系如图甲所示,下列条件能实现“控电位浸出”时发生目标反应的是
的关系如图甲所示,下列条件能实现“控电位浸出”时发生目标反应的是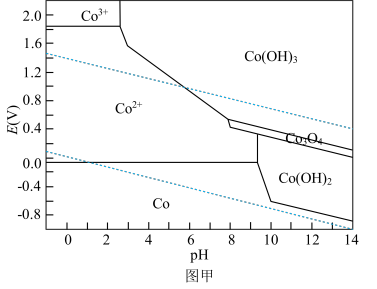
A.
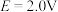
 B.
B.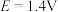

C.
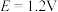
 D.
D.

(2)有关金属离子沉淀的相关
 见下表:
见下表:离子 |
|
|
|
|
|
开始沉淀时的 | 6.2 | 5.3 | 2.1 | 7.1 | 7.2 |
沉淀完全时的 | 8.2 | 6.7 | 3.2 | 9.3 | 9.4 |
 的理论范围是
的理论范围是 为
为(3)一定条件下,试剂B的用量对锌钴分离的影响如图乙所示。
 的用量在
的用量在 时效果最好,理由是
时效果最好,理由是
(4)取所得产品
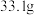 (忽略杂质的影响),在隔绝空气条件下高温充分煅烧,冷却后剩余固体的质量为
(忽略杂质的影响),在隔绝空气条件下高温充分煅烧,冷却后剩余固体的质量为 ,则产品
,则产品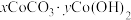 中
中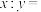
 用途广泛,如用于合成高品质电极材料锰酸锂、制造磁性材料锰锌铁氧体、制备汽车用温度传感器的热敏电阻等。以软锰矿为原料制备
用途广泛,如用于合成高品质电极材料锰酸锂、制造磁性材料锰锌铁氧体、制备汽车用温度传感器的热敏电阻等。以软锰矿为原料制备 的工艺流程如下所示。
的工艺流程如下所示。
已知:①浸出液
 中含有
中含有 、
、 、
、 等杂质。
等杂质。②常温时,一些物质的
 如下表所示。
如下表所示。| 物质 |  |  |  |  |  |  |
 |  |  | 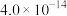 |  |  |  |
回答下列问题:
(1)基态锰原子中未成对电子数为
 发生反应的化学方程式:
发生反应的化学方程式:(2)“调节
 ”时,常温下,若使
”时,常温下,若使 、
、 沉淀完全(浓度不大于
沉淀完全(浓度不大于 ),则应调
),则应调 至少为
至少为
(3)P204是一种有机酸性萃取剂,用
 表示,萃取方程式可简写为
表示,萃取方程式可简写为 。当其他条件相同时,若按照不同相比(P204与滤液体积比)进行“萃取”,溶液中美、锰元素的萃取率记录如下。
。当其他条件相同时,若按照不同相比(P204与滤液体积比)进行“萃取”,溶液中美、锰元素的萃取率记录如下。| 相比 | 镁萃取率/% | 锰萃取率/% |
 | 35.19 | 3.43 |
 | 58.28 | 6.25 |
 | 72.29 | 13.03 |
 | 83.67 | 17.40 |
 | 90.17 | 23.97 |
根据流程及数据,判断“萃取”时最佳相比是
 并进行后续操作的目的为
并进行后续操作的目的为(4)此流程中能循环利用的试剂是
(5)工业上也可通过电解
 和硫酸的混合溶液先制得
和硫酸的混合溶液先制得 ,再通过
,再通过 还原得到
还原得到 。电解时阳极的电极反应式为
。电解时阳极的电极反应式为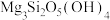 、
、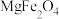 ,还有Ni、Co、Mn的氧化物]为原料提取有价金属(Ni、Co、Mn)的工艺流程如下图所示:
,还有Ni、Co、Mn的氧化物]为原料提取有价金属(Ni、Co、Mn)的工艺流程如下图所示: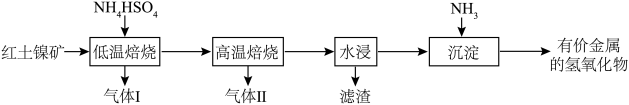
已知:①“低温培烧”前,控制焙烧温度为300℃,反应生成
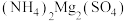 、
、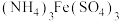 、有价金属的硫酸盐和二氧化硅;
、有价金属的硫酸盐和二氧化硅;②焙烧时,温度升高会使部分硫酸盐分解生成金属氧化物、氨气和三氧化硫,金属氧化物不溶于水,导致金属的浸出率降低;
③常温下,一些难溶电解质的溶度积常数如下表:
| 难溶电解质 |  |  |  |  |
 | 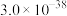 | 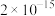 | 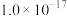 | 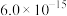 |
(1)“低温烙烧”前,粉碎矿石的目的是
(2)过程中不能省略“低温焙烧”而直接用硫酸氢铵进行“高温焙烧”的原因是

(3)“水浸”时,由题给信息和图1的推测可知滤渣的主要成分为
 、
、 和
和(4)“沉淀”时,发生反应的离子方程式为
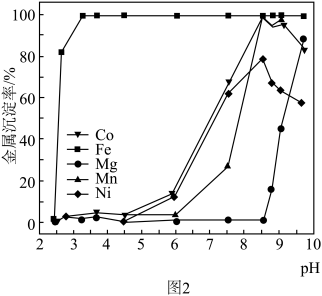
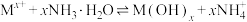 (M为有价金属)常温下,不同pH值下各金属的沉淀率变化曲线如图2所示,通入氨气至溶液的pH为3.5时,得到
(M为有价金属)常温下,不同pH值下各金属的沉淀率变化曲线如图2所示,通入氨气至溶液的pH为3.5时,得到 、
、 、
、 的共沉淀物,判断
的共沉淀物,判断
 沉淀时反应的平衡常数
沉淀时反应的平衡常数
 时,沉淀完全;
时,沉淀完全; 的电离平衡常数
的电离平衡常数 )。
)。
(5)实验过程中产生的气体1可在
 、
、 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | 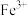 | 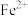 | 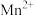 | 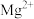 |
| 开始沉淀pH | 2.10 | 7.45 | 9.27 | 9.60 |
| 完全沉淀pH | 3.20 | 8.95 | 10.87 | 11.13 |
回答以下问题:
(1)
 中阴离子的中心原子杂化类型为
中阴离子的中心原子杂化类型为(2)提高“反应I”速率可采取的措施是
(3)“反应II”中硫铁矿(
 )的作用为
)的作用为(4)“反应III”的离子方程式为
(5)“调pH”步骤中,应调节pH不低于
(6)取
 产品,溶于适量水中,加硫酸酸化,用过量
产品,溶于适量水中,加硫酸酸化,用过量 (难溶于水)将其完全氧化为
(难溶于水)将其完全氧化为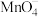 ,过滤,洗涤,洗涤液并入滤液后,加入
,过滤,洗涤,洗涤液并入滤液后,加入 固体,充分反应后,用
固体,充分反应后,用 溶液滴定,最终用去20.00mL,计算样品中
溶液滴定,最终用去20.00mL,计算样品中 的质量分数是
的质量分数是 、
、 等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示:
等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示:
 时:①
时:①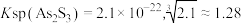 ;
;②将NH3通入H3PO4溶液中,当pH=3.8~4.5时生成NH4H2PO4,pH=8.0~8.2时生成(NH4)2HPO4。
回答下列问题:
(1)“滤渣1”中含硫化合物的化学式为
(2)“滤渣2”的主要成分有
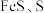 及
及 ,其中生成
,其中生成 的离子方程式为
的离子方程式为 下,当
下,当 沉淀完全时,
沉淀完全时, 至少为
至少为 [当
[当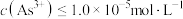 时认为沉淀完全]。
时认为沉淀完全]。(3)“氨化”的目的之一是通入NH3调节溶液的pH,当溶液pH为4.3时H3PO4转化为
(4)“脱镁”的目的是生成MgF2沉淀除去Mg2+。若将流程中“氨化”与“脱镁”交换,Mg2+沉淀不完全,原因是
(5)“结晶”后得到
 晶体,“煅烧”时生成
晶体,“煅烧”时生成 和
和 等物质,其反应的化学方程式为
等物质,其反应的化学方程式为 键角:
键角: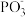
 (选填“
(选填“ ”“
”“ ”或“
”或“ ”),其原因是
”),其原因是




