A、B、C、D均为短周期元素。A、B可形成两种液态化合物甲和乙,其最简式分别为BA和B2A。A与D可形成气态化合物DA、DA2。B与D可形成一种极易溶于水的碱性气体X。B与C可形成极易溶于水的酸性气体Y。Y溶于水能完全电离。已知X分子与乙分子中的电子数相等,Y分子与甲分子中的电子数相等。请回答:
(1)甲的电子式为___________。
(2)常温下,aL pH为2的Y溶液与bL pH为12的氢氧化钠溶液混合后,所得溶液pH=3,则a:b=___________。
(3)X溶于水后发生电离,写出电离方程式____________,已知X在液态时和水一样,可发生微弱的电离,产生两种含相同电子数的粒子。请写出它的电离方程式:___________。
(4)X与甲在一定条件下可发生反应,生成无污染的产物,写出反应的化学方程式_________。
(1)甲的电子式为___________。
(2)常温下,aL pH为2的Y溶液与bL pH为12的氢氧化钠溶液混合后,所得溶液pH=3,则a:b=___________。
(3)X溶于水后发生电离,写出电离方程式____________,已知X在液态时和水一样,可发生微弱的电离,产生两种含相同电子数的粒子。请写出它的电离方程式:___________。
(4)X与甲在一定条件下可发生反应,生成无污染的产物,写出反应的化学方程式_________。
更新时间:2016/12/09 16:57:31
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】为探究某固体化合物X(仅含两种元素)的组成和性质。设计并完成如下实验。已知无色气体B能形成酸雨。请回答:
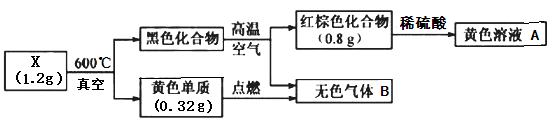
(1)红棕色化合物的化学式_______ 。
(2)将无色气体B通入黄色溶液A中,发现溶液变成浅绿色。请用离子方程式表示该反应_______ 。
(3)X的化学式是_______ 。

(1)红棕色化合物的化学式
(2)将无色气体B通入黄色溶液A中,发现溶液变成浅绿色。请用离子方程式表示该反应
(3)X的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知A是一种不溶于水的固体非金属氧化物,根据图中的转化关系,回答:
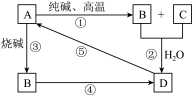
(1)A是______ ,B是_____ ,D是_____ 。
(2)写化学方程式:
①_________ ;
⑤_________ 。
(3)写离子方程式:
②__________ ;
③________ ;
④________ 。

(1)A是
(2)写化学方程式:
①
⑤
(3)写离子方程式:
②
③
④
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
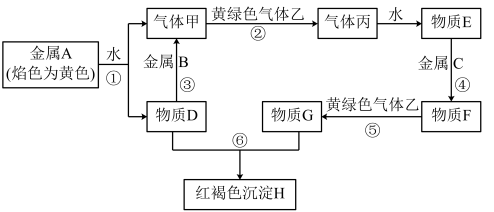
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:甲:______ 、乙:_____ 、F:_____ 、H________ ;
(2)金属B既能与强酸又能与强碱反应,该金属B是:_________ (填化学式),金属C的最高价阳离子遇KSCN溶液呈血红色,该金属C是:_______ (填化学式);
(3)反应③的化学方程式____________ ;
(4)反应⑤的离子方程式____________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:甲:
(2)金属B既能与强酸又能与强碱反应,该金属B是:
(3)反应③的化学方程式
(4)反应⑤的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】化学与社会、生产、生活息息相关,请回答下列问题:
(1)用热的纯碱水刷洗餐具上的油污,试解释原因___________ (用必要的语言和离子方程式作答)。
(2)已知:①2Zn(s)+O2(g)=2ZnO(s) ΔH=-702.2 kJ·mol-1
②2Hg(l)+O2(g)=2HgO(s) ΔH=-181.4 kJ·mol-1。
则Zn(s)+HgO(s)=ZnO(s)+Hg(l) ΔH=___________ kJ·mol-1
(3)常温下,V1 mL pH=1的盐酸与V2 mL 0.05 mol·L-1Ba(OH)2溶液混合,所得混合溶液的pH=2,则V1︰V2等于___________ (忽略混合前后溶液体积变化)。
(4)某反应过程中的能量变化如下图所示:
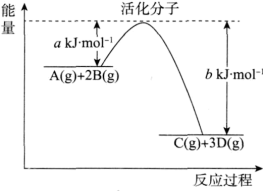
①该反应的ΔH___________ (填“>”或“<”)0。
②该反应的热化学方程式为___________ 。
③加入催化剂,b___________ (填“增大”“减小”或“不变”,下同),ΔH______ 。
(1)用热的纯碱水刷洗餐具上的油污,试解释原因
(2)已知:①2Zn(s)+O2(g)=2ZnO(s) ΔH=-702.2 kJ·mol-1
②2Hg(l)+O2(g)=2HgO(s) ΔH=-181.4 kJ·mol-1。
则Zn(s)+HgO(s)=ZnO(s)+Hg(l) ΔH=
(3)常温下,V1 mL pH=1的盐酸与V2 mL 0.05 mol·L-1Ba(OH)2溶液混合,所得混合溶液的pH=2,则V1︰V2等于
(4)某反应过程中的能量变化如下图所示:

①该反应的ΔH
②该反应的热化学方程式为
③加入催化剂,b
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有A、B、C、D四种强电解质,它们在水中电离产生系列离子(每种物质只含一种阴离子且互不重复)。
已知:①A、C溶液的pH均大于7;
②一定浓度的A、B的溶液中水的电离程度可以相同;
③C溶液和D溶液相遇时只生成白色沉淀;
④仅B溶液和C溶液相遇时只生成刺激性气味的气体;
⑤A溶液和D溶液混合时无现象。
(1)写出A物质中所含化学键的类型____________ 。
(2)写出C和D反应的离子方程式______________ 。
(3)25℃时,0.1 mol•L-1B溶液的pH=a,则B溶液中c(H+)-c(NH3•H2O)=_________ (用含有a的关系式表示)。
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是____________ 。
(5)25℃时,在一定体积的0.01 mol•L-1的C溶液中,加入一定体积的0.01 mol•L-1的盐酸,混合溶液的pH=12,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是_________ 。
| 阳离子 | Na+、Ba2+、 |
| 阴离子 | CH3COO-、OH-、Cl-、 |
②一定浓度的A、B的溶液中水的电离程度可以相同;
③C溶液和D溶液相遇时只生成白色沉淀;
④仅B溶液和C溶液相遇时只生成刺激性气味的气体;
⑤A溶液和D溶液混合时无现象。
(1)写出A物质中所含化学键的类型
(2)写出C和D反应的离子方程式
(3)25℃时,0.1 mol•L-1B溶液的pH=a,则B溶液中c(H+)-c(NH3•H2O)=
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是
(5)25℃时,在一定体积的0.01 mol•L-1的C溶液中,加入一定体积的0.01 mol•L-1的盐酸,混合溶液的pH=12,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】已知水的电离平衡曲线如图示,试回答下列问题:
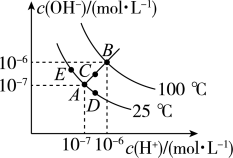
(1)图中五点Kw间的关系是_________ 。
(2)若从A点到D点,可采用的措施是_________ 。
A 升温 B 加入少量的盐酸 C 加入少量的NH4Cl
(3)B对应温度下,将pH=11的苛性钠溶液V1 L与0.05mol/L的稀硫酸V2L 混合(设混合前后溶液的体积不变),所得混合溶液的pH=2,则 V1∶V2=__________ 。
(4)常温下,将V mL、0.1000mol·L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L-1醋酸溶液中充分反应。如果溶液pH=7,此时V的取值___________ 20.00(填“>”“<”或“=”)(忽略溶液体积的变化)。而溶液 中c(Na+)、c(CH3COO-)、c(H+)、c(OH-)的大小关系为___________ 。
(5)在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=____________ mol·L-1。(Ksp[Cu(OH)2]=2.2×10-20)

(1)图中五点Kw间的关系是
(2)若从A点到D点,可采用的措施是
A 升温 B 加入少量的盐酸 C 加入少量的NH4Cl
(3)B对应温度下,将pH=11的苛性钠溶液V1 L与0.05mol/L的稀硫酸V2L 混合(设混合前后溶液的体积不变),所得混合溶液的pH=2,则 V1∶V2=
(4)常温下,将V mL、0.1000mol·L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L-1醋酸溶液中充分反应。如果溶液pH=7,此时V的取值
(5)在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】H2O2是重要的化学试剂,在实验室和生产实际中应用广泛。
(1)写出H2O2的结构式:_______ ,H2O2在MnO2催化下分解的化学方程式:_______ 。
(2)①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:_______
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是_______ 。
③你认为H2O2被称为绿色氧化剂的主要原因是_______ 。
(3)H2O2还有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:_______
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在_______ (填“酸式”或“碱式”)滴定管中,判断到达滴定终点的现象是_______ 。
(4)H2O2是一种二元弱酸,写出其第一步电离的方程式:_______ ,它与过量的Ba(OH)2反应的化学方程式为_______ 。
(1)写出H2O2的结构式:
(2)①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是
③你认为H2O2被称为绿色氧化剂的主要原因是
(3)H2O2还有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在
(4)H2O2是一种二元弱酸,写出其第一步电离的方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】研究硫元素及其化合物的性质具有重要意义。
(1)氢硫酸溶液中,H2S电离方程式为_______ 。
(2)25℃时,在0.10 mol·L-1 H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如下图(忽略溶液体积的变化、H2S的挥发)。

①T=25℃、pH=11时,溶液中的c(H2S)+c(HS–)═_______ mol·L-1
②25℃时,某溶液含0.020 mol·L-1 Mn2+、0.10 mol·L-1H2S,当溶液pH═_______ 时,Mn2+开始沉淀;
③向含有Cu2+的废水中,加入足量MnS固体除去Cu2+,平衡时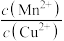 ═
═_______ [已知:Ksp(MnS)=2.8×10-13 ,Ksp(CuS)=1.3×10-36 ]
(3)25℃时,两种酸的电离平衡常数如下表:
①25℃时,酸性强弱:H2SO3 _______ H2CO3(填“>”或“<”)。
②0.10 mol·L-1Na2SO3溶液中离子浓度由大到小的顺序为_______ 。
③H2SO3溶液和NaHCO3溶液反应的离子方程式为_______ 。
(1)氢硫酸溶液中,H2S电离方程式为
(2)25℃时,在0.10 mol·L-1 H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如下图(忽略溶液体积的变化、H2S的挥发)。

①T=25℃、pH=11时,溶液中的c(H2S)+c(HS–)═
②25℃时,某溶液含0.020 mol·L-1 Mn2+、0.10 mol·L-1H2S,当溶液pH═
③向含有Cu2+的废水中,加入足量MnS固体除去Cu2+,平衡时
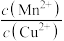 ═
═(3)25℃时,两种酸的电离平衡常数如下表:
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
②0.10 mol·L-1Na2SO3溶液中离子浓度由大到小的顺序为
③H2SO3溶液和NaHCO3溶液反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】连二次硝酸(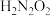 )是一种二元酸,可用于制取
)是一种二元酸,可用于制取 气体。已知
气体。已知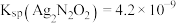 ,
,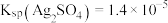 。
。
(1)连二次硝酸中氮元素的化合价为_______ 。
(2)常温下,用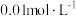 的
的 溶液滴定
溶液滴定
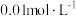
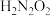 溶液,测得溶液
溶液,测得溶液 与
与 溶液体积的关系如图所示。
溶液体积的关系如图所示。
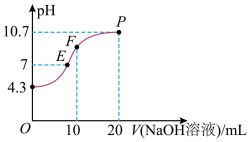
①写出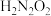 在水溶液中的电离方程式:
在水溶液中的电离方程式:_______ 。
②P点时溶液中各离子浓度由大到小的顺序为_______ 。
③F点时溶液中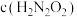
_______ (填“<”“>”或“=”) 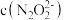 。
。
④E点时溶液中
_______ (填“<”“>”或“=”) 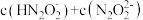 。
。
(3)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中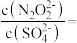
_______ 。
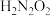 )是一种二元酸,可用于制取
)是一种二元酸,可用于制取 气体。已知
气体。已知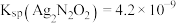 ,
,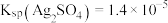 。
。(1)连二次硝酸中氮元素的化合价为
(2)常温下,用
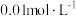 的
的 溶液滴定
溶液滴定
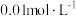
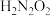 溶液,测得溶液
溶液,测得溶液 与
与 溶液体积的关系如图所示。
溶液体积的关系如图所示。
①写出
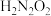 在水溶液中的电离方程式:
在水溶液中的电离方程式:②P点时溶液中各离子浓度由大到小的顺序为
③F点时溶液中
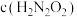
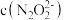 。
。④E点时溶液中

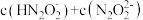 。
。(3)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中
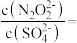
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E、F、G是元素周期表前四周期中常见的七种元素,其原子序数依次增大,其相关信息如下表:
(1)①下列物质的分子与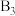 分子的空间结构最相似的是
分子的空间结构最相似的是___________ (填序号)。
A. B.
B. C.
C. D.
D.
②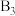 分子是否为极性分子?
分子是否为极性分子?___________ (填“是”或“否”)。
(2)根据等电子体原理,则1mol AB中含有共用电子对的数目为___________ ;
(3)工业上常通过在空气中煅烧G的低价含硫矿获得G单质,请写出该反应的方程式___________ ;若往含有 的溶液中加过量氢氧化钠溶液,可生成
的溶液中加过量氢氧化钠溶液,可生成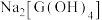 溶液,
溶液,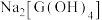 具有的化学键类型有
具有的化学键类型有___________ 。
A.离子键 B.极性共价键 C.非极性共价键 D.配位键
(4)表中F元素与Mn、Fe在工业上统称“黑色金属”,Mn、Fe均为第4周期过渡金属元素,两元素的部分电离能数据列于下表:
F元素的单质中存在化学键为___________ ;请写出基态 的价电子轨道排布图
的价电子轨道排布图___________ ,比较两元素的 、
、 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,请解释原因
再失去1个电子难,请解释原因___________ 。
| 元素 | 相关信息 |
| A | A的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| B | B的某一种单质是大气污染物监测物之一 |
| C | C在组成化合物时没有正价 |
| D | D常温常压下,D单质是淡黄色固体,常在火山口附近沉积 |
| E | E和D同周期,E的电负性大于D |
| F | F的基态原子核外有6个原子轨道处于半充满状态 |
| G | G能形成红色的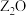 和黑色的ZO两种氧化物。 和黑色的ZO两种氧化物。 |
 分子的空间结构最相似的是
分子的空间结构最相似的是A.
 B.
B. C.
C. D.
D.
②
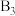 分子是否为极性分子?
分子是否为极性分子?(2)根据等电子体原理,则1mol AB中含有共用电子对的数目为
(3)工业上常通过在空气中煅烧G的低价含硫矿获得G单质,请写出该反应的方程式
 的溶液中加过量氢氧化钠溶液,可生成
的溶液中加过量氢氧化钠溶液,可生成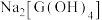 溶液,
溶液,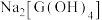 具有的化学键类型有
具有的化学键类型有A.离子键 B.极性共价键 C.非极性共价键 D.配位键
(4)表中F元素与Mn、Fe在工业上统称“黑色金属”,Mn、Fe均为第4周期过渡金属元素,两元素的部分电离能数据列于下表:
| 元素 | Mn | Fe | |
电离能/ |  | 717 | 759 |
 | 1509 | 1561 | |
 | 4048 | 2957 | |
 的价电子轨道排布图
的价电子轨道排布图 、
、 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,请解释原因
再失去1个电子难,请解释原因
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、B、C、D、E、M是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是nsnnp2n;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。M是第四周期元素中未成对电子数最多的元素。
请用元素符号完成下列空白:
(1)B、C、D、E四种元素中,简单离子半径最小的离子符号是___________ 。
(2)BC 的中心原子的价层电子对数为
的中心原子的价层电子对数为___________ ,VSEPR模型名称为___________ 。
(3)下表是A~M元素中某种元素的部分电离能,由此可判断该元素是___________ 。根据对角线规则,在短周期元素中,该元素的一些化学性质与元素___________ 的相似。
(4)某含M、Ca(钙)、O(氧)的化合物的立方晶胞如图所示。___________ 区,其基态原子的价层电子排布式为___________ 。
②该化合物的化学式是___________ 。
③Ca和M的最近距离为acm,晶体密度为ρg·cm-3。则阿伏加德罗常数(NA)为___________ mol-1(用代数式表示)。
请用元素符号完成下列空白:
(1)B、C、D、E四种元素中,简单离子半径最小的离子符号是
(2)BC
 的中心原子的价层电子对数为
的中心原子的价层电子对数为(3)下表是A~M元素中某种元素的部分电离能,由此可判断该元素是
| 某种元素 | 电离能I(kJ·mol-1) | ||||
| I1 | I2 | I3 | I4 | I5 | |
| 578 | 1817 | 2745 | 11575 | 14830 | |
(4)某含M、Ca(钙)、O(氧)的化合物的立方晶胞如图所示。

②该化合物的化学式是
③Ca和M的最近距离为acm,晶体密度为ρg·cm-3。则阿伏加德罗常数(NA)为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的最外层电子数是次外层电子数2倍,B是短周期中金属性最强的元素,C是同周期中阳离子半径最小的元素,D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,E的最外层电子数与内层电子数之比为3﹕5。请回答:
(1)D的元素符号为________ 。
(2)F在元素周期表中的位置_________ 。
(3)用电子式表示由元素B和F组成的化合物的形成过程:__________ 。
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关的化学方程式为________ 、_______ 。
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2。该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为_______________ 。
(1)D的元素符号为
(2)F在元素周期表中的位置
(3)用电子式表示由元素B和F组成的化合物的形成过程:
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关的化学方程式为
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2。该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为
您最近一年使用:0次



