下列说法正确的是
| A.根据溶液中有CH3COOH、CH3COO-和H+即可证明CH3COOH达到电离平衡状态 |
| B.根据溶液中CH3COO-和H+的物质的量浓度相等即可证明CH3COOH达到电离平衡状态 |
| C.当NH3·H2O达到电离平衡时,溶液中NH3·H2O、NH4+和OH-的浓度相等 |
| D.H2CO3是分步电离的,电离程度依次减弱 |
15-16高二下·内蒙古巴彦淖尔·期中 查看更多[11]
2015-2016学年内蒙古杭锦后旗奋斗中学高二下期中化学卷(已下线)同步君 选修4 第3章 第1节 弱电解质的电离(已下线)【百强校】2016-2017学年浙江省温州中学高二上期中化学卷(带解析)高中化学人教版 选修四 第三章 水溶液中的离子反应 第一节 弱电解质的电离 弱电解质的电离(已下线)2019年10月2日 《每日一题》选修4—— 电离平衡的特征及建立浙江省丽水四校2019-2020学年高三10月联考化学试题辽宁省铁岭市开原市第二高级中学2020-2021学年高二上学期期初考试化学试题广西贺州市平桂管理区公会中学2021-2022学年上学期高二第二次月考化学(理)试题山西省太原市英才学校2021-2022学年高二上学期第二次月考化学试题(已下线)专题卷12 强弱电解质分析比较-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)3.1.1强电解质和弱电解质 弱电解质的电离平衡 课前
更新时间:2016-12-09 17:33:01
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是
| A.二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质 |
| B.氯化钠溶液在电流作用下完全电离成钠离子和氯离子 |
| C.硫酸钡难溶于水,但硫酸钡属于强电解质 |
| D.弱电解质的电离平衡常数与浓度、温度等条件有关 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法中,正确的是( )
| A.相同温度下, 0.1mol/L 氨水中NH4+的浓度为0.1mol/L。 |
| B.冰醋酸是弱电解质,液态时能导电。 |
| C.盐酸中加入固体NaCl,因Cl-浓度增大,所以溶液酸性减弱。 |
| D.强电解质溶液的导电能力不一定比弱电解质强。 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】用0.1000 的NaOH溶液滴定20.00mL未知浓度的二元酸H2A溶液。溶液pH、微粒分布系数
的NaOH溶液滴定20.00mL未知浓度的二元酸H2A溶液。溶液pH、微粒分布系数 [比如
[比如 的分布系数:
的分布系数: ]随滴加NaOH溶液体积VNaOH的变化关系如图所示。下列叙述正确的是
]随滴加NaOH溶液体积VNaOH的变化关系如图所示。下列叙述正确的是

 的NaOH溶液滴定20.00mL未知浓度的二元酸H2A溶液。溶液pH、微粒分布系数
的NaOH溶液滴定20.00mL未知浓度的二元酸H2A溶液。溶液pH、微粒分布系数 [比如
[比如 的分布系数:
的分布系数: ]随滴加NaOH溶液体积VNaOH的变化关系如图所示。下列叙述正确的是
]随滴加NaOH溶液体积VNaOH的变化关系如图所示。下列叙述正确的是
A.H2A的第一步电离方程式: |
B.H2A溶液的浓度为0.2000 |
C. 的电离常数为 的电离常数为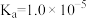 |
D.溶液滴定过程中: |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】相同温度、相同体积、c(H+)相同的盐酸和醋酸溶液分别跟足量的镁完全反应,下列说法正确的是
| A.醋酸溶液产生的氢气较多 | B.盐酸产生的氢气较多 |
| C.盐酸和醋酸的物质的量浓度相同 | D.开始时醋酸溶液反应更快 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】依据下列实验现象,不能得出对应结论的是
| 实验 | 现象 | 结论 | |
| A | 室温下测0.1 mol·L-1醋酸pH | pH≈3.3 | 醋酸是弱酸 |
| B | 向2 mL 0.1 mol·L-1NaOH溶液中 i.滴加几滴同浓度的MgSO4溶液 ii.再滴加几滴同浓度FeCl3溶液 | i.产生白色沉淀 ii.产生红褐色沉淀 | 溶解度:Fe(OH)3<Mg(OH)2 |
| C | 常温下,将CO2通入苯酚钠溶液中 | 溶液变浑浊 | 酸性:碳酸>苯酚 |
| D | 将少量溴乙烷与NaOH溶液共热,冷却、HNO3酸化后,滴加AgNO3溶液 | 淡黄色沉淀 | 证明含有溴元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次





