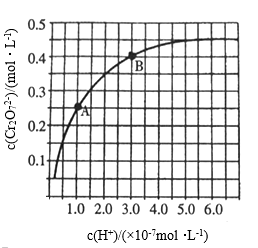
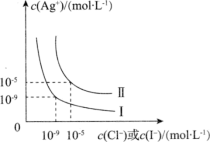
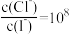化学平衡常数(K)、弱酸的电离平衡常数(Ka)、难溶物的溶度积常数(KSP)是判断物质性质或变化的重要的平衡常数.下列关于这些常数的说法中,正确的是
| A.平衡常数的大小与温度、浓度、压强、催化剂等有关 |
| B.KSP(AgCl)>KSP(AgI),由此可以判断AgCl(s)+I-=AgI(s)+Cl-(aq)能够发生 |
| C.当温度升高时,弱酸的电离常数Ka变小 |
| D.Ka(HCN)<Ka(CH3COOH),说明相同物质的量浓度时,氢氰酸的酸性比醋酸强 |
11-12高三·广东·阶段练习 查看更多[8]
浙江省杭州东方中学2023-2024学年高二上学期期中考试化学试题(已下线)专题八 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第八章 能力提升检测卷-2021年高考化学一轮复习讲练测夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——弱电解质的电离及影响因素 (强化练习)2016-2017学年吉林省实验中学高二上学期期末化学试卷(已下线)2014届高考化学二轮专题冲刺第7讲 水溶液中的离子平衡练习卷(已下线)2014高考化学二轮复习限时集训 专题8电解质溶液练习卷B(已下线)2013届广东省六校高三第一次联考化学试卷
更新时间:2017-02-17 14:59:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作现象及解释或结论均正确的是
| 选项 | 实验操作及现象 | 解释或结论 |
| A | 常温下,相同体积相同浓度的盐酸、醋酸与大小相同的镁片反应,产生气泡的速率:前者快 | 得出结论:盐酸是强电解质,醋酸是弱电解质 |
| B | 常温下,向浓度、体积都相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞,变红,前者红色更深 红色更深 | 结合质子的能力:CO >HCO >HCO |
| C | 向FeCl3和KSCN混合溶液中,加入少量KCl的固体,溶液颜色变浅 | FeCl3+3KSCN Fe(SCN)3+3KCl平衡向逆反应方向移动 Fe(SCN)3+3KCl平衡向逆反应方向移动 |
| D | 将0.1mol/L的AgNO3加入到0.1mol/L的NaCl溶液中至不再产生白色沉淀,再向悬浊液中加入0.1mol/L的KI溶液,有黄色沉淀产生 | 证明:Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列反应的离子方程式不正确的是
A. 气体通入足量NaClO溶液: 气体通入足量NaClO溶液: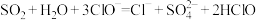 |
B.明矾溶液中加入过量NaOH溶液: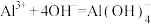 |
C.向血红色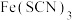 溶液加入过量铁粉: 溶液加入过量铁粉: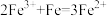 |
D.向硫化锌悬浊液滴加硫酸铜溶液; |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列用于解释事实的方程式书写不正确 的是
A.用饱和Na2CO3溶液处理锅炉水垢中的CaSO4:Ca2++CO =CaCO3 =CaCO3 |
B.用明矾[KAl(SO4)2·12H2O]作净水剂:Al3++3H2O Al(OH)3+3H+ Al(OH)3+3H+ |
C.向氢氧化镁悬浊液中滴入酚酞溶液,溶液变红:Mg(OH)2(s) Mg2+(aq)+2OH−(aq) Mg2+(aq)+2OH−(aq) |
D.将纯水加热至较高温度,水的pH变小:H2O H++OH− ΔH>0 H++OH− ΔH>0 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知常温下反应①NH3+H+ NH
NH (平衡常数为K1),②Ag++Cl-
(平衡常数为K1),②Ag++Cl- AgCl(平衡常数为K2),③Ag++2NH3
AgCl(平衡常数为K2),③Ag++2NH3 Ag(NH3)
Ag(NH3) (平衡常数为K3)。
(平衡常数为K3)。
①、②、③的平衡常数关系为K1>K3>K2,据此所做的以下推测合理的是
 NH
NH (平衡常数为K1),②Ag++Cl-
(平衡常数为K1),②Ag++Cl- AgCl(平衡常数为K2),③Ag++2NH3
AgCl(平衡常数为K2),③Ag++2NH3 Ag(NH3)
Ag(NH3) (平衡常数为K3)。
(平衡常数为K3)。①、②、③的平衡常数关系为K1>K3>K2,据此所做的以下推测合理的是
| A.氯化银不溶于氨水 |
| B.银氨溶液中加入少量氯化钠有白色沉淀 |
| C.银氨溶液中加入盐酸有白色沉淀 |
| D.银氨溶液可在酸性条件下稳定存在 |
您最近半年使用:0次

 +2H+
+2H+ +H2O,25℃时,调节初始浓度为1.0mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(
+H2O,25℃时,调节初始浓度为1.0mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(