已知:2 +2H+
+2H+
 +H2O,25℃时,调节初始浓度为1.0mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(
+H2O,25℃时,调节初始浓度为1.0mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c( )和c(H+),获得如图曲线。
)和c(H+),获得如图曲线。
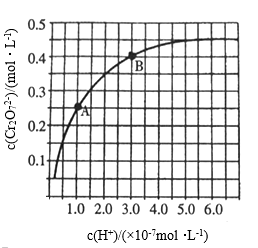
下列说法不正确的是( )
 +2H+
+2H+
 +H2O,25℃时,调节初始浓度为1.0mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(
+H2O,25℃时,调节初始浓度为1.0mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c( )和c(H+),获得如图曲线。
)和c(H+),获得如图曲线。
下列说法不正确的是( )
A.平衡时,pH越小,c( )越大 )越大 |
B.A、B两点c( )之比为5:2 )之比为5:2 |
C.B点 的平衡转化率为40% 的平衡转化率为40% |
D.平衡时,若溶液中c( )=2c( )=2c( ),则c(H+)=1.0×10-7mol·L-1 ),则c(H+)=1.0×10-7mol·L-1 |
更新时间:2020-09-15 16:02:33
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在某温度时,将n mol/L氨水滴入10mL 1.0mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,有关说法正确的是


A.a点Kw=1.0×10﹣14 mol 2 L﹣2 L﹣2 |
| B.水的电离程度:b>c>a>d |
| C.b点:c(NH4+)>c(Cl﹣)>c(H+)>c(OH﹣) |
D.25℃ 时NH3·H2O的电离常数为 mol mol L-1(用n表示) L-1(用n表示) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃, 的
的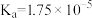 。依次进行如下实验:
。依次进行如下实验:
①取一定量冰醋酸,配制成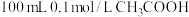 溶液
溶液
②取20 mL①中所配溶液,加入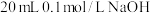 溶液
溶液
③继续滴加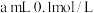 盐酸,至溶液的
盐酸,至溶液的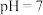
下列说法错误的是
 的
的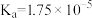 。依次进行如下实验:
。依次进行如下实验:①取一定量冰醋酸,配制成
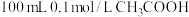 溶液
溶液②取20 mL①中所配溶液,加入
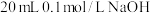 溶液
溶液③继续滴加
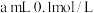 盐酸,至溶液的
盐酸,至溶液的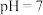
下列说法错误的是
A.水电离的 :①<② :①<② |
B.②中,反应后的溶液: |
C.③中,反应后的溶液: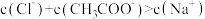 |
D.③中, |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】1922年范斯莱克(Vanslyke)提出用缓冲容量β来描述缓冲溶液缓冲能力大小,β越大,缓冲能力越大。下图是常温下,CH3COOH和CH3COONa组成缓冲溶液的β-pH关系图,其中A、B两条曲线分别对应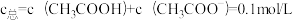 和
和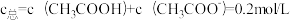 。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是
。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是
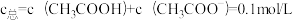 和
和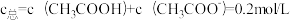 。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是
。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是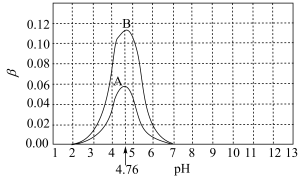
| A.向pH=4.76的上述缓冲溶液中加入少量NaOH溶液,水的电离程度会增大 |
B.A曲线上任意一点的溶液中均存在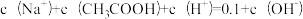 |
| C.B曲线代表的溶液缓冲能力最大时,溶液中c(Na+)>c(CH3COOH) |
D.pH=4时,A、B曲线所代表的溶液中 相等 相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列陈述I与陈述II均正确, 且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | SO2具有氧化性 | 在葡萄酒酿制过程中添加适量SO2 |
| B | 人体需要补充铁单质 | 酱油中加入铁强化剂 |
| C | NaHCO3受热易分解生成CO2气体 | 用纯碱焙制糕点 |
| D | S2-能与Cu2+、Hg2+生成难溶的硫化物沉淀 | 用Na2S处理 含Cu2+、Hg2+的工业废水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,Ksp(FeS)= 6.3×10-18,Ksp(CuS)= 1.3×10-36,下列有关说法中正确的是( )
| A.FeS在水中的沉淀溶解平衡可表示为:FeS(s) = Fe2+ (aq) + S2-(aq) |
| B.饱和CuS溶液中,Cu2+的浓度为1.3×10-36mol·L-1 |
| C.因为H2SO4是强酸,所以反应CuSO4+H2S=CuS↓+H2SO4不能发生 |
| D.除去某溶液中的Cu2+,可以选用FeS作沉淀剂 |
您最近一年使用:0次

 在水溶液中水解:
在水溶液中水解: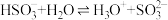
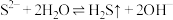

 (aq)+CaSO4(s)
(aq)+CaSO4(s) (aq)
(aq)

