(1)下列物质中,只存在离子键的是______ ,属于共价化合物的是____ ,不存在化学键的是____ 。
①Ar ②CO2 ③Na2O2 ④H2SO4 ⑤NaCl ⑥NH4Cl ⑦CaO
(2)阴离子Xn﹣含N个中子,X的质量数为A,则ag X的氢化物中含质子的物质的量为_________ mol。
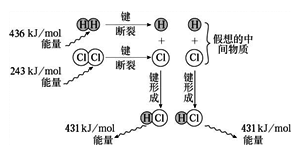
(3)观察如图,计算1molH2与1molCl2反应释放的能量为______ 。若氢气在氯气中燃烧,反应过程中产生苍白色的火焰,该反应中形成2 mol HCl时释放的能量与上述计算的数值相比_______ (填“大”或“小”或“相等”)。

①Ar ②CO2 ③Na2O2 ④H2SO4 ⑤NaCl ⑥NH4Cl ⑦CaO
(2)阴离子Xn﹣含N个中子,X的质量数为A,则ag X的氢化物中含质子的物质的量为
(3)观察如图,计算1molH2与1molCl2反应释放的能量为
更新时间:2017-05-07 21:18:18
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:
(1)SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)=SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol-1
3SiH2Cl2(g)=SiH4(g)+2SiHCl3 (g) ΔH2=−30 kJ·mol-1
则反应4SiHCl3(g)=SiH4(g)+3SiCl4(g)的ΔH=__________ kJ·mol-1。
(2)对于反应2SiHCl3(g)=SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。
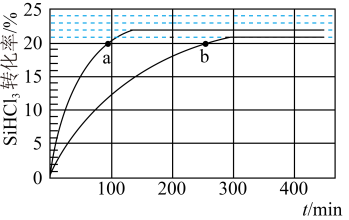
① 343K时反应的平衡转化率α=__________ %。平衡常数表达式__________ 。
②在343K下,要提高SiHCl3转化率,可采取的措施是__________ ;要缩短反应达到平衡的时间,可采取的措施有__________ 、__________ 。
③比较a、b处反应速率大小:va__________ vb(填“大于”“小于”或“等于”)。
(1)SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)=SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol-1
3SiH2Cl2(g)=SiH4(g)+2SiHCl3 (g) ΔH2=−30 kJ·mol-1
则反应4SiHCl3(g)=SiH4(g)+3SiCl4(g)的ΔH=
(2)对于反应2SiHCl3(g)=SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。

① 343K时反应的平衡转化率α=
②在343K下,要提高SiHCl3转化率,可采取的措施是
③比较a、b处反应速率大小:va
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)某化学兴趣小组要完成中和热的测定实验。实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、量筒、温度计、0.5 mol·L-1盐酸、0.55 mol·L-1氢氧化钠溶液。实验尚缺少的玻璃用品是___________ 。若用醋酸代替盐酸做实验,测得的中和热数值___________ (填“偏大”、“偏小”或“无影响”)。
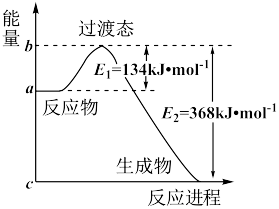
(2)如图是1 mol NO2(g)和1 mol CO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,则E1___________ (填“增大”、“减小”或“不变”,下同),ΔH___________ 。请写出NO2和CO反应的热化学方程式:___________ 。
(3)在25℃、101 kPa时,1 g CH4完全燃烧生成液态水时放出的热量是55.7kJ,则表示甲烷燃烧热的热化学方程式是___________ 。
(4)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5 kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4 kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3=___________ 。
(1)某化学兴趣小组要完成中和热的测定实验。实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、量筒、温度计、0.5 mol·L-1盐酸、0.55 mol·L-1氢氧化钠溶液。实验尚缺少的玻璃用品是
(2)如图是1 mol NO2(g)和1 mol CO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,则E1

(3)在25℃、101 kPa时,1 g CH4完全燃烧生成液态水时放出的热量是55.7kJ,则表示甲烷燃烧热的热化学方程式是
(4)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5 kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4 kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)许多运动会使用的火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O过程中的能量变化图,请在图中的括号内填入“+”或“-”。
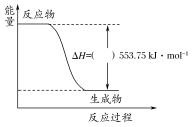
②写出表示丙烷燃烧热的热化学方程式:____________________________________________ 。
(2)2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=﹣99 kJ•mol-1。
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=﹣99 kJ•mol-1。
请回答下列问题:
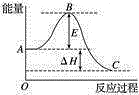
①图中ΔH=______ kJ•mol-1。
②已知单质硫的燃烧热为296 kJ•mol-1,计算由S(s)生成1 mol SO3(g)的ΔH=______ kJ•mol-1。
①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O过程中的能量变化图,请在图中的括号内填入“+”或“-”。

②写出表示丙烷燃烧热的热化学方程式:
(2)2SO2(g)+O2(g)
 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=﹣99 kJ•mol-1。
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=﹣99 kJ•mol-1。请回答下列问题:

①图中ΔH=
②已知单质硫的燃烧热为296 kJ•mol-1,计算由S(s)生成1 mol SO3(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】
(1)写出具有10个电子,两个或两个以上原子核的离子符号:________ ;________ ;________ 。
(2)写出具有18个电子的无机化合物的化学式:________ 、________ 、________ 、________ 。
(3)在(1)(2)题涉及的粒子中,空间结构为正四面体形的有_________ ;为三角锥形的有______ 。
(1)写出具有10个电子,两个或两个以上原子核的离子符号:
(2)写出具有18个电子的无机化合物的化学式:
(3)在(1)(2)题涉及的粒子中,空间结构为正四面体形的有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2020年,嫦娘五号带回1731克月壤样本,完成我国首次地外天体采样,并首次发现新矿石——嫦娥石 。月壤中存在着大量的
。月壤中存在着大量的 ,
, 有望成为未来的清洁能源。
有望成为未来的清洁能源。
(1)有关 说法正确的是_______。
说法正确的是_______。
(2)写出P原子的电子式_______ 。
(3) 属于_______。
属于_______。
(4)已知 为阿伏加德罗常数的值。标准状况下,
为阿伏加德罗常数的值。标准状况下,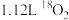 中所含的中子数为_______。
中所含的中子数为_______。
(5)同温同压下,氮气与氧气的体积不同,主要原因是_______。
(6) 的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。
的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。
(7)人造空气(氧气和氮气的混合气)可用于宇航员登月使用。在标准状况下, “人造空气”的质量是
“人造空气”的质量是 。该混合气体的平均相对分子质量为
。该混合气体的平均相对分子质量为_______ ,氧气和氦气的分子数之比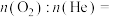
_______ 。
 。月壤中存在着大量的
。月壤中存在着大量的 ,
, 有望成为未来的清洁能源。
有望成为未来的清洁能源。(1)有关
 说法正确的是_______。
说法正确的是_______。| A.质子数为3 | B.与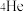 互为同素异形体 互为同素异形体 |
C.与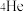 的化学性质相同 的化学性质相同 | D.与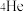 具有相同的电子数 具有相同的电子数 |
(3)
 属于_______。
属于_______。| A.磷酸盐 | B.钙盐 | C.混合物 | D.有机物 |
 为阿伏加德罗常数的值。标准状况下,
为阿伏加德罗常数的值。标准状况下,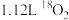 中所含的中子数为_______。
中所含的中子数为_______。A. | B. | C.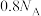 | D. |
| A.气体的分子大小不同 | B.气体的性质不同 |
| C.气体的分子数不同 | D.气体的分子间距不同 |
 的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。
的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。| A.核外电子的质量太小,忽略不计 |
| B.质子和中子的相对原子质量都很接近1 |
| C.氧的其它同位素的丰度太低,忽略不计 |
| D.元素的近似相对原子质量约等于质量数 |
 “人造空气”的质量是
“人造空气”的质量是 。该混合气体的平均相对分子质量为
。该混合气体的平均相对分子质量为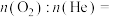
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D、E五种微粒。已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。
请回答:
(1)写出这五种微粒的符号:A_______ ,B_______ ,C_______ ,D______ ,E_______ 。
(2)B微粒的结构示意图________ ,D微粒的结构示意图_________ 。
(3)A的单质与EB溶液反应的离子方程式:_______________ 。
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。
请回答:
(1)写出这五种微粒的符号:A
(2)B微粒的结构示意图
(3)A的单质与EB溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】安全气囊是行车安全的重要设施。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客。为研究安全气囊工作的化学原理,取安全装置中的粉末进行研究。经实验分析,确定该粉末是一种混合物且只含Na、Fe、N、O四种元素。
(1)氧元素在元素周期表中的位置是______________________________________ ,其中三种主族元素的原子半径从大到小的顺序是_____________________________ (用原子符号表示)。
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,写出该化学反应方程式:_______________ , 该盐晶体中含有的化学键类型是__________ 。
(3)水溶性实验表明,安全气囊中固体粉末部分溶解,不溶物为一种红棕色固体,可溶于盐酸,写出反应的离子方程式________________________________________________________ 。
(1)氧元素在元素周期表中的位置是
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,写出该化学反应方程式:
(3)水溶性实验表明,安全气囊中固体粉末部分溶解,不溶物为一种红棕色固体,可溶于盐酸,写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是_____ (填序号,下同);仅发生离子键破坏的是_____ 。
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空),其中只存在非极性键的分子是_____ ;既存在离子键又存在极性键的是_____ 。
(3)写出下列物质的电子式。
①Na2O2_____ 。
②HClO_____ 。
③NH4Cl_____ 。
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空),其中只存在非极性键的分子是
(3)写出下列物质的电子式。
①Na2O2
②HClO
③NH4Cl
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】表为元素周期表的一部分,a、b、c……为其中几种元素。回答下列问题:
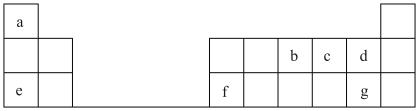
(1)写出b在元素周期表中的位置_______ 。
(2)元素d和g的气态氢化物中,更稳定的是_______ (写化学式)。
(3)元素d、e、g中原子半径由大到小的顺序为_______ (用元素符号表示)。
(4)元素e、g形成的化合物的电子式为_______ ,所含化学键类型为_______ 。
(5)a、c、e三种元素形成化合物的水溶液与g的最高价氧化物对应水化物反应的离子方程式:_______ 。

(1)写出b在元素周期表中的位置
(2)元素d和g的气态氢化物中,更稳定的是
(3)元素d、e、g中原子半径由大到小的顺序为
(4)元素e、g形成的化合物的电子式为
(5)a、c、e三种元素形成化合物的水溶液与g的最高价氧化物对应水化物反应的离子方程式:
您最近一年使用:0次



