前四周期的A、B、C、D四种元素在周期表中均与元素X紧密相邻。已知元素X最高价氧化物的化学式为X2O5,B、D同主族且B元素的原子半径是同族元素中最小的,C的最高价氧化物对应的水化物是强酸(本题中出现的 B 、 C 均为字母,不是元素符号 )。
(1)D元素基态原子的外围电子排布式为____________________ 。
(2)A、C、X三种元素原子的第一电离能由大到小的顺序为________________ (用相应的元素符号作答)。
(3)B、X、D氢化物的沸点由高到低的顺序为_______________ (用相应的化学式作答)。
(4)C元素的原子可形成多种离子,试推测下列微粒的立体构型(C为字母,不是碳元素):
(5)元素B的一种氢化物B2H4具有重要的用途。有关B2H4的说法正确的是___ 。
A.B2H4分子间可形成氢键 B.B原子是sp3杂化
C.B2H4分子中含有5个σ键和1个π键 D.B2H4晶体变为液态时破坏共价键
(6)E元素和D元素在同一周期,属于VIII族,价层有三个单电子,E(OH)2为两性氢氧化物,在浓的强碱溶液中可形成E(OH)42-,写出E(OH)2酸式电离的电离方程式_____________________________ 。
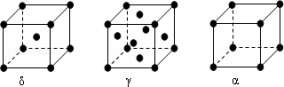
(7)F元素基态原子M层上有5对成对电子,F形成的单质有δ、γ、α三种同素异形体,三种晶胞(如下图所示)中F原子的配位数之比为___________ ,δ、γ、α三种晶胞的边长之比为_____________ 。
(1)D元素基态原子的外围电子排布式为
(2)A、C、X三种元素原子的第一电离能由大到小的顺序为
(3)B、X、D氢化物的沸点由高到低的顺序为
(4)C元素的原子可形成多种离子,试推测下列微粒的立体构型(C为字母,不是碳元素):
| 微粒 | CO32- | CO42- |
| 立体构型名称 |
(5)元素B的一种氢化物B2H4具有重要的用途。有关B2H4的说法正确的是
A.B2H4分子间可形成氢键 B.B原子是sp3杂化
C.B2H4分子中含有5个σ键和1个π键 D.B2H4晶体变为液态时破坏共价键
(6)E元素和D元素在同一周期,属于VIII族,价层有三个单电子,E(OH)2为两性氢氧化物,在浓的强碱溶液中可形成E(OH)42-,写出E(OH)2酸式电离的电离方程式
(7)F元素基态原子M层上有5对成对电子,F形成的单质有δ、γ、α三种同素异形体,三种晶胞(如下图所示)中F原子的配位数之比为

更新时间:2017-05-24 16:38:13
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】早期发现的一种天然二十面体准晶颗粒由 Al、Cu、Fe 三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过________ 方法区分晶体、准晶体和非晶体。
(2)基态Fe原子有________ 个未成对电子。Fe3+的电子排布式为_______________ 。
(3)新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为________ ,1 mol乙醛分子中含有的σ键的数目为________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有__________ 个铜原子。锗也是一种半导体材料,Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键,从原子结构角度分析,原因是______________________________ 。
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图:
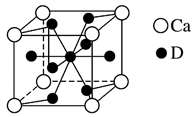
镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=________ (填数值);氢在合金中的密度为________ 。
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态Fe原子有
(3)新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图:

镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】碳是形成化合物种类最多的元素,其单质及化合物有独特的性质和用途。请回答下列问题。
(1)碳原子核外电子有_____ 种不同的运动状态。碳原子的价电子在形成sp3杂化后,其轨道表达式为_____ 。
(2)写出一种CO32-的等电子体微粒的化学式_______ ,其空间构型为_______ 。
(3)有机物M(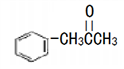 )在一定条件下生成N(
)在一定条件下生成N(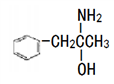 )。
)。
①沸点:M_____ N (填“大于”或“小于”)。
②M中碳原子杂化类型为_____ ,不同杂化类型的碳原子数之比为_____ 。
③有机物N中除氢原子之外的其他原子的第一电离能由大到小的顺序为_____ 。
(4)已知CaCO3的热分解温度为900℃,SrCO3的热分解温度为1172℃,试从原子结构的角度解释CaCO3的热分解温度低于SrCO3的原因_____________ 。
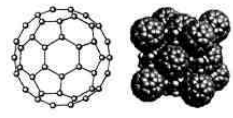
(5)碳的一种同素异形体C60,又名足球烯,是一种高度堆成的球碳分子。立方烷(分子式:C8H8,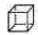 )是比C60约早20年合成出的一种对称性烃类分子,而如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
)是比C60约早20年合成出的一种对称性烃类分子,而如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为______________ 。
(6)石墨是碳的一种同素异形体,它的一种晶胞结构和部分晶胞参数如下图:
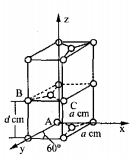
①原子坐标参数描述的是晶胞内原子间的相对位置。石墨晶胞中碳原子A、B的坐标参数分别为:A(0,0,0)、B(0,1,1/2)。则C原子的坐标参数为_______________ 。
②晶胞参数用以描述晶胞的大小和形状。已知石墨晶胞底边长为acm ,层间距为dcm,阿伏伽德罗常数的值为NA,则石墨的密度为_____ g·cm-3(写出表达式即可)。
(1)碳原子核外电子有
(2)写出一种CO32-的等电子体微粒的化学式
(3)有机物M(
 )在一定条件下生成N(
)在一定条件下生成N( )。
)。①沸点:M
②M中碳原子杂化类型为
③有机物N中除氢原子之外的其他原子的第一电离能由大到小的顺序为
(4)已知CaCO3的热分解温度为900℃,SrCO3的热分解温度为1172℃,试从原子结构的角度解释CaCO3的热分解温度低于SrCO3的原因
(5)碳的一种同素异形体C60,又名足球烯,是一种高度堆成的球碳分子。立方烷(分子式:C8H8,
 )是比C60约早20年合成出的一种对称性烃类分子,而如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
)是比C60约早20年合成出的一种对称性烃类分子,而如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
(6)石墨是碳的一种同素异形体,它的一种晶胞结构和部分晶胞参数如下图:

①原子坐标参数描述的是晶胞内原子间的相对位置。石墨晶胞中碳原子A、B的坐标参数分别为:A(0,0,0)、B(0,1,1/2)。则C原子的坐标参数为
②晶胞参数用以描述晶胞的大小和形状。已知石墨晶胞底边长为acm ,层间距为dcm,阿伏伽德罗常数的值为NA,则石墨的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】锰及其化合物的用途非常广泛。回答下列问题:
Ⅰ.一种锰化合物在不同条件下能高效催化 还原为CO或HCOOH,反应如下:
还原为CO或HCOOH,反应如下:

(1)基态Mn原子的价层电子排布为__________ 。含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物,则1mol该锰化合物中通过螯合作用形成的配位键有__________ mol。
(2) 中C的杂化方式为
中C的杂化方式为__________ ,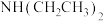 中N的杂化方式为
中N的杂化方式为__________ 。
(3)N、O和C三种元素的第一电离能大小顺序为__________ 。
(4)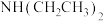 的碱性强于
的碱性强于 的主要原因为
的主要原因为__________ 。
Ⅱ.一种锰氧化物的晶胞结构如图所示。

(5)该锰氧化物的化学式为__________ 。
(6)已知该晶胞参数为a nm,阿伏加德罗常数为 ,则该锰氧化物的摩尔体积
,则该锰氧化物的摩尔体积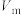 为
为__________  (列出计算式)。
(列出计算式)。
Ⅰ.一种锰化合物在不同条件下能高效催化
 还原为CO或HCOOH,反应如下:
还原为CO或HCOOH,反应如下:
(1)基态Mn原子的价层电子排布为
(2)
 中C的杂化方式为
中C的杂化方式为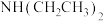 中N的杂化方式为
中N的杂化方式为(3)N、O和C三种元素的第一电离能大小顺序为
(4)
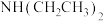 的碱性强于
的碱性强于 的主要原因为
的主要原因为Ⅱ.一种锰氧化物的晶胞结构如图所示。

(5)该锰氧化物的化学式为
(6)已知该晶胞参数为a nm,阿伏加德罗常数为
 ,则该锰氧化物的摩尔体积
,则该锰氧化物的摩尔体积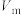 为
为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】M、N、R、X、Y为原子序数依次增大的短周期主族元素,Z、W都是第四周期过渡元素。R是同主族元素中最活泼的非金属元素,且能生成分子式为MR2型的共价化合物,Z和Z2+具有相同的单电子数,Z2+的价电子数是W+的二分之一,Z的一种氧化物是常见的催化剂。W有W+和W2+两种常见离子,R和X同主族。请回答下列问题(以下均用化学符号表示):
(1)写出R基态原子的电子排布图__ ,M、N和R第一电离能由小到大的顺序是__ 。
(2)N的气态氢化物极易溶于R的氢化物,且该体系呈碱性,由此可推出两者主要的结合方式(请用结构式表示)___ 。
(3)在上述元素形成的分子中,有四种分子互为等电子体,分别是MR2、MX2和MRX以及___ ,该分子的结构式为__ ,N与Y形成的NY3分子的空间构型是___ 。
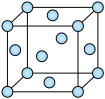
(4)M和R所形成MR2晶体以及W晶体的结构都可以如图表示(O表示一个MR2分子或一个W原子),晶体中正八面体和正四面体空隙数的比值是__ ,Z的硫化物有3种晶体,其中一种是Z2+为面心立方堆积,而晶体中全部正四面体空隙的二分之一被S2+占据,如果两种离子核间距为acm,则该晶体密度为___ 。
(1)写出R基态原子的电子排布图
(2)N的气态氢化物极易溶于R的氢化物,且该体系呈碱性,由此可推出两者主要的结合方式(请用结构式表示)
(3)在上述元素形成的分子中,有四种分子互为等电子体,分别是MR2、MX2和MRX以及
(4)M和R所形成MR2晶体以及W晶体的结构都可以如图表示(O表示一个MR2分子或一个W原子),晶体中正八面体和正四面体空隙数的比值是

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】[化学——选修3:物质结构与性质]
Ga和As在材料科学领域用途广泛。请回答下列问题:
(1)基态Ga原子价层电子的轨道表达式为_________ ;其核外电子占据最高能级的符号为___________ 。
(2)GaAs是优良的半导体材料,晶胞结构与金刚石相似。该晶体中不含有的化学键类型
为___________ (填选项字母)。
A.σ键 B.π键 C.配位键 D.金属键
(3)Ga、N、As的合金材料是制作太阳能电池的重要原料,三种基态原子的第一电离能由小到大的顺序为________________________ (用元素符号表示)。
(4)AsH3的立体构型为___________ 。相同压强下,AsH3的沸点低于NH3的原因为___________ 。
(5)LiZnAS基稀磁半导体晶胞如图所示,该晶体的密度为ρg·cm-3,阿伏伽德罗常数的值为NA。则:

①与Li原子距离最近且相等的Zn原子的数目为____________ 。
②晶胞参数a =_____________ pm(用代数式表示)。
Ga和As在材料科学领域用途广泛。请回答下列问题:
(1)基态Ga原子价层电子的轨道表达式为
(2)GaAs是优良的半导体材料,晶胞结构与金刚石相似。该晶体中不含有的化学键类型
为
A.σ键 B.π键 C.配位键 D.金属键
(3)Ga、N、As的合金材料是制作太阳能电池的重要原料,三种基态原子的第一电离能由小到大的顺序为
(4)AsH3的立体构型为
(5)LiZnAS基稀磁半导体晶胞如图所示,该晶体的密度为ρg·cm-3,阿伏伽德罗常数的值为NA。则:

①与Li原子距离最近且相等的Zn原子的数目为
②晶胞参数a =
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】由金属Na、Cu、C、N、B等元素组成的物质在生活和工业上有着广泛用途。
(1)基态Cu+的外围电子轨道式为_______ 。
(2)H3BNH3是储氢材料,其制备原理为:3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3,其中(HB=NH)3是一种六元环状化合物。化合物H3BNH3中B原子的杂化方式为_______ ;1个(HB=NH)3分子中含有 ___ 个σ键。
(3) B、C、N、O原子的第一电离能由大到小的顺序为_____________________ 。
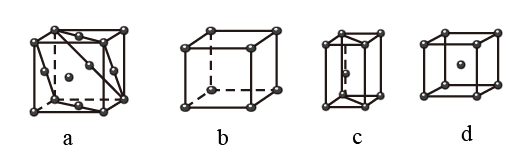
(4)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为____ (填字母)。
(5)已知NaCl的摩尔质量为Mg·mol-1,密度为pg·㎝-3,阿伏伽德罗常数为NA mol-1,在NaCl晶体中,两个距离最近的Cl-中心间的距离为____________ 。
(1)基态Cu+的外围电子轨道式为
(2)H3BNH3是储氢材料,其制备原理为:3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3,其中(HB=NH)3是一种六元环状化合物。化合物H3BNH3中B原子的杂化方式为
(3) B、C、N、O原子的第一电离能由大到小的顺序为
(4)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为

(5)已知NaCl的摩尔质量为Mg·mol-1,密度为pg·㎝-3,阿伏伽德罗常数为NA mol-1,在NaCl晶体中,两个距离最近的Cl-中心间的距离为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】卤化物、氢化物在科研和生活中占有重要地位。回答下列问题:
(1)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是 。
(2) 的VSEPR模型名称为
的VSEPR模型名称为____________ 。
(3)二氟氮烯(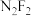 )分子中,每个原子均满足八电子稳定结构,则
)分子中,每个原子均满足八电子稳定结构,则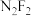 的结构式为
的结构式为____________ 。
(4)C、N、O三种元素都能与H元素形成含A-A(A表示C、N、O元素)键的氢化物。氢化物中A-A键的键能( )如下表:
)如下表:
A-A键的键能依次降低的原因是____________________________________________________________ 。
(5)第三代太阳能电池利用有机金属卤化物碘化铅甲胺( )半导体作为吸光材料。
)半导体作为吸光材料。 的晶胞如图所示,其中
的晶胞如图所示,其中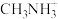 位于顶点(大空心球)位置。已知
位于顶点(大空心球)位置。已知 晶体的晶胞参数为a nm,阿伏加德罗常数的值为
晶体的晶胞参数为a nm,阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为____________  。(用最简式表达)
。(用最简式表达)

(1)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是 。
A. | B. | C. | D. |
 的VSEPR模型名称为
的VSEPR模型名称为(3)二氟氮烯(
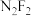 )分子中,每个原子均满足八电子稳定结构,则
)分子中,每个原子均满足八电子稳定结构,则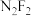 的结构式为
的结构式为(4)C、N、O三种元素都能与H元素形成含A-A(A表示C、N、O元素)键的氢化物。氢化物中A-A键的键能(
 )如下表:
)如下表:
|
| HO-OH |
346 | 247 | 207 |
(5)第三代太阳能电池利用有机金属卤化物碘化铅甲胺(
 )半导体作为吸光材料。
)半导体作为吸光材料。 的晶胞如图所示,其中
的晶胞如图所示,其中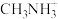 位于顶点(大空心球)位置。已知
位于顶点(大空心球)位置。已知 晶体的晶胞参数为a nm,阿伏加德罗常数的值为
晶体的晶胞参数为a nm,阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为 。(用最简式表达)
。(用最简式表达)
您最近一年使用:0次
【推荐2】现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素。请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有___________ 个方向,C简单离子核外有___________ 种运动状态不同的电子。
(2) 难溶于二硫化碳,简要说明理由
难溶于二硫化碳,简要说明理由___________ 。
(3) 分子的空间构型为
分子的空间构型为___________ , 分子的VSEPR模型名称为
分子的VSEPR模型名称为___________ 。
(4)下列气态分子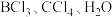 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为___________ 。
| 元素 | 相关信息 |
| A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 原子核外P电子数与s电子数相等 |
| C | 基态原子的价电子排布为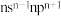 |
| D | 能层数与C相同,且电负性比C大 |
| E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)
 难溶于二硫化碳,简要说明理由
难溶于二硫化碳,简要说明理由(3)
 分子的空间构型为
分子的空间构型为 分子的VSEPR模型名称为
分子的VSEPR模型名称为(4)下列气态分子
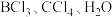 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的作用。
(1)Cu+的核外电子排布式为__________ ;N元素与O元素的第一电离能比较:N____ O(填“>”、“<”或“=”)。
(2)与N3-含有相同电子数的四原子分子的空间构型为____________________ 。
(3)在Cu催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中醛其(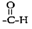 )碳原子的杂化方式为
)碳原子的杂化方式为_________ 。
(4)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被C1-取代可生成Cu(H2O)2Cl2,试画出其具有极性的分子的结构式_________ 。
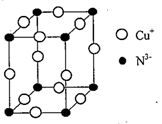
(5)Cu3N 的晶胞结构如图所示,N3-的配位数为________ ;若晶胞棱长为anm,NA表示阿伏伽德罗常数的值,则Cu3N的密度p=______ g/cm3[用含a和NA 的式子表示,Mr(Cu3N)=206]
 .
.
(1)Cu+的核外电子排布式为
(2)与N3-含有相同电子数的四原子分子的空间构型为
(3)在Cu催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中醛其(
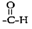 )碳原子的杂化方式为
)碳原子的杂化方式为(4)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被C1-取代可生成Cu(H2O)2Cl2,试画出其具有极性的分子的结构式
(5)Cu3N 的晶胞结构如图所示,N3-的配位数为
 .
.
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】我国秦俑彩绘和汉代器物上用的颜料被称为“中国蓝”、“中国紫”,近年来,人们对这些颜料的成分进行了研究,发现其成分主要为BaCuSi4O10、BaCuSi2O6
(1)颜料中含有Cu元素,基态Cu原子的价电子排布式为___________ ;Si、O、Ba元素电负性由大到小的顺序为_____ ,干冰、Si、SiC熔点由高到低的顺序为_____________ 。
(2)“中国蓝”的发色中心是以Cu2+为中心离子的配位化合物,其中提供孤电子对的是_______ 元素。
(3)铜可作CH3CH2OH氧化生成CH3CHO的催化剂。乙醇的沸点高于乙醛,其主要原因是_____________________________ 。
(4)C、N元素与颜料中的氧元素同周期。
①写出CO的一种常见等电子体分子的电子式________________ ;C、N、O的第一电离能由大到小的顺序为__________________________________ 。
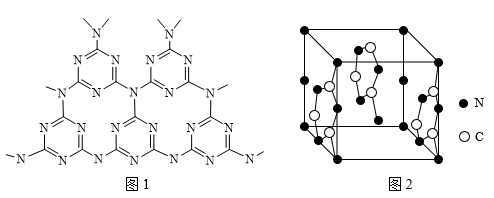
②C、N元素能形成一种类石墨的聚合物半导体g-C3N4其单层平面结构如图1,晶胞结构如图2。
ⅰ.g-C3N4中氮原子的杂化类型是___________________ 。
ⅱ.根据图2,在图1中用平行四边形画出一个最小重复单元_____________ 。
ⅲ.已知该晶胞的体积为Vcm3,中间层原子均在晶胞内部。设阿伏加德罗常数的值为NA,则g- C3N4的密度为___________________ 。
(1)颜料中含有Cu元素,基态Cu原子的价电子排布式为
(2)“中国蓝”的发色中心是以Cu2+为中心离子的配位化合物,其中提供孤电子对的是
(3)铜可作CH3CH2OH氧化生成CH3CHO的催化剂。乙醇的沸点高于乙醛,其主要原因是
(4)C、N元素与颜料中的氧元素同周期。
①写出CO的一种常见等电子体分子的电子式
②C、N元素能形成一种类石墨的聚合物半导体g-C3N4其单层平面结构如图1,晶胞结构如图2。

ⅰ.g-C3N4中氮原子的杂化类型是
ⅱ.根据图2,在图1中用平行四边形画出一个最小重复单元
ⅲ.已知该晶胞的体积为Vcm3,中间层原子均在晶胞内部。设阿伏加德罗常数的值为NA,则g- C3N4的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】稀土正铁氧体RFeO3晶体是一类重要的多功能磁性材料,稳定的RFeO3晶体具有优异的磁光和光磁特性,我国科学家在磁光和光磁调控方面取得一系列重要研究进展。
回答下列问题:
(1)铁元素是构成人体的不可缺少的元素之一,亚铁离子是血红蛋白的重要组成成分。请写出Fe2+的核外电子排布式___________ ;铁的第四电离能I4远大于第三电离能I3的原因是___________ 。
(2)某含铁络合物具有顺磁性,结构如图所示。组成该含铁络合物的第二周期元素中,电负性由大到小的顺序为___________ (用元素符号表示)。该含铁络合物中N原子的杂化方式为___________ ,碳原子价层电子对的空间构型为___________ 。
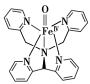
(3)铁在200 ℃、1×104 kPa压强下和一氧化碳反应,生成五羰基铁Fe(CO)5.Fe(CO)5为黄色液体,沸点103 ℃,Fe(CO)5属于___________ 晶体;铁在氯气中加热,生成三氯化铁,三氯化铁在300 ℃以上升华,气相为二聚体Fe2Cl6.Fe2Cl6中所含的化学键为___________ (填字母序号)。
A.离子键 B.共价键 C.配位键 D.氢键
(4)六方相RFeO3晶胞结构如图所示。R表示Sc与Lu元素,晶胞上下面面心为Sc,顶点为Lu,六方晶胞的高为p nm,正六边形底的边长为q nm。
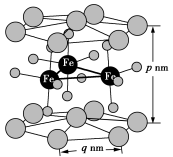
①六方相RFeO3的化学式为___________ 。
②RFeO3晶胞的密度是___________ g·cm−3。
回答下列问题:
(1)铁元素是构成人体的不可缺少的元素之一,亚铁离子是血红蛋白的重要组成成分。请写出Fe2+的核外电子排布式
(2)某含铁络合物具有顺磁性,结构如图所示。组成该含铁络合物的第二周期元素中,电负性由大到小的顺序为

(3)铁在200 ℃、1×104 kPa压强下和一氧化碳反应,生成五羰基铁Fe(CO)5.Fe(CO)5为黄色液体,沸点103 ℃,Fe(CO)5属于
A.离子键 B.共价键 C.配位键 D.氢键
(4)六方相RFeO3晶胞结构如图所示。R表示Sc与Lu元素,晶胞上下面面心为Sc,顶点为Lu,六方晶胞的高为p nm,正六边形底的边长为q nm。

①六方相RFeO3的化学式为
②RFeO3晶胞的密度是
您最近一年使用:0次
【推荐3】铼被誉为21世纪的超级金属,被广泛应用于航空航天领域,一种由铼渣(主要成分:ReS2)提取铼的工艺流程图如下:

(1)已知铼的价电子排布与锰相似,写出75Re的价电子排布式为_______ 。
(2)第一步酸浸过程中ReS2转化为两种强酸,其中一种为高铼酸(化学式:HReO4),请写出反应的离子方程式:_______ ,根据图1所示,浸出过程中应将铼渣粉碎至_______ 目左右,根据图2所示,操作II过程中萃取液流速应选择6~8BV/h,其原因为_______ 。

(3)已知高铼酸铵微溶于冷水,易溶于热水。提纯粗高铼酸铵固体的方法是_______ 。
(4)写出由高铼酸铵热解得到Re2O7的化学方程式:_____ ,通入氧气的目的是______ 。
(5)实际生产过程中,使用氢气还原Re2O7时,氢气的用量始终要大于理论计算值,其原因是_______ 。
(6)整个工艺中可循环利用的物质有硫酸、氨气以及_______ 。
(7)已知铼的晶胞如图3所示,晶胞的参数如图4所示(a、c的单位为Å,1Å=10-10m),则金属铼的密度表达式为_______ g/cm3.(用NA表示阿伏加德罗常数的值,M表示Re的摩尔质量,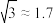 )
)


(1)已知铼的价电子排布与锰相似,写出75Re的价电子排布式为
(2)第一步酸浸过程中ReS2转化为两种强酸,其中一种为高铼酸(化学式:HReO4),请写出反应的离子方程式:

(3)已知高铼酸铵微溶于冷水,易溶于热水。提纯粗高铼酸铵固体的方法是
(4)写出由高铼酸铵热解得到Re2O7的化学方程式:
(5)实际生产过程中,使用氢气还原Re2O7时,氢气的用量始终要大于理论计算值,其原因是
(6)整个工艺中可循环利用的物质有硫酸、氨气以及
(7)已知铼的晶胞如图3所示,晶胞的参数如图4所示(a、c的单位为Å,1Å=10-10m),则金属铼的密度表达式为
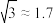 )
)
您最近一年使用:0次





