已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:
3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
①写出该反应的离子方程式______ .
②用双线桥标出该反应电子转移的方向和数目______ .
3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
③若19.2g铜与足量硝酸完全反应,则消耗硝酸为______ mol,
被还原的硝酸为______ mol
生成NO的体积为______ L(标准状况)
3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
①写出该反应的离子方程式
②用双线桥标出该反应电子转移的方向和数目
3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
③若19.2g铜与足量硝酸完全反应,则消耗硝酸为
被还原的硝酸为
生成NO的体积为
更新时间:2017-07-04 10:50:13
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】将64g Cu投入100mL  的浓硝酸中,当硝酸全部反应时,收集到标准状况下
的浓硝酸中,当硝酸全部反应时,收集到标准状况下 和NO的混合气体8.96L。
和NO的混合气体8.96L。
(1)被还原的硝酸的物质的量是___________ 。
(2)生成的NO气体在标准状况下的体积为___________ 。
(3)如果向反应后的溶液中再加入100mL 2mol/L的稀硫酸,发现铜片又逐渐溶解,产生无色气体,则发生反应的离子方程式为___________ ,又继续溶解的Cu的质量为___________ 。
 的浓硝酸中,当硝酸全部反应时,收集到标准状况下
的浓硝酸中,当硝酸全部反应时,收集到标准状况下 和NO的混合气体8.96L。
和NO的混合气体8.96L。(1)被还原的硝酸的物质的量是
(2)生成的NO气体在标准状况下的体积为
(3)如果向反应后的溶液中再加入100mL 2mol/L的稀硫酸,发现铜片又逐渐溶解,产生无色气体,则发生反应的离子方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某兴趣小组设计实验测定“自然晶盐"的含碘量。取5.00g自然晶盐,加蒸馏水使其完全溶解后加稀硫酸酸化并加入足量的KI溶液,使 与KI反应完全。以淀粉为指示剂,逐滴滴加
与KI反应完全。以淀粉为指示剂,逐滴滴加 的
的 溶液5.00mL,达到滴定终点(反应为
溶液5.00mL,达到滴定终点(反应为 )。
)。
(1)写出 与KI反应的离子方程式
与KI反应的离子方程式___________ 。
(2)上述“自然晶盐"中的碘元素含量为___________ mg/kg(写出计算过程,精确到小数点后一位)。
 与KI反应完全。以淀粉为指示剂,逐滴滴加
与KI反应完全。以淀粉为指示剂,逐滴滴加 的
的 溶液5.00mL,达到滴定终点(反应为
溶液5.00mL,达到滴定终点(反应为 )。
)。(1)写出
 与KI反应的离子方程式
与KI反应的离子方程式(2)上述“自然晶盐"中的碘元素含量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】能基于物质的量认识物质的组成及其化学变化,是学生必备的学科素养。
(1)已知:①5.6LH2S(标准状况下)②1.204×1023个NH3分子③4.8gCH4④4℃时,5.4mL水,其中含有的氢原子数由大到小的顺序为__ 。
(2)同浓度的三种溶液:Na2SO4、MgSO4、Al2(SO4)3,其体积比为3:2:1,则SO 浓度之比为
浓度之比为__ 。
(3)在标准状况下,将VLHCl溶于0.1L水中,所得溶液的密度为dg·cm-3,则形成溶液的物质的量浓度为__ mol·L-1。
(4)某工厂废液中含有K2Cr2O7,排放废液前要将废液中的Cr2O 还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为
还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为__ mol·L-1。
(5)联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨气反应制备联氨(N2H4),反应的化学方程式为__ 。
(6)用零价铁(Fe)去除水体中的硝酸盐(NO )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。
实验研究表明,将足量铁粉投入 =2.5的水体中,经24小时测得水体中NO
=2.5的水体中,经24小时测得水体中NO 去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH
去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH ,反应0.1molNO
,反应0.1molNO 恰好消耗16.8gFe,则反应的离子方程式为
恰好消耗16.8gFe,则反应的离子方程式为__ 。
(1)已知:①5.6LH2S(标准状况下)②1.204×1023个NH3分子③4.8gCH4④4℃时,5.4mL水,其中含有的氢原子数由大到小的顺序为
(2)同浓度的三种溶液:Na2SO4、MgSO4、Al2(SO4)3,其体积比为3:2:1,则SO
 浓度之比为
浓度之比为(3)在标准状况下,将VLHCl溶于0.1L水中,所得溶液的密度为dg·cm-3,则形成溶液的物质的量浓度为
(4)某工厂废液中含有K2Cr2O7,排放废液前要将废液中的Cr2O
 还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为
还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为(5)联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨气反应制备联氨(N2H4),反应的化学方程式为
(6)用零价铁(Fe)去除水体中的硝酸盐(NO
 )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。实验研究表明,将足量铁粉投入
 =2.5的水体中,经24小时测得水体中NO
=2.5的水体中,经24小时测得水体中NO 去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH
去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH ,反应0.1molNO
,反应0.1molNO 恰好消耗16.8gFe,则反应的离子方程式为
恰好消耗16.8gFe,则反应的离子方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,实验室制取高铁酸钠的化学方程式如下 :
(1)请用双线桥法表达出此反应的电子转移情况:__________
2Fe( NO3 )3+16NaOH+3Cl2=2Na2FeO4+6NaNO3 +6NaCl+8H2O
(2)若要制取8.3g高铁酸钠需要标准下Cl2的体积为多少?______ 若所用氢氧化钠溶液体积为200mL,则氢氧化钠溶液的物质的量浓度是多少?(写出计算过程)_______
(1)请用双线桥法表达出此反应的电子转移情况:
2Fe( NO3 )3+16NaOH+3Cl2=2Na2FeO4+6NaNO3 +6NaCl+8H2O
(2)若要制取8.3g高铁酸钠需要标准下Cl2的体积为多少?
您最近一年使用:0次
【推荐2】过氧化氢溶液俗称双氧水,有杀菌消毒的作用,医疗上常用它来清洗伤口。双氧水有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。
(1)配平下列化学反应,并用单线桥表示电子转移的方向和数目:____________ 。


(2)要消除采矿业胶液中的氰化物(如KCN,C为+2价),可经反应
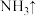 实现,A的化学式为
实现,A的化学式为_______ ,若此反应中有6.72 L(标准状况)气体生成,则转移电子的数目为_______ (用NA表示)。
(3)高锰酸钾也可用于医疗杀菌消毒。根据反应条件可判断氧化剂氧化能力的强弱。例如:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则MnO2和KMnO4相比,
MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则MnO2和KMnO4相比,__________ (填化学式)的氧化性强。某强酸性反应体系中,反应物和产物共六种粒子: 、
、 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生了如下过程:
只发生了如下过程: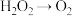 ,则该反应中发生还原反应的过程是
,则该反应中发生还原反应的过程是__________ →__________ ,该反应应选择的酸是__________ (填字母)。
A.盐酸 B.醋酸 C.稀硫酸
(4)用32 mL 0.2 mol/L 溶液,还原含4×10-3 mol
溶液,还原含4×10-3 mol 的溶液,过量的Na2SO3用0.2 mol/L酸性KMnO4溶液氧化(其中KMnO4被还原成Mn2+),共消耗0.8 mL酸性KMnO4溶液,则元素X在还原产物中的化合价是
的溶液,过量的Na2SO3用0.2 mol/L酸性KMnO4溶液氧化(其中KMnO4被还原成Mn2+),共消耗0.8 mL酸性KMnO4溶液,则元素X在还原产物中的化合价是______ (填字母)。
A.+1 B.+2 C.+3 D.+4
(1)配平下列化学反应,并用单线桥表示电子转移的方向和数目:


(2)要消除采矿业胶液中的氰化物(如KCN,C为+2价),可经反应

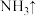 实现,A的化学式为
实现,A的化学式为(3)高锰酸钾也可用于医疗杀菌消毒。根据反应条件可判断氧化剂氧化能力的强弱。例如:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则MnO2和KMnO4相比,
MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则MnO2和KMnO4相比, 、
、 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生了如下过程:
只发生了如下过程: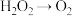 ,则该反应中发生还原反应的过程是
,则该反应中发生还原反应的过程是A.盐酸 B.醋酸 C.稀硫酸
(4)用32 mL 0.2 mol/L
 溶液,还原含4×10-3 mol
溶液,还原含4×10-3 mol 的溶液,过量的Na2SO3用0.2 mol/L酸性KMnO4溶液氧化(其中KMnO4被还原成Mn2+),共消耗0.8 mL酸性KMnO4溶液,则元素X在还原产物中的化合价是
的溶液,过量的Na2SO3用0.2 mol/L酸性KMnO4溶液氧化(其中KMnO4被还原成Mn2+),共消耗0.8 mL酸性KMnO4溶液,则元素X在还原产物中的化合价是A.+1 B.+2 C.+3 D.+4
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】根据物质的量的相关知识,填写下列空格:
(1)标准状况下,33.6L混合气体中CO、H2的质量比为42: 4,则CO的体积为___________ ;
(2)若30g密度为dg/mL的AlCl3的溶液中含有0.9gAl3+ (不考虑Al3+与水反应),则Cl-物质的量浓度为___________ ;
(3)反应3NO2+H2O=2HNO3+NO中,当有0.6mol e- 发生转移时,产生NO气体在标准状况下的体积为___________ 。
(1)标准状况下,33.6L混合气体中CO、H2的质量比为42: 4,则CO的体积为
(2)若30g密度为dg/mL的AlCl3的溶液中含有0.9gAl3+ (不考虑Al3+与水反应),则Cl-物质的量浓度为
(3)反应3NO2+H2O=2HNO3+NO中,当有0.6mol e- 发生转移时,产生NO气体在标准状况下的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3==K2O+5Na2O+16N2↑。
(1)用单线桥法标明电子转移的方向和数目。______ 10NaN3+2KNO3==K2O+5Na2O+16N2↑
(2)若氧化产物比还原产物多49g,则:
A.生成______ gN2
B.有______ g的KNO3被还原
C.参加反应的NaN3质量为______ g
(1)用单线桥法标明电子转移的方向和数目。
(2)若氧化产物比还原产物多49g,则:
A.生成
B.有
C.参加反应的NaN3质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】钾是活泼的碱金属,钾和氧有氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物。
⑴钾和硝酸钾反应可制得氧化钾:K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有___________ g
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。写出超氧化钾与二氧化碳反应的化学方程式______________________ ,为了维持气压稳定,可以使用超氧化钾和过氧化钾的混合物使吸收的CO2与生成的O2体积相同(同温同压),则它们的物质的量之比为n(KO2) :n(K2O2)=____________
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比_______ 。如果产物A只含有两种化合物,写出所有可能的化学式并计算A中两种化合物的物质的量之比_______ 。
⑴钾和硝酸钾反应可制得氧化钾:K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。写出超氧化钾与二氧化碳反应的化学方程式
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比
您最近一年使用:0次

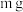 某气体(由双原子分子构成),其摩尔质量为
某气体(由双原子分子构成),其摩尔质量为 ,阿伏加 德罗常数用
,阿伏加 德罗常数用 表示,试求
表示,试求 。
。
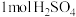 被还原时,转移电子的物质的量为
被还原时,转移电子的物质的量为 ,生成标准状况下
,生成标准状况下 的体积为
的体积为

