钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______ nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据的最高能层的符号是_________ ,占据该能层电子的电子云轮廓图形状为___________ 。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________________________ 。
(3)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为_____________ ,中心原子的杂化形式为________________ 。
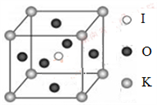
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为______ nm,与K紧邻的O个数为__________ 。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于______ 位置,O处于______ 位置。
 .
.
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据的最高能层的符号是
(3)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于
 .
.
2017·全国·高考真题 查看更多[22]
云南省富宁县第一中学校2021-2022学年高三下学期开学考试理综化学试题云南省玉溪市民族中学2021-2022学年高三1月份考试理综化学试题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)广西蒙山县第一中学2018-2019学年高二下学期第二次月考化学试题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练湖北省武汉市华中师范大学第一附属中学2020届高三下学期四月份网络教学质量监测理科综合化学试题安徽省合肥市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题北京市中国人民大学附属中学2020届高三教学质量监测理科综合化学试题广东省深圳中学2020届高三2月份网络教学质量监测理综化学试题河北省衡水中学2020届高三四月份质量监测理综化学试题广东省梅州市五华县2018-2019学年高二上学期第六次质量监测化学试题云南省大理白族自治州祥云县第一中学2020届高三下学期4月月考理综化学试题第3章 物质的聚集状态与物质性质——C挑战区 模拟高考(鲁科版选修3)四川省成都实验中学2019-2020学年度高三上学期1月月考理科综合化学试题云南省富宁县民族中学2020届高三上学期开学考试化学试题(已下线)《2019年高考总复习巅峰冲刺》专题12 物质结构与性质应试策略西藏自治区昌都第四高级中学2019届高三下学期4月月考理科综合化学试题(已下线)解密21 物质的结构与性质(教师版)——备战2018年高考化学之高频考点解密(已下线)《考前20天终极攻略》5月30日 物质结构与性质(已下线)【艺体生文化课百题突围系列-基础练测】专题2.17 物质结构与性质(选修)(已下线)【中等生百日捷进提升系列-基础练测】专题2.17 物质结构与性质2017年全国普通高等学校招生统一考试理综化学(新课标Ⅰ卷精编版)
更新时间:2017/08/09 09:10:30
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】镓(Ga)、锗( Ge)、砷(As)、硒(Se)均为第四周期的元素,它们在高科技尖端科学特别是信息领域有着广泛的用途。试回答下列问题:
(1)基态锗原子的价电子排布图为______________________ 。
(2)沸点:NH3__________ AsH3(填“>”、“<”或“=”),原因是_________________________ 。
(3)H2SeO4和H2SeO3是硒的两种含氧酸,请根据结构与性质的关系,解释H2SeO4比H2SeO3 酸性强的原因____ 。
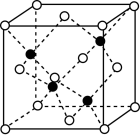
(4)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,同时得到一种最简单的有机物,写出该反应的方程式为_____________________ ;砷化镓的晶胞结构如下图所示,其晶胞边长为a pm(1pm=10-12m),则每立方厘米该晶体中所含砷元素的质量为____________ g(用NA表示阿伏伽德罗常数的值)。
(1)基态锗原子的价电子排布图为
(2)沸点:NH3
(3)H2SeO4和H2SeO3是硒的两种含氧酸,请根据结构与性质的关系,解释H2SeO4比H2SeO3 酸性强的原因
(4)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,同时得到一种最简单的有机物,写出该反应的方程式为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钾和碘是人体内的必需元素,两者的化合物也有着广泛的应用。回答下列问题:
(1)某化合物的晶胞结构如图所示,该晶胞的边长为a。
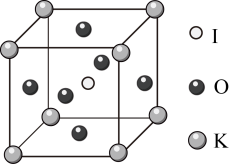
则该晶体的化学式为________ ,K与I间的最短距离为________ (用a表示),与I紧邻的O个数为________ 。
(2)该晶胞结构的另一种表示中,I 处于各顶角位置,则K处于________ 位置,O处于________ 位置。
(3)碳元素的单质有多种形式,如图依次是C60、石墨和金刚石的结构图:
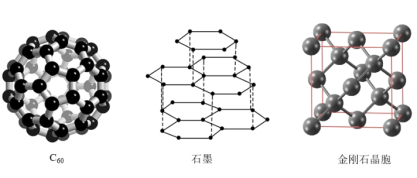
回答下列问题:
①在石墨晶体中,碳原子数与化学键数之比为________ 。
②上述三种晶体的熔点由高到低的顺序为________ ,解释原因_________ 。
(1)某化合物的晶胞结构如图所示,该晶胞的边长为a。

则该晶体的化学式为
(2)该晶胞结构的另一种表示中,I 处于各顶角位置,则K处于
(3)碳元素的单质有多种形式,如图依次是C60、石墨和金刚石的结构图:

回答下列问题:
①在石墨晶体中,碳原子数与化学键数之比为
②上述三种晶体的熔点由高到低的顺序为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】【化学一选修3: 物质结构与性质】1735年瑞典化学家布兰特(G·Brands)制出金属钴。钴的矿物或钴的化合物一直用作陶瓷、玻璃、珐琅的釉料。到20世纪,钴及其合金在电机、机械、化工、航空和航天等工业部门得到广泛的应用,并成为一种重要的战略金属。所以钴及其化合物具有重要作用,回答下列问题:
(1)基态Co原子的电子排布式为___________ 。
(2)[Co(NH3)5H2O]Cl3是一种砖红色的晶体,可通过CoCl2、NH4Cl、浓氨水、H2O2制得。
①Co、N、0原子的第一电离能由大到小的顺序是__________ 。
②[Co(NH3)5H2O]Cl3中Co元素化合价为____ ,其配位原子为_____ ;1mol该晶体中含有____ molσ键。
③H2O2中O原子的杂化轨道类型是______ ,H2O2能与水互溶,除都是极性分子外,还因为____ 。
④NH3、NF3的空间构型都相同,但Co3+易与NH3形成配离子,而NF3不能。原因是________ 。
(3)CoO晶胞如图,已知Co原子半径为apm,O原子半径为bpm,则等距最近的所有O原子围成的空间形状为_____ ;该晶胞中原子的空间利用率为__________ (用含a、b的计算式表示)。

(1)基态Co原子的电子排布式为
(2)[Co(NH3)5H2O]Cl3是一种砖红色的晶体,可通过CoCl2、NH4Cl、浓氨水、H2O2制得。
①Co、N、0原子的第一电离能由大到小的顺序是
②[Co(NH3)5H2O]Cl3中Co元素化合价为
③H2O2中O原子的杂化轨道类型是
④NH3、NF3的空间构型都相同,但Co3+易与NH3形成配离子,而NF3不能。原因是
(3)CoO晶胞如图,已知Co原子半径为apm,O原子半径为bpm,则等距最近的所有O原子围成的空间形状为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】含硼、氮、磷的化合物有许多重要用途,如:(CH3)3N、Cu3P、磷化硼等。回答下列问题:
(1)基态B原子电子占据最高能级的电子云轮廓图为_____ ;基态Cu+的核外电子排布式为_____ 。
(2)化合物(CH3)3N分子中N原子杂化方式为_____ ,该物质能溶于水的原因是_____ 。
(3)PH3分子的键角小于NH3分子的原因是_____ ;亚磷酸(H3PO3)是磷元素的一种含氧酸,与NaOH反应只生成NaH2PO3和Na2HPO3两种盐,则H3PO3分子的结构式为_____ 。
(4)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图1所示:
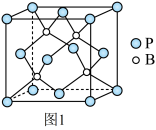
①在一个晶胞中磷原子的配位数为_____ 。
②已知磷化硼晶体的密度为ρg/cm3,阿伏加 德罗常数为NA,则B-P键长为_____ 。
(1)基态B原子电子占据最高能级的电子云轮廓图为
(2)化合物(CH3)3N分子中N原子杂化方式为
(3)PH3分子的键角小于NH3分子的原因是
(4)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图1所示:

①在一个晶胞中磷原子的配位数为
②已知磷化硼晶体的密度为ρg/cm3,阿伏加 德罗常数为NA,则B-P键长为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】KZnF3是一种良好的光学材料,可由K2CO3、ZnF2、NH4HF2制备,掺杂Co、Ni等过渡金属可得到不同的荧光材料,回答下列问题:
(1)基态F原子的价电子轨道表达式为___ ;基态Zn原子核外占据最高能层电子的电子云轮廓图形状为___ 。
(2)K2CO3中阴离子的立体构型为___ ,NH4HF2中N原子的杂化方式为___ 。
(3)某镍配合物结构如图所示。
①分子内含有的化学键有___ (填序号)。
②配合物中元素原子的第一电离能N___ O(填“>”“<”或“=”),从原子结构角度解释原因是___ 。
(4)KZnF3具有钙钛矿型立方结构,其晶胞结构如图所示:___ 。
②已知晶胞边长为a pm,NA表示阿伏加德罗常数的值,则KZnF3晶体的密度为___ g·cm-3(用含a、NA的代数式表示)。
(1)基态F原子的价电子轨道表达式为
(2)K2CO3中阴离子的立体构型为
(3)某镍配合物结构如图所示。
①分子内含有的化学键有
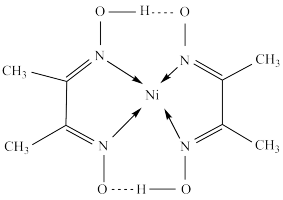
②配合物中元素原子的第一电离能N
(4)KZnF3具有钙钛矿型立方结构,其晶胞结构如图所示:
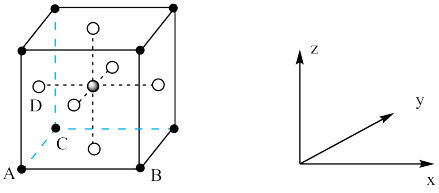
②已知晶胞边长为a pm,NA表示阿伏加德罗常数的值,则KZnF3晶体的密度为
您最近半年使用:0次
【推荐3】合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。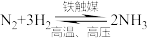
(1)基态氢原子中,核外电子的电子云轮廓图形状为_______
(2)自然界中的复元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为_______
② 分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
分子中,与N原子相连的H显正电性。N、H电负性大小顺序为_______ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、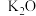 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是_______ 。
②比较 、
、 第一电高能的大小:
第一电高能的大小:_______
③表中的数据从上到下是纳、镁、铝逐级失去电子的电离能。
为什么原子的逐级电高能越来越大?______ ;结合数据说明为什么 的常见化合价为
的常见化合价为 价:请解释之:
价:请解释之:_______ 。
(4)目前合成氨通常采用的压强为 温度为
温度为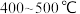 ,十分耗能。我国科研人员研制出了“
,十分耗能。我国科研人员研制出了“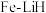 ”等催化剂,温度、压强分别降到了350℃、
”等催化剂,温度、压强分别降到了350℃、 ,这是近年来合成纸反应研究中的重要突破。
,这是近年来合成纸反应研究中的重要突破。
①基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
②比较 与
与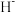 的半径大小关系:
的半径大小关系:
_______ 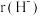 (填“>”或“<”)。
(填“>”或“<”)。
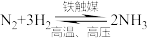
(1)基态氢原子中,核外电子的电子云轮廓图形状为
(2)自然界中的复元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②
 分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
分子中,与N原子相连的H显正电性。N、H电负性大小顺序为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、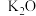 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较
 、
、 第一电高能的大小:
第一电高能的大小:③表中的数据从上到下是纳、镁、铝逐级失去电子的电离能。
| 元素 |  |  |  |
电离能(kJ mol-1) mol-1) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
 的常见化合价为
的常见化合价为 价:请解释之:
价:请解释之:(4)目前合成氨通常采用的压强为
 温度为
温度为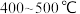 ,十分耗能。我国科研人员研制出了“
,十分耗能。我国科研人员研制出了“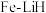 ”等催化剂,温度、压强分别降到了350℃、
”等催化剂,温度、压强分别降到了350℃、 ,这是近年来合成纸反应研究中的重要突破。
,这是近年来合成纸反应研究中的重要突破。①基态
 原子的核外电子排布式为
原子的核外电子排布式为②比较
 与
与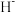 的半径大小关系:
的半径大小关系:
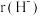 (填“>”或“<”)。
(填“>”或“<”)。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用,其中铁和铜是两种应用广泛的元素。
(1)基态铁原子的价电子轨道表达式为_____ 。
(2)磁性材料铁氧体在制备时常加入 CH3COONa、尿素[CO(NH2)2]等碱性物质。尿素分子中所含元素的电负性由小到大的顺序是_____ ,1mol 尿素分子中含有的 σ 键数目为_____ 。 CH3COONa 中碳原子的杂化类型为_________ 。
(3)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则 Fe(CO)5的晶体类型是_____ ,写出与CO互为等电子体的分子的电子式_____ (任写一种)。
(4)CuO在高温时分解为 O2和 Cu2O,请从阳离子的结构来说明在高温时,Cu2O比 CuO更稳定的原因_____ 。
(5)磷青铜是含少量锡、磷的铜合金,某磷青铜晶胞结构如图所示:
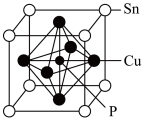
①其化学式为_____ 。
②若晶体密度为 8.82g/cm3,则最近的 Cu原子核间距为_____ pm(用含 NA的代数式表示)。
(1)基态铁原子的价电子轨道表达式为
(2)磁性材料铁氧体在制备时常加入 CH3COONa、尿素[CO(NH2)2]等碱性物质。尿素分子中所含元素的电负性由小到大的顺序是
(3)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则 Fe(CO)5的晶体类型是
(4)CuO在高温时分解为 O2和 Cu2O,请从阳离子的结构来说明在高温时,Cu2O比 CuO更稳定的原因
(5)磷青铜是含少量锡、磷的铜合金,某磷青铜晶胞结构如图所示:

①其化学式为
②若晶体密度为 8.82g/cm3,则最近的 Cu原子核间距为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】元素周期表在化学中有举足轻重的地位。请根据提示回答下列问题:
(1)铁在生活生产中用途广泛,写出 Fe 在元素周期表中的位置_______ 。Fe 分别与硫单质和氯气共热,可以得到两种含铁的二元化合物。请问这两种物质中金属阳离子的未成对电子数之比为_______ 。
(2)古往今来,人类发展的脚步离不开青铜器的冶炼,锻造及使用。如今,铜元素依旧为科研人员所钟爱,请写出铜原子的价电子排布式_______ 。利用铜离子作为中心原子可以形成多种具有良好特性的配合物。我们熟知的是一种深蓝色配合物,向硫酸铜溶液中通入过量氨气,可制备这种深蓝色配合物[Cu(NH3)4]2+。请用适当的化学用语描述该反应过程的实质_______ 。写出[Cu(NH3)4]2+配体的电子式_______ 。
(3)I1表示第一电离,I1(Mg)> I1(Al)> I1(Na),原因是_______ 。
(4)CoO 的晶胞如图所示。
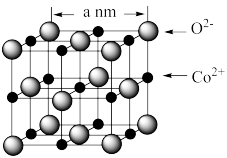
设阿伏加德罗常数的值为 NA,则 CoO 晶体的密度为_______ g﹒cm−3(列出计算式即可)
(5)磷元素在农药的合成中有着重要作用。了解其化合物的结构有助于我们合成新型农药,提高粮食的产量。PO 的 VSEPR 模型为
的 VSEPR 模型为_______ ,其中 P 的杂化轨道类型为_______ 。
(6)配位化学中,硼元素深受研究者的喜爱。其原因在于 B 容易与配体形成配位键,如BF 、B(OH)
、B(OH) 等,从原子结构分析其原因
等,从原子结构分析其原因_______ 。
(7)溶解度、熔沸点、颜色等是每种物质自身特有的性质,但也存在一定的规律。
①水和 H2S 均可以溶于乙醇,但 H2O 在乙醇中的溶解度大于 H2S 的原因_______
a.水和乙醇均为分子晶体 b.水和乙醇分子间可以形成氢键 c.水和乙醇可以发生反应
②比较下列锗卤化物的熔点和沸点,分析其变化规律的原因_______ 。
(1)铁在生活生产中用途广泛,写出 Fe 在元素周期表中的位置
(2)古往今来,人类发展的脚步离不开青铜器的冶炼,锻造及使用。如今,铜元素依旧为科研人员所钟爱,请写出铜原子的价电子排布式
(3)I1表示第一电离,I1(Mg)> I1(Al)> I1(Na),原因是
(4)CoO 的晶胞如图所示。

设阿伏加德罗常数的值为 NA,则 CoO 晶体的密度为
(5)磷元素在农药的合成中有着重要作用。了解其化合物的结构有助于我们合成新型农药,提高粮食的产量。PO
 的 VSEPR 模型为
的 VSEPR 模型为(6)配位化学中,硼元素深受研究者的喜爱。其原因在于 B 容易与配体形成配位键,如BF
 、B(OH)
、B(OH) 等,从原子结构分析其原因
等,从原子结构分析其原因(7)溶解度、熔沸点、颜色等是每种物质自身特有的性质,但也存在一定的规律。
①水和 H2S 均可以溶于乙醇,但 H2O 在乙醇中的溶解度大于 H2S 的原因
a.水和乙醇均为分子晶体 b.水和乙醇分子间可以形成氢键 c.水和乙醇可以发生反应
②比较下列锗卤化物的熔点和沸点,分析其变化规律的原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约 400 |
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】目前半导体生产展开了一场“铜芯片”革命——在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:

回答下列问题:
(1)基态铜原子的电子排布式为___________ ,硫、氧元素相比,第一电离能较小的元素是___________ (填元素符号)。
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是___________ ,其立体结构是___________ 。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液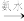 蓝色沉淀
蓝色沉淀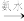 沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式
沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式___________ ;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有___________ 。
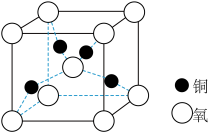
(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为___________ ;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为___________ pm。(用含d和NA的式子表示)。

回答下列问题:
(1)基态铜原子的电子排布式为
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液
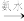 蓝色沉淀
蓝色沉淀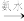 沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式
沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】CuSO4和Cu(NO3)2是自然界中重要的铜盐。请回答下列问题:
(1)CuSO4和Cu(NO3)2中阳离子的核外价电子排布式为_______ ,S、O、N三种元素的第一电离能由大到小的顺序为__________ 。
(2)NO3-的立体构型是_____ ,与NO3-互为等电子体的一种非极性分子为_________ (填化学式)。
(3)CuSO4的熔点为560°C,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是_____ 。
(4)往CuSO4溶液中加入过量NaOH能生成配合物[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为(用箭头表示出配位键的位置)_______ 。
(5)化学实验室常利用新制氢氧化铜检验醛基的存在,乙醛分子中碳原子的杂化方式为___ 。
(6)利用新制的Cu(OH)2检验醛基时,生成红色的Cu2O,其晶胞结构如下图所示。
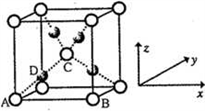
该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为( ,
, ,
, )。则D原子的坐标参数为
)。则D原子的坐标参数为________ ,它代表_______ 原子。
(1)CuSO4和Cu(NO3)2中阳离子的核外价电子排布式为
(2)NO3-的立体构型是
(3)CuSO4的熔点为560°C,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是
(4)往CuSO4溶液中加入过量NaOH能生成配合物[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为(用箭头表示出配位键的位置)
(5)化学实验室常利用新制氢氧化铜检验醛基的存在,乙醛分子中碳原子的杂化方式为
(6)利用新制的Cu(OH)2检验醛基时,生成红色的Cu2O,其晶胞结构如下图所示。

该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为(
 ,
, ,
, )。则D原子的坐标参数为
)。则D原子的坐标参数为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学小组同学利用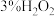 溶液制
溶液制 ,再用
,再用 氧化
氧化 ,并检验氧化产物。
,并检验氧化产物。
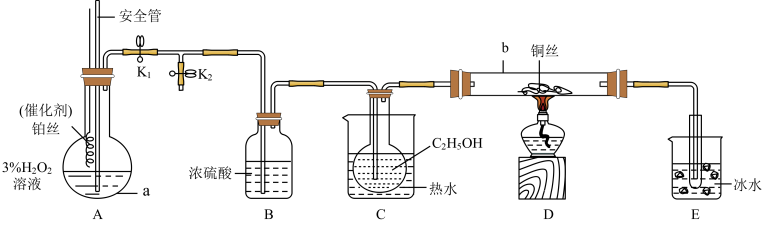
(1)仪器b中发生反应的化学方程式为_______ 。
(2)C和E两个水浴作用不相同,其中E中冰水的作用是_______ 。
(3)为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论。
实验①~③中的结论不合理的是_______ (填序号),原因是_______ 。
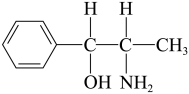
(4)化合物的分子中采取 杂化方式成键的原子数目是
杂化方式成键的原子数目是_______ 个。
(5)氮化钛晶体的晶胞结构如图所示,则氮化钛晶体化学式为_______ ,该晶体结构中与N原子距离最近且相等的N原子有_______ 个;该晶胞的密度 ,则晶胞结构中两个氮原子之间的最近距离为
,则晶胞结构中两个氮原子之间的最近距离为_______ 。(NA为阿伏加德罗常数的数值,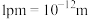 ,只列计算式)。
,只列计算式)。

 溶液制
溶液制 ,再用
,再用 氧化
氧化 ,并检验氧化产物。
,并检验氧化产物。
(1)仪器b中发生反应的化学方程式为
(2)C和E两个水浴作用不相同,其中E中冰水的作用是
(3)为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论。
| 实验序号 | 检验试剂和反应条件 | 现象 | 结论 |
| ① | 酸性 溶液 溶液 | 紫红色褪去 | 产物含有乙醛 |
| ② | 新制 加热 加热 | 生成砖红色沉淀 | 产物含有乙醛 |
| ③ | 微红色含酚酞的NaOH溶液 | 微红色褪去 | 产物可能含有乙酸 |
(4)化合物的分子中采取
 杂化方式成键的原子数目是
杂化方式成键的原子数目是
(5)氮化钛晶体的晶胞结构如图所示,则氮化钛晶体化学式为
 ,则晶胞结构中两个氮原子之间的最近距离为
,则晶胞结构中两个氮原子之间的最近距离为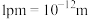 ,只列计算式)。
,只列计算式)。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】元素C与过渡元素Co、Fe、Ni等在工业、农业、科学技术以及人类生活有机合成等方面有重要作用。
(1)基态Co原子价电子轨道排布图为______ ,第四电离能I4(Co)<I4(Fe),其原因是______ 。
(2)(CH3)3C+是有机合成重要中间体,该中间体中碳原子杂化方式为______ 。
(3)Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,其原因是______ 。
(4)Co的一种氧化物的晶胞如图1。已知钴原子的半径为apm,氧原子的半径为bpm,它们在晶体中是紧密接触的,在该钴的氧化物晶胞中原子的空间利用率为______ (列出含a、b的计算表达式即可)(提示:条件不足,无法判断钴原子之间是否紧密接触)。
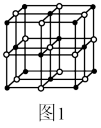
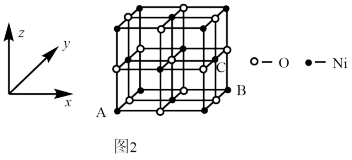
(5)NiO的晶体结构如图2所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为______ 。
(1)基态Co原子价电子轨道排布图为
(2)(CH3)3C+是有机合成重要中间体,该中间体中碳原子杂化方式为
(3)Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,其原因是
(4)Co的一种氧化物的晶胞如图1。已知钴原子的半径为apm,氧原子的半径为bpm,它们在晶体中是紧密接触的,在该钴的氧化物晶胞中原子的空间利用率为

(5)NiO的晶体结构如图2所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为

您最近半年使用:0次



