【化学一选修3: 物质结构与性质】1735年瑞典化学家布兰特(G·Brands)制出金属钴。钴的矿物或钴的化合物一直用作陶瓷、玻璃、珐琅的釉料。到20世纪,钴及其合金在电机、机械、化工、航空和航天等工业部门得到广泛的应用,并成为一种重要的战略金属。所以钴及其化合物具有重要作用,回答下列问题:
(1)基态Co原子的电子排布式为___________ 。
(2)[Co(NH3)5H2O]Cl3是一种砖红色的晶体,可通过CoCl2、NH4Cl、浓氨水、H2O2制得。
①Co、N、0原子的第一电离能由大到小的顺序是__________ 。
②[Co(NH3)5H2O]Cl3中Co元素化合价为____ ,其配位原子为_____ ;1mol该晶体中含有____ molσ键。
③H2O2中O原子的杂化轨道类型是______ ,H2O2能与水互溶,除都是极性分子外,还因为____ 。
④NH3、NF3的空间构型都相同,但Co3+易与NH3形成配离子,而NF3不能。原因是________ 。
(3)CoO晶胞如图,已知Co原子半径为apm,O原子半径为bpm,则等距最近的所有O原子围成的空间形状为_____ ;该晶胞中原子的空间利用率为__________ (用含a、b的计算式表示)。

(1)基态Co原子的电子排布式为
(2)[Co(NH3)5H2O]Cl3是一种砖红色的晶体,可通过CoCl2、NH4Cl、浓氨水、H2O2制得。
①Co、N、0原子的第一电离能由大到小的顺序是
②[Co(NH3)5H2O]Cl3中Co元素化合价为
③H2O2中O原子的杂化轨道类型是
④NH3、NF3的空间构型都相同,但Co3+易与NH3形成配离子,而NF3不能。原因是
(3)CoO晶胞如图,已知Co原子半径为apm,O原子半径为bpm,则等距最近的所有O原子围成的空间形状为

更新时间:2018-07-02 21:25:40
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】I.氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如下图所示。

(1)基态硼原子的电子排布式为____ 。
(2)关于这两种晶体的说法,正确的是____ (填序号)。
a.六方相氮化硼与石墨一样可以导电
b.立方相氮化硼只含有σ键
c.两种晶体均为分子晶体
d.六方相氮化硼晶体层内一个硼原子与相邻氮原子构成平面三角形
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为___ ,其结构与石墨相似却不导电,原因是___ 。
II.有一种氮化硼晶体的结构与金刚石相似,其晶胞如图所示。

(1)在一个晶胞中,含有硼原子___ 个,氮原子___ 个。
(2)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。已知三个原子分数坐标参数:A为(0,0,0)、B为(0,1,1)、C为(1,1,0);则E原子为___ 。
(3)氮化硼晶胞的俯视投影图是___ 。

(4)已知氮化硼晶胞为ρg•cm-3,设NA为阿伏加德罗常数的值,则氮化硼晶胞的棱长为___ cm(用代数式表示)。

(1)基态硼原子的电子排布式为
(2)关于这两种晶体的说法,正确的是
a.六方相氮化硼与石墨一样可以导电
b.立方相氮化硼只含有σ键
c.两种晶体均为分子晶体
d.六方相氮化硼晶体层内一个硼原子与相邻氮原子构成平面三角形
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为
II.有一种氮化硼晶体的结构与金刚石相似,其晶胞如图所示。

(1)在一个晶胞中,含有硼原子
(2)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。已知三个原子分数坐标参数:A为(0,0,0)、B为(0,1,1)、C为(1,1,0);则E原子为
(3)氮化硼晶胞的俯视投影图是

(4)已知氮化硼晶胞为ρg•cm-3,设NA为阿伏加德罗常数的值,则氮化硼晶胞的棱长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铜及其化合物应用广泛。请回答下列问题:
(1)铜原子价层电子排布式为___________
(2)钾和铜都是第四周期元素,且原子的最外层电子数相同,铜的熔沸点远大于钾的原因是___________ 。
(3)在高温下,Cu2O比CuO稳定,从离子的电子层结构角度分析,其主要原因是___________
(4)CuSO4·5H2O结构示意图如下,
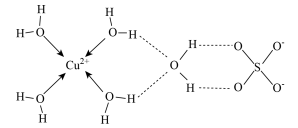
①CuSO4·5H2O中不存在的相互作用有___________ (填序号,下同)。加热该蓝色胆矾晶体得到白色硫酸铜固体破坏的相互作用有___________ 。
A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键
②硫酸铜中SO 的空间构型为
的空间构型为___________ ,其中心原子的杂化类型是___________ 。
(5)铜镍合金的立方晶胞结构如图所示:

若该晶体密度为dg·cm-3,则铜镍原子间最短距离为___________ pm。
(1)铜原子价层电子排布式为
(2)钾和铜都是第四周期元素,且原子的最外层电子数相同,铜的熔沸点远大于钾的原因是
(3)在高温下,Cu2O比CuO稳定,从离子的电子层结构角度分析,其主要原因是
(4)CuSO4·5H2O结构示意图如下,

①CuSO4·5H2O中不存在的相互作用有
A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键
②硫酸铜中SO
 的空间构型为
的空间构型为(5)铜镍合金的立方晶胞结构如图所示:

若该晶体密度为dg·cm-3,则铜镍原子间最短距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】我国的航空航天事业取得了举世瞩目的成就,近年来硼氢类离子液体作为火箭推进剂燃料得到了广泛使用,该火箭推进剂具有点火延迟时间、宽液程和极低的蒸汽压等优点。硼氢类离子液体的合成如图所示:

回答下列问题:
(1)基态Ba原子的价层电子排布式为___________ ,其N层具有的电子数是___________ 。
(2)C、O、N的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)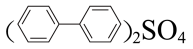 中碳原子的杂化方式为
中碳原子的杂化方式为___________ ; 的空间构型为
的空间构型为___________ 形。
(4) 中不存在的作用力有
中不存在的作用力有___________ (填字母)。
a.离子键 b.配位键 c. 键 d.
键 d. 键 e.金属键
键 e.金属键
(5)多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成大 键。大
键。大 键可用
键可用 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的原子个数和电子数,则
键的原子个数和电子数,则 的大
的大 键可表示为
键可表示为___________ 。
(6)硼化钙晶胞结构如图所示,B原子构成B6八面体,各个顶点通过B—B键互相连接成三维骨架,八个B6多面体围成立方体,中心为Ca2+,晶胞密度为 。
。
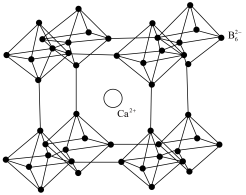
①硼化钙的化学式为___________ 。
②晶胞边长为___________ nm(已知 为阿伏加德罗常数)。
为阿伏加德罗常数)。

回答下列问题:
(1)基态Ba原子的价层电子排布式为
(2)C、O、N的第一电离能由大到小的顺序为
(3)
 中碳原子的杂化方式为
中碳原子的杂化方式为 的空间构型为
的空间构型为(4)
 中不存在的作用力有
中不存在的作用力有a.离子键 b.配位键 c.
 键 d.
键 d. 键 e.金属键
键 e.金属键(5)多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成大
 键。大
键。大 键可用
键可用 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的原子个数和电子数,则
键的原子个数和电子数,则 的大
的大 键可表示为
键可表示为(6)硼化钙晶胞结构如图所示,B原子构成B6八面体,各个顶点通过B—B键互相连接成三维骨架,八个B6多面体围成立方体,中心为Ca2+,晶胞密度为
 。
。
①硼化钙的化学式为
②晶胞边长为
 为阿伏加德罗常数)。
为阿伏加德罗常数)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】I.快离子导体是一类具有优良离子导电能力的固体电解质,研究得最多的是Ag、Cu、Li、Na、F、O等的快离子导体。
(1)Cu-e-=Cu+的过程中,失去的电子是基态Cu中_____ 轨道上的电子。
(2)N、O、F的第一电离能从小到大的顺序为______ (用元素符号表示);NH3、H2O、HF的沸点由低到高的顺序为_____ (用化学式表示,下同),其中NH3、H2O的键角由小到大的顺序为_____ 。
(3)二乙二胺合铜配离子{[Cu(H2NCH2CH2NH2)2]2+}的结构如图,1mol该配合物中所含的配位键为____ mol。

II.碳及其化合物广泛存在于自然界中,回答下列问题:
(4)基态碳原子的价电子轨道表示式是______ 。
a.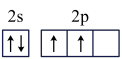 b.
b.
请阐述其原因是______ 。处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_____ 形象地描述。在基态14C原子中,核外存在_____ 对自旋相反的电子。
(5)碳在形成化合物时,其键型以共价键为主,原因是______ 。写出两个与CS2互为等电子体的分子或离子______ 。
(6)甲醚(CH3OCH3)中氧原子的杂化方式为______ ,甲醚的沸点比乙醇(CH3CH2OH)的沸点_____ 。
(1)Cu-e-=Cu+的过程中,失去的电子是基态Cu中
(2)N、O、F的第一电离能从小到大的顺序为
(3)二乙二胺合铜配离子{[Cu(H2NCH2CH2NH2)2]2+}的结构如图,1mol该配合物中所含的配位键为

II.碳及其化合物广泛存在于自然界中,回答下列问题:
(4)基态碳原子的价电子轨道表示式是
a.
 b.
b.
请阐述其原因是
(5)碳在形成化合物时,其键型以共价键为主,原因是
(6)甲醚(CH3OCH3)中氧原子的杂化方式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】我国科学家利用Cs2CO3、XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7的非线性光学晶体。回答下列问题:
(1)C、O、Si三种元素电负性由大到小的顺序为___________ ;第一电离能I1(Si)___________ I1(Ge)(填“>”或“<”)。
(2)基态Ge原子价电子排布式为___________ ;SiO2、GeO2具有类似的晶体结构,SiO2熔点较高,其原因是___________
(3)如图为硼酸晶体的片层结构,其中硼原子的杂化方式为___________ 。该晶体中存在的作用力有___________ 。
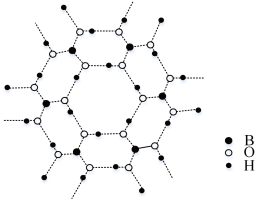
A.共价键B.离子键C.氢键
(4)Fe和Cu可分别与氧元素形成低价态氧化物FeO和Cu2O。
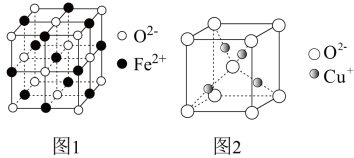
①FeO立方晶胞结构如图1所示,则Fe2+的配位数为___________ 。
②Cu2O立方晶胞结构如图2所示,若晶胞边长为acm,则该晶体的密度为___________ g·cm-3。(用含a、NA的代数式表示,NA代表阿伏加 德罗常数)
(1)C、O、Si三种元素电负性由大到小的顺序为
(2)基态Ge原子价电子排布式为
(3)如图为硼酸晶体的片层结构,其中硼原子的杂化方式为

A.共价键B.离子键C.氢键
(4)Fe和Cu可分别与氧元素形成低价态氧化物FeO和Cu2O。

①FeO立方晶胞结构如图1所示,则Fe2+的配位数为
②Cu2O立方晶胞结构如图2所示,若晶胞边长为acm,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】前四周期A、B、C、D、E、F、G原子序数依次增大,A元素的质子数和质量数相等,B元素具有三个能级且所排电子数相同,D元素2p能级上电子数是2s能级的两倍;D和E相邻且同主族.F是第四周期未成对电子最多的原子,G是目前使用量最多的金属。
请回答下列问题: 用推出的元素符号或者化学式作答
用推出的元素符号或者化学式作答
(1)F的价电子排布式为__ ,B、C、D三种元素的第一电离能从大到小的顺序为___ ,D和E电负性较大的是__ 。
(2)BD32-中B原子的杂化方式为__ ,该离子的空间构型为__ ,键角为___ 。
(3)写出一种由A、C、D组成且既含离子键又含共价键的物质的化学式__ ,化合物ABC中σ键和π键数目之比为___ ,C的气态氢化物在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因__ 。
(4)B和C的最高价含氧酸的酸性较强的是___ ,过量的G与C的最高价含氧酸稀溶液反应的离子方程式为__ 。
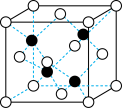
(5)E和G形成的某种晶胞如图所示:其中白球表示E,黑球表示G。则该物质的化学式为___ ,假设该晶胞的密度为ρg/cm3,用NA表示阿伏加 德罗常数,则该晶胞中距离最近的G原子之间的距离为___ cm。
请回答下列问题:
 用推出的元素符号或者化学式作答
用推出的元素符号或者化学式作答
(1)F的价电子排布式为
(2)BD32-中B原子的杂化方式为
(3)写出一种由A、C、D组成且既含离子键又含共价键的物质的化学式
(4)B和C的最高价含氧酸的酸性较强的是
(5)E和G形成的某种晶胞如图所示:其中白球表示E,黑球表示G。则该物质的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】铁元素在地壳中含量丰富,应用广泛:回答以下问题:
(1)基态Fe的价电子排布式为_______ ,其中未成对电子数目为_______ 。
(2)水溶液中 发生水解,水解过程中出现双核阳离子
发生水解,水解过程中出现双核阳离子 。
。

①该双核阳离子中, 原子的配位数为
原子的配位数为_______ ,配体 的空间构型为
的空间构型为_______ ,其键角_______ 109°28′ (填“大于”、“小于”或“等于”)。
②用 可检验溶液中
可检验溶液中 的存在,l mol中
的存在,l mol中 中含有的π键数目为
中含有的π键数目为_______ NA。
(3)铁的氧化物有多种,科研工作者常使用 来表示各种铁氧化物。如图为某种铁的氧化物样品的晶胞结构,其化学式为
来表示各种铁氧化物。如图为某种铁的氧化物样品的晶胞结构,其化学式为_______ 。

(1)基态Fe的价电子排布式为
(2)水溶液中
 发生水解,水解过程中出现双核阳离子
发生水解,水解过程中出现双核阳离子 。
。
①该双核阳离子中,
 原子的配位数为
原子的配位数为 的空间构型为
的空间构型为②用
 可检验溶液中
可检验溶液中 的存在,l mol中
的存在,l mol中 中含有的π键数目为
中含有的π键数目为(3)铁的氧化物有多种,科研工作者常使用
 来表示各种铁氧化物。如图为某种铁的氧化物样品的晶胞结构,其化学式为
来表示各种铁氧化物。如图为某种铁的氧化物样品的晶胞结构,其化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)写出元素符号A:_______ ,B:_______ ,E_______ ,G:_______ 。
(2)C、D、E三种元素的原子半径由大到小的顺序为_______ (用元素符号表示)。
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:_______ ,_______ ,_______ 。
(4)已知元素A、B形成的 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为_______ 。
(5)G元素可形成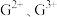 ,其中较稳定的是
,其中较稳定的是 ,试从核外电子排布的角度解释其原因:
,试从核外电子排布的角度解释其原因:_______ 。
(6)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是_______ 化合物(填“离子”或“共价”)。根据“对角线规则”,元素周期表中某些处于对角的元素,它们的化合物性质具有相似性,则M的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为_______ 。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 电离能数据(单位: ):738、1451、7733、10540、13630…… ):738、1451、7733、10540、13630…… |
| E | 基态原子最外层电子排布式为: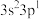 |
| F | 基态原子的最外层p轨道上2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 其中一种氧化物是有磁性的黑色固体 |
(2)C、D、E三种元素的原子半径由大到小的顺序为
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:
(4)已知元素A、B形成的
 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为(5)G元素可形成
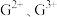 ,其中较稳定的是
,其中较稳定的是 ,试从核外电子排布的角度解释其原因:
,试从核外电子排布的角度解释其原因:(6)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氮元素可以形成多种化合物。回答以下问题:
(1)基态氮原子的价电子排布式是___________ 。
(2)C、N、O三种元素第一电离能从大到小的是___________ 。
(3)肼(N2H4)分子可视为NH3 分子中的一个氢原子被﹣NH2(氨基)取代形成的另一种氮化物。NH3 分子的空间构型是___________ ;N2H4分子中氮原子轨道的杂化类型是___________ 。
(4)肼可用作火箭燃料,燃烧时发生的反应是: 若该反应中有4mol N﹣H键断裂,则形成的π键有
若该反应中有4mol N﹣H键断裂,则形成的π键有___________ mol。
(1)基态氮原子的价电子排布式是
(2)C、N、O三种元素第一电离能从大到小的是
(3)肼(N2H4)分子可视为NH3 分子中的一个氢原子被﹣NH2(氨基)取代形成的另一种氮化物。NH3 分子的空间构型是
(4)肼可用作火箭燃料,燃烧时发生的反应是:
 若该反应中有4mol N﹣H键断裂,则形成的π键有
若该反应中有4mol N﹣H键断裂,则形成的π键有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】钼酸铋作为新型半导体光催化材料,广泛应用于生产生活中。以氧化铋渣(主要成分是Bi2O3、Sb2O3、还含有Fe2O3、ZnO、Ag2O和SiO2等杂质)为原料制备钼酸铋(Bi2MoO6,其中Mo为+6价)的工艺流程如下:

回答下列问题:
(1)基态S的价电子排布式为___________ 。
(2)“浸渣”的主要成分为___________ (填化学式)。
(3)①“除锑”过程中发生反应的化学方程式为___________ ;
②该过程需要加热的原因为___________ 。
(4)H2S常温下为气体,而H2O常温下为液体的原因为___________ 。
(5)“酸溶”时会有NO逸出,此过程中氧化剂与还原剂的物质的量之比为___________ 。
(6)Bi2O3的立方晶胞结构如图所示(O占据部分Bi的四面体空隙),以A点为原点建立分数坐标,已知A点坐标为(0,0,0),B点坐标为( ,
, ,
, ),则C点坐标为
),则C点坐标为___________ 。晶胞边长为anm,则密度为___________ g·cm-3(Bi2O3的摩尔质量为Mr,阿伏加德罗常数为NA)


回答下列问题:
(1)基态S的价电子排布式为
(2)“浸渣”的主要成分为
(3)①“除锑”过程中发生反应的化学方程式为
②该过程需要加热的原因为
(4)H2S常温下为气体,而H2O常温下为液体的原因为
(5)“酸溶”时会有NO逸出,此过程中氧化剂与还原剂的物质的量之比为
(6)Bi2O3的立方晶胞结构如图所示(O占据部分Bi的四面体空隙),以A点为原点建立分数坐标,已知A点坐标为(0,0,0),B点坐标为(
 ,
, ,
, ),则C点坐标为
),则C点坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】磷锡青铜(一种磷、锡、铜合金)是有名的弹性材料,广泛应用于仪器仪表中耐磨零件和弹性元件。回答下列问题:
(1)白磷(P4)晶体熔点44.1℃、沸点280℃,质软,则白磷属于___________ 晶体(写“分子”、“共价”、“离子”)。
(2)Cu2+与NH3能形成的配离子为___________ (写化学式),该配离子水溶液的颜色为___________ 。该配离子具有对称的空间构型,若其中两个NH3被两个Cl-取代,能得到两种不同结构的产物,则该配离子的空间构型为___________ (填“正四面体”、“平面正方形”)。
(3)PO 中P原子的杂化方式为
中P原子的杂化方式为___________ 杂化,PO 的空间构型为
的空间构型为___________ 。
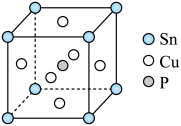
(4)磷锡青铜的立方晶胞结构如图所示,则该晶体的化学式为___________ 。
(1)白磷(P4)晶体熔点44.1℃、沸点280℃,质软,则白磷属于
(2)Cu2+与NH3能形成的配离子为
(3)PO
 中P原子的杂化方式为
中P原子的杂化方式为 的空间构型为
的空间构型为(4)磷锡青铜的立方晶胞结构如图所示,则该晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】我国科学家创造了一种用于卫星的世界最纯的砷化镓样品。第IIIA和VA族元素可组成多种半导体材料。回答下列问题:
(1)基态砷原子电子排布简式为[Ar]_______ 。
(2)砷与硒、溴位于同周期,第一电离能由大到小排序为_______ (填元素符号)。
(3)硼、铝、镓位于同主族,电负性由小到大排序为_______ (填元素符号)。 、
、 都是有机合成的重要还原剂,
都是有机合成的重要还原剂, 中B的杂化轨道类型是
中B的杂化轨道类型是_______ , 的空间构型是
的空间构型是_______ 。
(4)1 mol 含
含_______ mol配位键。
(5)镓的一种氧化物晶胞如图1所示, 以六方最密方式堆积,
以六方最密方式堆积, 在其八面体空隙中(注:未全部标出,如:
在其八面体空隙中(注:未全部标出,如: 在1、2、3、4、5、6构成的八面体心)。该氧化物的化学式为
在1、2、3、4、5、6构成的八面体心)。该氧化物的化学式为_______ ;在该晶胞中 的配位数为
的配位数为_______ 。该晶胞中正八面体空隙中阳离子填充率为_______ (用分数表示)。

(6)砷化镓晶胞如图2所示,砷化镓的熔点为1238℃,它的晶体类型是_______ 。已知砷化镓晶体密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。x和y原子键长为
。x和y原子键长为_______ nm。

(1)基态砷原子电子排布简式为[Ar]
(2)砷与硒、溴位于同周期,第一电离能由大到小排序为
(3)硼、铝、镓位于同主族,电负性由小到大排序为
 、
、 都是有机合成的重要还原剂,
都是有机合成的重要还原剂, 中B的杂化轨道类型是
中B的杂化轨道类型是 的空间构型是
的空间构型是(4)1 mol
 含
含(5)镓的一种氧化物晶胞如图1所示,
 以六方最密方式堆积,
以六方最密方式堆积, 在其八面体空隙中(注:未全部标出,如:
在其八面体空隙中(注:未全部标出,如: 在1、2、3、4、5、6构成的八面体心)。该氧化物的化学式为
在1、2、3、4、5、6构成的八面体心)。该氧化物的化学式为 的配位数为
的配位数为
(6)砷化镓晶胞如图2所示,砷化镓的熔点为1238℃,它的晶体类型是
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。x和y原子键长为
。x和y原子键长为
您最近一年使用:0次



