铁元素在地壳中含量丰富,应用广泛:回答以下问题:
(1)基态Fe的价电子排布式为_______ ,其中未成对电子数目为_______ 。
(2)水溶液中 发生水解,水解过程中出现双核阳离子
发生水解,水解过程中出现双核阳离子 。
。

①该双核阳离子中, 原子的配位数为
原子的配位数为_______ ,配体 的空间构型为
的空间构型为_______ ,其键角_______ 109°28′ (填“大于”、“小于”或“等于”)。
②用 可检验溶液中
可检验溶液中 的存在,l mol中
的存在,l mol中 中含有的π键数目为
中含有的π键数目为_______ NA。
(3)铁的氧化物有多种,科研工作者常使用 来表示各种铁氧化物。如图为某种铁的氧化物样品的晶胞结构,其化学式为
来表示各种铁氧化物。如图为某种铁的氧化物样品的晶胞结构,其化学式为_______ 。

(1)基态Fe的价电子排布式为
(2)水溶液中
 发生水解,水解过程中出现双核阳离子
发生水解,水解过程中出现双核阳离子 。
。
①该双核阳离子中,
 原子的配位数为
原子的配位数为 的空间构型为
的空间构型为②用
 可检验溶液中
可检验溶液中 的存在,l mol中
的存在,l mol中 中含有的π键数目为
中含有的π键数目为(3)铁的氧化物有多种,科研工作者常使用
 来表示各种铁氧化物。如图为某种铁的氧化物样品的晶胞结构,其化学式为
来表示各种铁氧化物。如图为某种铁的氧化物样品的晶胞结构,其化学式为
更新时间:2022-04-12 12:16:04
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】硅及其化合物在生活生产中广泛应用。请按要求回答下列问题。
(1)基态硅原子的电子排布式为_______ ;Si原子间难形成双键而C原子间却可以形成,是因为Si的原子半径_______ (填“大于”或“小于”)C的,两个Si原子的p电子难于重叠形成π键。
(2)工业上制备高纯硅的示意图如下:

①步骤Ⅰ反应所涉及元素的第一电离能由大到小的顺序是(填元素符号)_______ 。根据下图所示物质反应过程中的能量变化,写出用石英砂和焦炭制取粗硅,同时生成CO的热化学方程式:_______ 。

②步骤Ⅱ产物中含有 (沸点为33.0℃),还有少量
(沸点为33.0℃),还有少量 (沸点为57.6℃)和HCl(沸点为-84.7℃)。若先将步骤Ⅱ产物降至室温,提纯
(沸点为57.6℃)和HCl(沸点为-84.7℃)。若先将步骤Ⅱ产物降至室温,提纯 ,方法是
,方法是_______ 。所用到的玻璃仪器除酒精灯、温度计、锥形瓶、尾接管外,还需要_______ 、_______ 。
(3)已知:硅的最高价氧化物对应的水化物有 和原硅酸(
和原硅酸( )。常温下,
)。常温下, :
: 、
、 ;
; :
: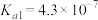 、
、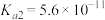
①向盛有饱和 溶液(滴有酚酞溶液)的试管中通入过量
溶液(滴有酚酞溶液)的试管中通入过量 ;充分反应后,用激光笔照射上述液体时发现有光亮的通路。预测液体颜色的变化:
;充分反应后,用激光笔照射上述液体时发现有光亮的通路。预测液体颜色的变化:_______ ;写出该反应的离子方程式:_______ 。
②写出原硅酸脱水得到的产物(写两种)_______ 、_______ 。
(1)基态硅原子的电子排布式为
(2)工业上制备高纯硅的示意图如下:

①步骤Ⅰ反应所涉及元素的第一电离能由大到小的顺序是(填元素符号)

②步骤Ⅱ产物中含有
 (沸点为33.0℃),还有少量
(沸点为33.0℃),还有少量 (沸点为57.6℃)和HCl(沸点为-84.7℃)。若先将步骤Ⅱ产物降至室温,提纯
(沸点为57.6℃)和HCl(沸点为-84.7℃)。若先将步骤Ⅱ产物降至室温,提纯 ,方法是
,方法是(3)已知:硅的最高价氧化物对应的水化物有
 和原硅酸(
和原硅酸( )。常温下,
)。常温下, :
: 、
、 ;
; :
: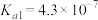 、
、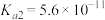
①向盛有饱和
 溶液(滴有酚酞溶液)的试管中通入过量
溶液(滴有酚酞溶液)的试管中通入过量 ;充分反应后,用激光笔照射上述液体时发现有光亮的通路。预测液体颜色的变化:
;充分反应后,用激光笔照射上述液体时发现有光亮的通路。预测液体颜色的变化:②写出原硅酸脱水得到的产物(写两种)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】开发新型材料是现在科学研究的一项重要工作,科学家开发一种形状记忆陶瓷,它的主要原材料是纳米级 。用锆石
。用锆石 (含少量
(含少量 、
、 、
、 和
和 )制备纳米级
)制备纳米级 的流程设计如图:
的流程设计如图:

回答下列问题:
(1)锆石杂质中含铁元素,则基态Fe的价电子排布式为________ , 易被氧化为
易被氧化为 的原因是
的原因是________ 。(从原子结构角度解释)
(2)为提高碱熔率,可采取的措施是________ (至少写出两种)。
(3)“酸浸”过程中 发生氧化还原反应的离子方程式为
发生氧化还原反应的离子方程式为________ ,滤渣2的主要成分是________ 。
(4)“除铜”过程中,若要完全除掉 ,溶液中
,溶液中 的浓度至少为
的浓度至少为________ mol/L。(已知常温下 )
)
(5)“酸浸”时,得到的溶质主要是 ,而不是
,而不是 ,是因为
,是因为 很容易水解,则
很容易水解,则 水解的化学方程式是
水解的化学方程式是________ 。
(6)若锆石中含有 的质量分数是73.2%,在制备
的质量分数是73.2%,在制备 的过程中损失10%的锆元素,则1kg锆石理论上能够制得
的过程中损失10%的锆元素,则1kg锆石理论上能够制得 的质量是
的质量是________ g。
 。用锆石
。用锆石 (含少量
(含少量 、
、 、
、 和
和 )制备纳米级
)制备纳米级 的流程设计如图:
的流程设计如图:
回答下列问题:
(1)锆石杂质中含铁元素,则基态Fe的价电子排布式为
 易被氧化为
易被氧化为 的原因是
的原因是(2)为提高碱熔率,可采取的措施是
(3)“酸浸”过程中
 发生氧化还原反应的离子方程式为
发生氧化还原反应的离子方程式为(4)“除铜”过程中,若要完全除掉
 ,溶液中
,溶液中 的浓度至少为
的浓度至少为 )
)(5)“酸浸”时,得到的溶质主要是
 ,而不是
,而不是 ,是因为
,是因为 很容易水解,则
很容易水解,则 水解的化学方程式是
水解的化学方程式是(6)若锆石中含有
 的质量分数是73.2%,在制备
的质量分数是73.2%,在制备 的过程中损失10%的锆元素,则1kg锆石理论上能够制得
的过程中损失10%的锆元素,则1kg锆石理论上能够制得 的质量是
的质量是
您最近一年使用:0次
【推荐3】许多金属及其化合物在生活、化工、医药、材料等各个领域有着广泛的应用。
(1)钛由于其稳定的化学性质,良好的耐高温、耐低温、抗强酸、抗强碱以及高强度、低密度,被美誉为“未来钢铁”“战略金属”。钛基态原子中电子占据最高能级的符号为___________ 。与钛同周期的元素中,基态原子的未成对电子数与钛相同的有___________ 种。钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是___________ 。
(2)Fe3+可以与SCN-、CN-、有机分子等形成配合物。基态Fe3+的核外电子排布式为___________ ;与CN-互为等电子体且为非极性分子的化学式为___________ 。
(3)化合物FeCl3是棕色固体、易潮解、 左右时升华,它的晶体类型是
左右时升华,它的晶体类型是___________ 。
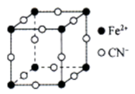
(4)普鲁士蓝俗称铁蓝,结构如图所示( 未画出),平均每两个立方体中含有一个K+,该晶体的化学式为
未画出),平均每两个立方体中含有一个K+,该晶体的化学式为___________ 。又知该晶体中铁元素有+2价和+3价两种,则Fe3+与Fe2+的个数比为___________ 。

(1)钛由于其稳定的化学性质,良好的耐高温、耐低温、抗强酸、抗强碱以及高强度、低密度,被美誉为“未来钢铁”“战略金属”。钛基态原子中电子占据最高能级的符号为
(2)Fe3+可以与SCN-、CN-、有机分子等形成配合物。基态Fe3+的核外电子排布式为
(3)化合物FeCl3是棕色固体、易潮解、
 左右时升华,它的晶体类型是
左右时升华,它的晶体类型是(4)普鲁士蓝俗称铁蓝,结构如图所示(
 未画出),平均每两个立方体中含有一个K+,该晶体的化学式为
未画出),平均每两个立方体中含有一个K+,该晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)写出CO 的VSEPR模型名称
的VSEPR模型名称___________ ;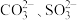 的中心原子上的孤电子对数分别是
的中心原子上的孤电子对数分别是___________ 、___________ 。
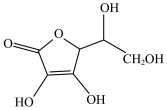
(2)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为___________ ;1mol该分子中π键数为___________ 。
(3)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示,富马酸分子中 键与
键与 键的数目比为
键的数目比为___________ 。

(4)已知,可用异氰酸苯酯与2—氯—4—氨基吡啶反应生成氯吡苯脲:

反应过程中,每生成 氯吡苯脲,断裂
氯吡苯脲,断裂___________  键,断裂
键,断裂___________ 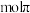 键;已知该2—氯—4—氨基分子中六元环结构与苯环相似,也存在大π键,可表示为
键;已知该2—氯—4—氨基分子中六元环结构与苯环相似,也存在大π键,可表示为___________ (写成π 的形式)
的形式)
(5)N2H 的电子式为
的电子式为___________ ,CH3NH 中N原子的
中N原子的___________ 杂化轨道与H的1s轨道形成σ键;CH3NH 中H-N-H键角比NH3中H-N-H键角
中H-N-H键角比NH3中H-N-H键角___________ (填“大”或“小”),理由是___________ 。
(1)写出CO
 的VSEPR模型名称
的VSEPR模型名称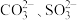 的中心原子上的孤电子对数分别是
的中心原子上的孤电子对数分别是(2)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为

(3)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示,富马酸分子中
 键与
键与 键的数目比为
键的数目比为
(4)已知,可用异氰酸苯酯与2—氯—4—氨基吡啶反应生成氯吡苯脲:

反应过程中,每生成
 氯吡苯脲,断裂
氯吡苯脲,断裂 键,断裂
键,断裂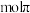 键;已知该2—氯—4—氨基分子中六元环结构与苯环相似,也存在大π键,可表示为
键;已知该2—氯—4—氨基分子中六元环结构与苯环相似,也存在大π键,可表示为 的形式)
的形式)(5)N2H
 的电子式为
的电子式为 中N原子的
中N原子的 中H-N-H键角比NH3中H-N-H键角
中H-N-H键角比NH3中H-N-H键角
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】亚铁氰化钾属于批准使用的食品添加剂,受热易分解:3K4[Fe(CN)6] 12KCN+Fe3C+2(CN)2↑+N2↑+C,回答下列问题:
12KCN+Fe3C+2(CN)2↑+N2↑+C,回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为_______ 。
(2)常温常压下CCl4为无色液体,CCl4空间构型为_______ ,它属于_______ 晶体。
(3)NH3、PH3、AsH3的沸点由高到低的顺序为_______ (填化学式)。
(4)(CN)2分子中σ键和π键数目比为_______ 。
(5)H、C、N三种元素的电负性由大到小的顺序为_____ 。三种元素组成的化合物HCN分子中碳原子的轨道杂化类型为_____ 。
 12KCN+Fe3C+2(CN)2↑+N2↑+C,回答下列问题:
12KCN+Fe3C+2(CN)2↑+N2↑+C,回答下列问题:(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)常温常压下CCl4为无色液体,CCl4空间构型为
(3)NH3、PH3、AsH3的沸点由高到低的顺序为
(4)(CN)2分子中σ键和π键数目比为
(5)H、C、N三种元素的电负性由大到小的顺序为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】(1)A、B、C为同一短周期金属元素。依据下表数据分析,A、B、C三种元素的离子半径由大到小的顺序是_____ 。(用离子符号表示)
(2)已知H2O2分子的空间结构如图所示,H2O2分子中氧原子采取____________ 杂化;H2O2分子是______ (填“极性分子”或“非极性分子”)。

(3)R是第4周期元素中未成对电子数最多的原子。R3+在溶液中存在如下转化:
R3+ R(OH)3
R(OH)3 [R(OH)4]-
[R(OH)4]-
①基态R原子的价电子排布式为_____ 。
②[R(OH)4]-中存在的化学键是_____ ;1mol[R(OH)4]-离子中含有σ键的数目为_______ mol。
A.离子键 B.极性键 C.非极性键D .配位键
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 500 | 4600 | 6900 | 9500 |
| B | 740 | 1500 | 7700 | 10500 |
| C | 580 | 1800 | 2700 | 11600 |
(2)已知H2O2分子的空间结构如图所示,H2O2分子中氧原子采取

(3)R是第4周期元素中未成对电子数最多的原子。R3+在溶液中存在如下转化:
R3+
 R(OH)3
R(OH)3 [R(OH)4]-
[R(OH)4]-①基态R原子的价电子排布式为
②[R(OH)4]-中存在的化学键是
A.离子键 B.极性键 C.非极性键D .配位键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】钴的合金及其配合物用途非常广泛。已知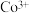 比
比 的氧化性更强,在水溶液中不能大量存在.
的氧化性更强,在水溶液中不能大量存在.
(1)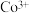 的核外电子排布式为
的核外电子排布式为_____________ 。
(2)无水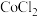 的熔点为
的熔点为 、沸点为
、沸点为 ,
, 熔点为
熔点为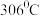 、沸点为
、沸点为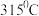 .
.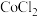 属于
属于_______ 晶体, 属于
属于_____ 晶体。
(3) 可用于激光起爆器等,可由
可用于激光起爆器等,可由 、
、 、
、 共反应制备.
共反应制备.
① 的空间构型为
的空间构型为______________________ 。
② 的化学式为
的化学式为 ,与
,与 (III)形成配位键的原子是
(III)形成配位键的原子是_____
已知 的结构式是
的结构式是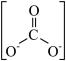
③ 可以
可以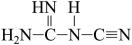 (双聚氰胺)为原料制备,
(双聚氰胺)为原料制备, 双聚氯胺分子中含
双聚氯胺分子中含 键的数目为
键的数目为___________ 。
(4) 与
与 作用可生成
作用可生成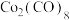 ,其结构如图所示,该分子中
,其结构如图所示,该分子中 原子的杂化方式为
原子的杂化方式为_____________________________ 。

(5)钴酸锂是常见锂电池的电极材料,其晶胞结构如图所示。该晶胞中氧原子的数目为______ 。已知 为阿伏伽德罗常数的数值,则该晶胞的密度为
为阿伏伽德罗常数的数值,则该晶胞的密度为______ (用含 、
、 、
、 的代数式表示)
的代数式表示)
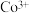 比
比 的氧化性更强,在水溶液中不能大量存在.
的氧化性更强,在水溶液中不能大量存在.(1)
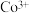 的核外电子排布式为
的核外电子排布式为(2)无水
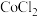 的熔点为
的熔点为 、沸点为
、沸点为 ,
, 熔点为
熔点为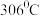 、沸点为
、沸点为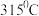 .
.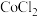 属于
属于 属于
属于(3)
 可用于激光起爆器等,可由
可用于激光起爆器等,可由 、
、 、
、 共反应制备.
共反应制备.①
 的空间构型为
的空间构型为②
 的化学式为
的化学式为 ,与
,与 (III)形成配位键的原子是
(III)形成配位键的原子是已知
 的结构式是
的结构式是
③
 可以
可以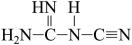 (双聚氰胺)为原料制备,
(双聚氰胺)为原料制备, 双聚氯胺分子中含
双聚氯胺分子中含 键的数目为
键的数目为(4)
 与
与 作用可生成
作用可生成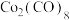 ,其结构如图所示,该分子中
,其结构如图所示,该分子中 原子的杂化方式为
原子的杂化方式为
(5)钴酸锂是常见锂电池的电极材料,其晶胞结构如图所示。该晶胞中氧原子的数目为
 为阿伏伽德罗常数的数值,则该晶胞的密度为
为阿伏伽德罗常数的数值,则该晶胞的密度为 、
、 、
、 的代数式表示)
的代数式表示)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
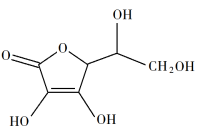
【推荐2】Cu2O广泛应用于太阳能电池。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。
(1)Cu2+基态核外电子排布式为_______ 。
(2)Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的存在的化学键_______。
(3)抗坏血酸的分子结构如图所示,其中碳原子的杂化轨道类型是_______ 。_______ 。_______ g/cm3(只列出计算表达式)
(1)Cu2+基态核外电子排布式为
(2)Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的存在的化学键_______。
| A.离子键 | B.极性共价键 | C.配位键 | D.氢键 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)基态Si原子中存在___________ 种不同能量的电子。
(2)基态Ge原子核外有___________ 种不同空间运动状态的电子。
(3)Si为重要的半导体材料,硅与NaOH溶液反应生成Na2SiO3溶液,该溶液中四种元素电负性由小到大的顺序为___________ 。硅酸盐中的硅酸根离子通常以[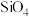 ]四面体(如图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,写出其化学式:
]四面体(如图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,写出其化学式:___________ 。

(4)实验中常用K3[Fe(CN)6]检验Fe2+,K3[Fe(CN)6]中Fe3+的配位数为___________ ,其中碳原子的杂化轨道类型为___________ 。1 mol K3[Fe(CN)6]中含有σ键与π键的数目之比为___________ 。
(5)灰锡的晶体结构(如图3所示)与金刚石相似,其中A处原子的原子分数坐标为(0,0,0),则B处原子的原子分数坐标为___________ 。

(1)基态Si原子中存在
(2)基态Ge原子核外有
(3)Si为重要的半导体材料,硅与NaOH溶液反应生成Na2SiO3溶液,该溶液中四种元素电负性由小到大的顺序为
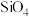 ]四面体(如图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,写出其化学式:
]四面体(如图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,写出其化学式:
(4)实验中常用K3[Fe(CN)6]检验Fe2+,K3[Fe(CN)6]中Fe3+的配位数为
(5)灰锡的晶体结构(如图3所示)与金刚石相似,其中A处原子的原子分数坐标为(0,0,0),则B处原子的原子分数坐标为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1。在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,原理为:2XCl+2CO+ 2H2O=X2Cl2·2CO·2H2O。
(1)X原子基态核外电子排布式为_______________ 。
(2)C、H、O三种元素的电负性由大到小的顺序为_______________ 。
(3)H2O中氧原子的轨道杂化类型为____________ 。
(4)化合物XCl晶体的晶胞如图所示,距离每个X离子最近的Cl的个数为__ 。

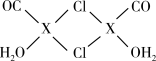
(5)X2Cl2·2CO·2H2O是一种配合物,结构如图所示,每个X原子能与其他原子形成3个配位键,在图中用“→"标出相应的配位键________ 。CO与N2分子的结构相似,则1 mol X2Cl2·2CO·2H2O含有σ键的数目为____________ 。
(1)X原子基态核外电子排布式为
(2)C、H、O三种元素的电负性由大到小的顺序为
(3)H2O中氧原子的轨道杂化类型为
(4)化合物XCl晶体的晶胞如图所示,距离每个X离子最近的Cl的个数为

(5)X2Cl2·2CO·2H2O是一种配合物,结构如图所示,每个X原子能与其他原子形成3个配位键,在图中用“→"标出相应的配位键

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】我国“嫦娥”五号首次实现地外天体采样返回,这是我国航天事业的又一突破。带回的月壤中含有H、N、O、Al、S、Cd、Zn、Ti、Cu、Au、Cr等多种元素。请完成下列问题:
(1)N、O、Al、S四种元素第一电离能从大到小的顺序为_______ 。
(2)Cu、Au是同一副族的元素,Au的原子序数更大,它们属于_______ 区元素,基态Au原子的价电子排布式为_______ 。
(3)SO2分子的空间构型为_______ ,请写出一种与SO2互为等电子体的单质_______ (填化学式)。
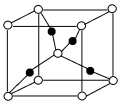
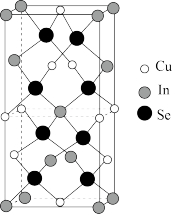
(4)某晶体的晶胞结构如图所示,该晶体的化学式为_______ 。如果将Se原子看做密堆积,则其堆积模型为_______ 。
(1)N、O、Al、S四种元素第一电离能从大到小的顺序为
(2)Cu、Au是同一副族的元素,Au的原子序数更大,它们属于
(3)SO2分子的空间构型为
(4)某晶体的晶胞结构如图所示,该晶体的化学式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】白云石的主要成分为 ,还含有少量的
,还含有少量的 和
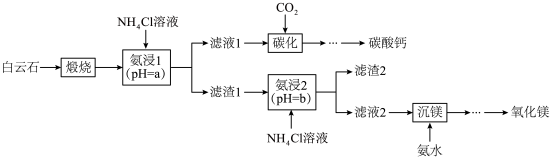
和 。利用白云石制备碳酸钙和氧化镁,其主要流程的示意图如下。
。利用白云石制备碳酸钙和氧化镁,其主要流程的示意图如下。
已知: 。
。
(1)组成 的四种元素,电负性由大到小的顺序是
的四种元素,电负性由大到小的顺序是___________ 。
(2)“氨浸1”在室温下进行,写出氯化铵浸取氧化钙总反应的离子方程式___________ 。
(3)两次“氨浸”的pH比较;a___________ b(填“>”“=”或“<”)。
(4)“碳化”时,测得碳酸钙的产率及碳酸钙中镁元素的含量随溶液pH的变化如图所示。
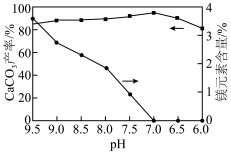

___________ 时,碳化效果最佳。低于该pH,碳酸钙的产率下降,其原因用离子方程式表示:___________ 。
(5)“沉镁”发生反应: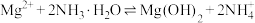 ,其平衡常数
,其平衡常数
___________ (用含氢氧化的 和
和 的
的 的代数式表示)。
的代数式表示)。
(6)制备过程除了充分利用 ,还可以循环利用的1种物质是
,还可以循环利用的1种物质是___________ (填化学式)。
(7)称取 试样置于烧杯中,加蒸馏水数滴润湿,盖一表面皿,滴加盐酸至固体完全溶解,定容在
试样置于烧杯中,加蒸馏水数滴润湿,盖一表面皿,滴加盐酸至固体完全溶解,定容在 的容量瓶内,用移液管吸取
的容量瓶内,用移液管吸取 待测液于锥形瓶中,加入相关试剂,摇匀后用
待测液于锥形瓶中,加入相关试剂,摇匀后用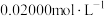 EDTA溶液滴定至终点(
EDTA溶液滴定至终点( 与EDTA以等物质的量比反应)。进行平行实验,测得平均消耗EDTA溶液
与EDTA以等物质的量比反应)。进行平行实验,测得平均消耗EDTA溶液 。产品中碳酸钙质量分数为
。产品中碳酸钙质量分数为___________ (列出计算式)。
(8)碳酸钙的某种晶胞结构如下图所示。

①每个晶胞中含有___________ 个“ ”单元。
”单元。
②每个阴离子团的配位数(紧邻的阳离子数)为___________ 。
 ,还含有少量的
,还含有少量的 和
和 。利用白云石制备碳酸钙和氧化镁,其主要流程的示意图如下。
。利用白云石制备碳酸钙和氧化镁,其主要流程的示意图如下。
已知:
 。
。(1)组成
 的四种元素,电负性由大到小的顺序是
的四种元素,电负性由大到小的顺序是(2)“氨浸1”在室温下进行,写出氯化铵浸取氧化钙总反应的离子方程式
(3)两次“氨浸”的pH比较;a
(4)“碳化”时,测得碳酸钙的产率及碳酸钙中镁元素的含量随溶液pH的变化如图所示。


(5)“沉镁”发生反应:
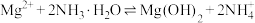 ,其平衡常数
,其平衡常数
 和
和 的
的 的代数式表示)。
的代数式表示)。(6)制备过程除了充分利用
 ,还可以循环利用的1种物质是
,还可以循环利用的1种物质是(7)称取
 试样置于烧杯中,加蒸馏水数滴润湿,盖一表面皿,滴加盐酸至固体完全溶解,定容在
试样置于烧杯中,加蒸馏水数滴润湿,盖一表面皿,滴加盐酸至固体完全溶解,定容在 的容量瓶内,用移液管吸取
的容量瓶内,用移液管吸取 待测液于锥形瓶中,加入相关试剂,摇匀后用
待测液于锥形瓶中,加入相关试剂,摇匀后用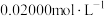 EDTA溶液滴定至终点(
EDTA溶液滴定至终点( 与EDTA以等物质的量比反应)。进行平行实验,测得平均消耗EDTA溶液
与EDTA以等物质的量比反应)。进行平行实验,测得平均消耗EDTA溶液 。产品中碳酸钙质量分数为
。产品中碳酸钙质量分数为(8)碳酸钙的某种晶胞结构如下图所示。

①每个晶胞中含有
 ”单元。
”单元。②每个阴离子团的配位数(紧邻的阳离子数)为
您最近一年使用:0次



