下列物质中的杂质(括号中)可用加热的方法除去的是
| A.Na2O2(Na2O) | B.Na2O(Na2O2) |
| C.CO2(CO) | D.KNO3(NaCl) |
更新时间:2017-08-24 19:46:49
|
相似题推荐
单选题
|
较难
(0.4)
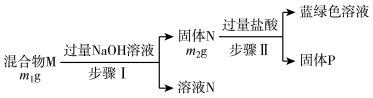
【推荐1】有8 g Na2O、Na2CO3、NaOH的混合物与200 g质量分数为3.65%的盐酸恰好反应,蒸干溶液,最终得固体质量为
| A.8 g | B.15.5 g | C.11.7 g | D.无法计算 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】相同温度下,分别将0.1mol Na、Na2O、Na2O2、NaOH加入盛有100mL水的甲、乙、丙、丁四个烧杯中并恢复至原温度,则甲、乙、丙、丁四烧杯中溶液的质量分数大小关系为 ( )
| A.丙>乙>丁>甲 | B.丁>甲>乙>丙 |
| C.乙=丙>甲>丁 | D.丁<丙<乙<甲 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列推断正确的是
| A.在化学反应中某元素由化合态变为游离态,该元素一定被还原了 |
| B.Na2O、Na2O2组成元素相同,阳离子与阴离子个数比也相同 |
| C.电子工业中,用三氯化铁溶液腐蚀铜箔印刷线路板,该过程发生了电化学腐蚀 |
| D.过量的铁与硝酸反应生成硝酸亚铁,过量的铁与氯气反应也生成氯化亚铁 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列指定微粒个数比不是2∶1的是
| A.Be2+离子中的质子和电子 | B.13H原子中的中子和质子 |
| C.NaHSO4晶体中的阳离子和阴离子 | D.Na2O2固体中的阳离子和阴离子 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】铁黄广泛用于建筑、涂料、橡胶、塑料等工业,工业上以硫酸渣(含Fe2O3、SiO2等)为原料制备铁黄(FeOOH)的一种工艺流程如下,下列说法错误的是
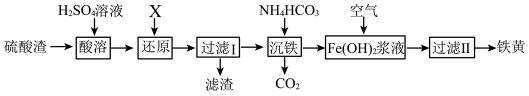

| A.“酸溶”工序适当加热可加快反应速率 |
| B.“还原”工序中加入的试剂X最好用铁粉 |
| C.若将“过滤Ⅰ”得到的溶液加热蒸干也能得到FeOOH |
| D.此工艺流程的副产物可作氮肥 |
您最近一年使用:0次
单选题
|
较难
(0.4)
真题
名校
【推荐2】利用如图所示的装置(夹持及加热装置略)制备高纯白磷的流程如下:

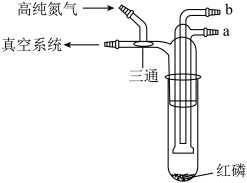
| A.红磷使用前洗涤以除去表面杂质 |
| B.将红磷转入装置,抽真空后加热外管以去除水和氧气 |
| C.从a口通入冷凝水,升温使红磷转化 |
| D.冷凝管外壁出现白磷,冷却后在氮气氛围下收集 |
您最近一年使用:0次
【推荐1】以高硫铝土矿(主要成分为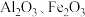 ,还含有少量
,还含有少量 )为原料,生产氧化铝并获得
)为原料,生产氧化铝并获得 的部分工艺流程如下,下列叙述不正确的是
的部分工艺流程如下,下列叙述不正确的是
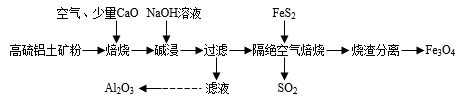
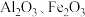 ,还含有少量
,还含有少量 )为原料,生产氧化铝并获得
)为原料,生产氧化铝并获得 的部分工艺流程如下,下列叙述不正确的是
的部分工艺流程如下,下列叙述不正确的是
A.隔绝空气焙烧时理论上反应消耗的 |
B.加入CaO可以减少 的排放同时生成建筑材料 的排放同时生成建筑材料 |
C.向滤液中通入过量 、过滤、洗涤、灼烧沉淀可制得 、过滤、洗涤、灼烧沉淀可制得 |
D.烧渣分离可以选择用磁铁将烧渣中的 分离出来 分离出来 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】工业以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3),其工业流程如图。下列说法错误的是


A.浸锰过程中Fe2O3与SO2反应的离子方程式为: Fe2O3+SO2+2H+=2Fe2++SO +H2O +H2O |
| B.过滤I所得滤液中主要存在的金属阳离子为Mn2+、Fe3+和Fe2+ |
| C.滤渣II的主要成分含有Fe(OH)3 |
D.过滤II所得的滤液中加入NH4HCO3溶液发生反应的主要离子方程式为: Mn2++2HCO =MnCO3↓+CO2↑+H2O =MnCO3↓+CO2↑+H2O |
您最近一年使用:0次