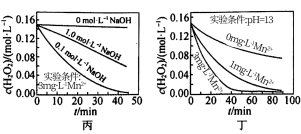
对H2O2的分解速率影响因素进行研究。在相同温度下,实验测得不同条件下出O2浓度随时间变化如图所示。下列说法不正确的是



| A.图甲表明,可通过适当增大H2O2浓度,加快H2O2分解速率 |
| B.图乙表明,可通过调节溶液的酸碱性,控制H2O2分解速率快慢 |
| C.图丙表明,Mn2+少量存在时,碱性太强,不利于H2O2分解 |
| D.图乙、图丙和图丁表明,Mn2+是H2O2分解的催化剂,提高Mn2+的浓度就能增大H2O2 分解速率 |
更新时间:2017-09-21 09:40:00
|
【知识点】 外因对化学反应速率影响的综合分析解读
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】探究 反应速率的影响因素,有关实验数据如下表所示:
反应速率的影响因素,有关实验数据如下表所示:
下列说法不正确的是
 反应速率的影响因素,有关实验数据如下表所示:
反应速率的影响因素,有关实验数据如下表所示:| 编号 | 温度/℃ | 酸性 溶液 溶液 |  溶液 溶液 |  的体积 的体积(mL) |  溶液褪色平均时间/min 溶液褪色平均时间/min | ||
| 体积/mL | 浓度/( ) ) | 体积/mL | 浓度/( ) ) | ||||
| 1 | 25 | 4 | 0.1 | 8 | 0.2 | 8 | 12 |
| 2 | 80 | 2 | 0.1 | 8 | 0.2 | a | b |
| 3 | 25 | 2 | 0.1 | 8 | 0.2 | 10 | c |
| A.a=10,b<c,6<c<12 |
B.可通过比较收集相同体积的 所消耗的时间来判断反应速率的快慢 所消耗的时间来判断反应速率的快慢 |
C.用 表示该反应速率,v(实验1)为 表示该反应速率,v(实验1)为 |
D.实验时可依次向试管中加入酸性 溶液、 溶液、 溶液和水 溶液和水 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】近似测定 氧化KI的瞬时速率公式
氧化KI的瞬时速率公式 与速率常数k的实验流程如下:
与速率常数k的实验流程如下:

加入KI后反应如下:① ;②
;②
在 耗尽时溶液变蓝色瞬间记录用时,测得不同起始浓度下反应时间、反应速率与反应速率常数如表所示:
耗尽时溶液变蓝色瞬间记录用时,测得不同起始浓度下反应时间、反应速率与反应速率常数如表所示:
下列说法正确的是
 氧化KI的瞬时速率公式
氧化KI的瞬时速率公式 与速率常数k的实验流程如下:
与速率常数k的实验流程如下:
加入KI后反应如下:①
 ;②
;②
在
 耗尽时溶液变蓝色瞬间记录用时,测得不同起始浓度下反应时间、反应速率与反应速率常数如表所示:
耗尽时溶液变蓝色瞬间记录用时,测得不同起始浓度下反应时间、反应速率与反应速率常数如表所示:| 实验编号 | 1 | 2 | 3 | 4 | 5 |
 溶液用量/mL 溶液用量/mL | 2.0 | 1.0 | 0.50 | 2.0 | 2.0 |
 溶液用量/mL 溶液用量/mL | 2.0 | 2.0 | 2.0 | 1.0 | 0.50 |
 溶液用量/mL 溶液用量/mL | 0 |  | 1.5 | 1 | 1.5 |
| 反应时间/s | 37 | 68 | 133 | 72 | 139 |
反应速率 | 2.0 | 1.1 | 0.5 | 1.0 | 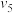 |
反应速率常数 | 3.4 | 3.8 | 3.4 | 3.4 | 4.0 |
A.上表中的速率为 完全消耗后测得的平均速率 完全消耗后测得的平均速率 |
B.由实验可知反应的速率公式为 |
C.表中数据 , ,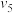 约为0.5 约为0.5 |
| D.实验测得的5组反应速率常数不完全相等,说明浓度对k有影响 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】下列实验操作与现象和对应结论均正确的是
| 实验操作与现象 | 结论 | |
| A | 加热盛有少量 固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变蓝。 固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变蓝。 | 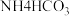 显碱性 显碱性 |
| B | 向某溶液中先加入氯化钡溶液,再滴入盐酸,先产生白色沉淀,后白色沉淀不消失。 | 该溶液中可能含有 |
| C | 其他条件相同的情况下,两只试管中均加入10ml,2mol/L的酸性 ,第一只试管中加入10ml,2mol/L的 ,第一只试管中加入10ml,2mol/L的 ,第二只试管中加入10ml,4mol/L的 ,第二只试管中加入10ml,4mol/L的 ,观察第二只试管褪色更快。 ,观察第二只试管褪色更快。 | 浓度越大,反应速率越大 |
| D | 向2支盛有2mL不同浓度 溶液的试管中同时加入1mL2% 溶液的试管中同时加入1mL2% 溶液,未观察到明显的实验现象差异。 溶液,未观察到明显的实验现象差异。 | 浓度对反应速率的影响不大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



