根据下列实验事实,不能得到相应结论的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向醋酸溶液中滴加少量Na2SiO3溶液,观察到白色沉淀 | 醋酸的酸性强于H2SiO3 |
| B | 向均盛有2mL5% H2O2溶液的两支试管中分别滴入0.2mol/LFeCl3和0.3mol/LCuCl2溶液各1mL,前者生成气泡的速率更快 | 催化效果: Fe3+> Cu2+ |
| C | 向一定浓度的醋酸溶液中加入镁条,产生气泡的速率会先加快再减慢 | 反应产生气泡速度变化,是因为醋酸电离平衡先正向移动,再逆向移动 |
| D | 常温下分别测等浓度的醋酸和氨水pH,二者的pH 分别为2和12 | 常温下,醋酸和氨水的电离平衡常数相等 |
| A.A | B.B | C.C | D.D |
更新时间:2018-01-03 19:16:24
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】日常生活中,下列做法与化学反应速率无关的是
| A.在铁制品表面刷油漆 | B.向 溶液中加入 溶液中加入 制取 制取 |
| C.面团放在温热处发酵 | D.在糖果制作过程中添加着色剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验操作,能有效改变反应速率且达到变化要求的是
| A.为增大泡沫灭火器中Al2(SO4)3与小苏打的反应速率,改用小苏打和苏打的混合物 |
| B.为加快盐酸和过量锌粒制取氢气的速率又不减少氢气的量,可加少量硝酸银溶液 |
| C.在稀硫酸和铁粉反应制取氢气时,为减慢反应速率,可以加入适量醋酸钠 |
| D.用3 mL乙醇、2 mL浓H2SO4、2 mL冰醋酸制乙酸乙酯,为增大反应速率,可改用6 mL乙醇、4 mL浓H2SO4、4 mL冰醋酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列实验能达到目的的是
| 实验目的 | 实验方法或操作 | |
| A | 测定中和反应的反应热 | 酸碱中和滴定的同时,用温度传感器采集锥形瓶内溶液的温度 |
| B | 探究浓度对化学反应速率的影响 | 量取同体积不同浓度的NaClO溶液,分别加入等体积等浓度的Na2SO3溶液,对比现象 |
| C | 判断反应后Ba2+是否沉淀完全 | 将Na2CO3溶液与BaCl2溶液混合,反应后静置,向上层清液中再加1滴Na2CO3溶液 |
| D | Ksp(AgCl)>Ksp(AgI) | 向2 mL 0.1 mol•L-1AgNO3溶液中滴加2滴0.1 mol•L-1NaCl溶液,观察现象。振荡试管,再滴加4滴0.1 mol•L-1KI溶液,观察现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在较低温度下可发生反应:
 ,其正反应速率方程为
,其正反应速率方程为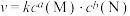 ,T℃时,实验得到了起始反应速率的一组数据如下表所示:
,T℃时,实验得到了起始反应速率的一组数据如下表所示:
下列说法不正确的是

 ,其正反应速率方程为
,其正反应速率方程为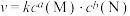 ,T℃时,实验得到了起始反应速率的一组数据如下表所示:
,T℃时,实验得到了起始反应速率的一组数据如下表所示:| 实验组别 | M起始浓度/( ) ) | N起始浓度/( ) ) | 起始时的正反应速率/( ) ) |
| Ⅰ | 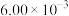 | 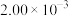 | 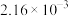 |
| Ⅱ | 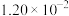 | 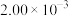 | 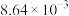 |
| Ⅲ | 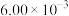 | 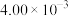 | 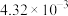 |
| A.正反应为放热反应 | B. , , |
| C.k的数值为30000 | D.升高温度,k的值减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室利用下列方案探究影响化学反应速率的因素,有关说法不正确的是
| 实验编号 | 温度/℃ | 酸性KMnO4溶液 | 乙醛(CH3CHO)溶液 |
| ① | 25 | 4mL0.01 mol∙L-1 | 2 mL 0.01 mol∙L-1 |
| ② | a | 4 mL 0.01 mol∙L-1 | 2 mL 0.02 mol∙L-1 |
| ③ | 50 | 4 mL 0.01 mol∙L-1 | 2 mL 0.01 mol∙L-1 |
| ④ | b | c | 2 mL 0.01 mol∙L-1 |
| A.a=25 |
| B.实验①③探究的是温度对化学反应速率的影响 |
| C.实验中需记录溶液颜色变化所需时间 |
| D.若b=25,c=4mL0.02 mol∙L-1,则实验①④也可用于化学反应速率影响因素的探究 |
您最近一年使用:0次
单选题
|
适中
(0.65)
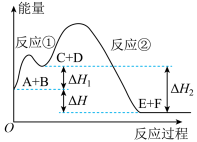
【推荐1】已知反应Ⅰ和反应Ⅱ的反应原理及反应进程中能量变化如下:
Ⅰ.

Ⅱ.

下列说法正确的是

Ⅰ.


Ⅱ.


下列说法正确的是

A. | B.反应Ⅰ的反应速率大于反应Ⅱ的反应速率 |
C.反应Ⅱ正反应的活化能为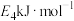 | D.加入合适催化剂后 、 、 、 、 均会降低 均会降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】氮及其化合物的转化过程如图所示。下列分析不合理的是
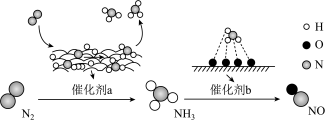

A. 与 与 反应生成 反应生成 的原子利用率为100% 的原子利用率为100% |
| B.催化剂a表面发生反应时,不涉及电子转移 |
| C.在催化剂b表面发生了极性共价键的断裂和形成 |
| D.催化剂a、b能加快反应的反应速率 |
您最近一年使用:0次